JACS:含季碳中心β-氨基酸酯的光化学合成新方法
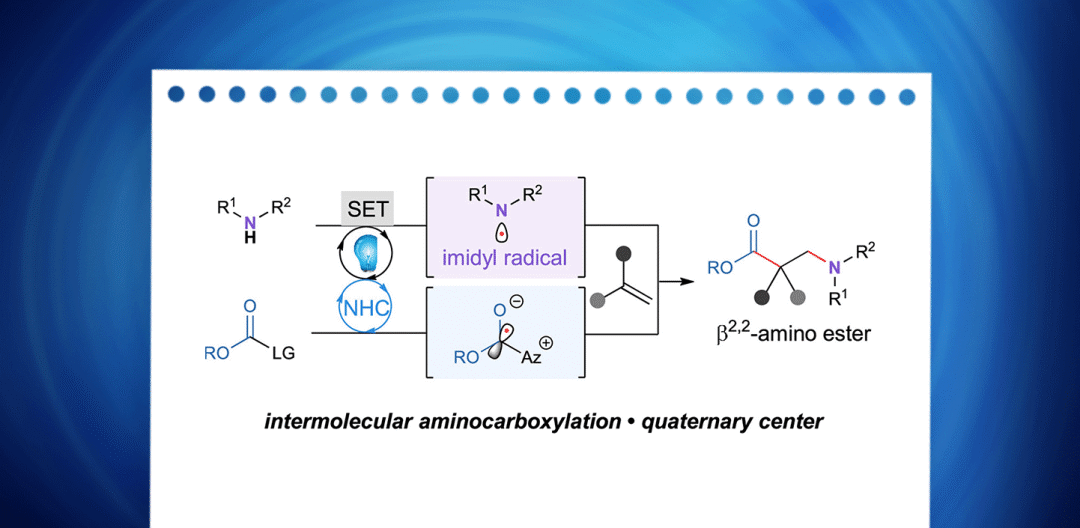
最近,美国西北大学(Northwestern University)Karl A. Scheidt课题组报道了NHC和光催化剂联合催化的光促烯烃氨羧基化反应,可以实现多种含季碳中心β-氨基酸酯的高效合成。相关研究成果发表在近期的《美国化学会志》上(J. Am. Chem. Soc. DOI: 10.1021/jacs.3c09875)。在该反应中,酰亚胺发生去质子化和单电子氧化生成氮中心自由基,然后和偕二取代烯烃发生区域选择性加成,生成三级碳自由基,再和稳定的原位生成azolium型自由基发生自由基偶联,构建起季碳中心,得到β-氨基酸酯。
背景介绍(Figure 1):
β-氨基酸是生物活性分子和天然产物中存在的一类特殊化学片段,能够转化成γ-氨基醇、β-内酰胺等重要片段,因此吸引着众多合成化学家的注意力(Figure 1A)。此外,有报道证明,β-氨基酸和肽结合,能改善肽的稳定性和生物活性。根据取代基不同,β-氨基酸可被分为β3-、β2-、β2,3-、β3,3-和β2,2-氨基酸。β2,2-氨基酸的ɑ-位含季碳立体中心,是其中最难合成的一类。β-氨基酸的经典合成方法包括:Mannich反应、含氮亲核试剂的共轭加成、β-氨基-ɑ,β-不饱和化合物的加氢还原、α-氨基酸的Arndt−Eistert同系化。Mannich反应是其中研究最多的合成方法,包括最近报道的基于手性磷酸或NHC催化剂的对映选择性合成方法。然而,这些方法中的大多数得到的是β3-、β2-、β2,3-型氨基酸。发展出能够合成β2,2-氨基酸的通用合成方法仍然极具挑战性。
光化学催化已成为一种重要的有机合成策略,可以将传统双电子化学无法断裂的键断裂。最近发展出的光化学方法能够获取氮中心自由基(NCRs),有助于发展出含氮化合物的光化学合成方法。但是,相比碳中心自由基,获取NCRs的方法仍然有限。已报道的光化学方法是利用质子耦合电子转移PCET(Knowles组报道)、ɑ-剪切(Knowles组报道)、SET(Studer和Leonori组报道)、三线态能量转移EnT(Glorius组报道)等策略,将NCR前体N-X化合物转化成NCRs(Figure 1B)。然而,使用无机碱将简单的酰亚胺转化成NCR并用于含氮化合物制备,目前还尚未有报道。除了能用于NCRs的获取,光化学方法还能应用于C-C键的构建。基于NHC的自由基中间体能够有效促进自由基偶联,有助于构建新的C-C键。基于此,Karl A. Scheidt课题组计划利用NHC/光催化剂双催化体系,经酰亚胺前体生成NCRs,并和焦碳酸二乙酯和苯乙烯化合物发生偶联,生成β2,2-氨基酸酯(Figure 1C)。
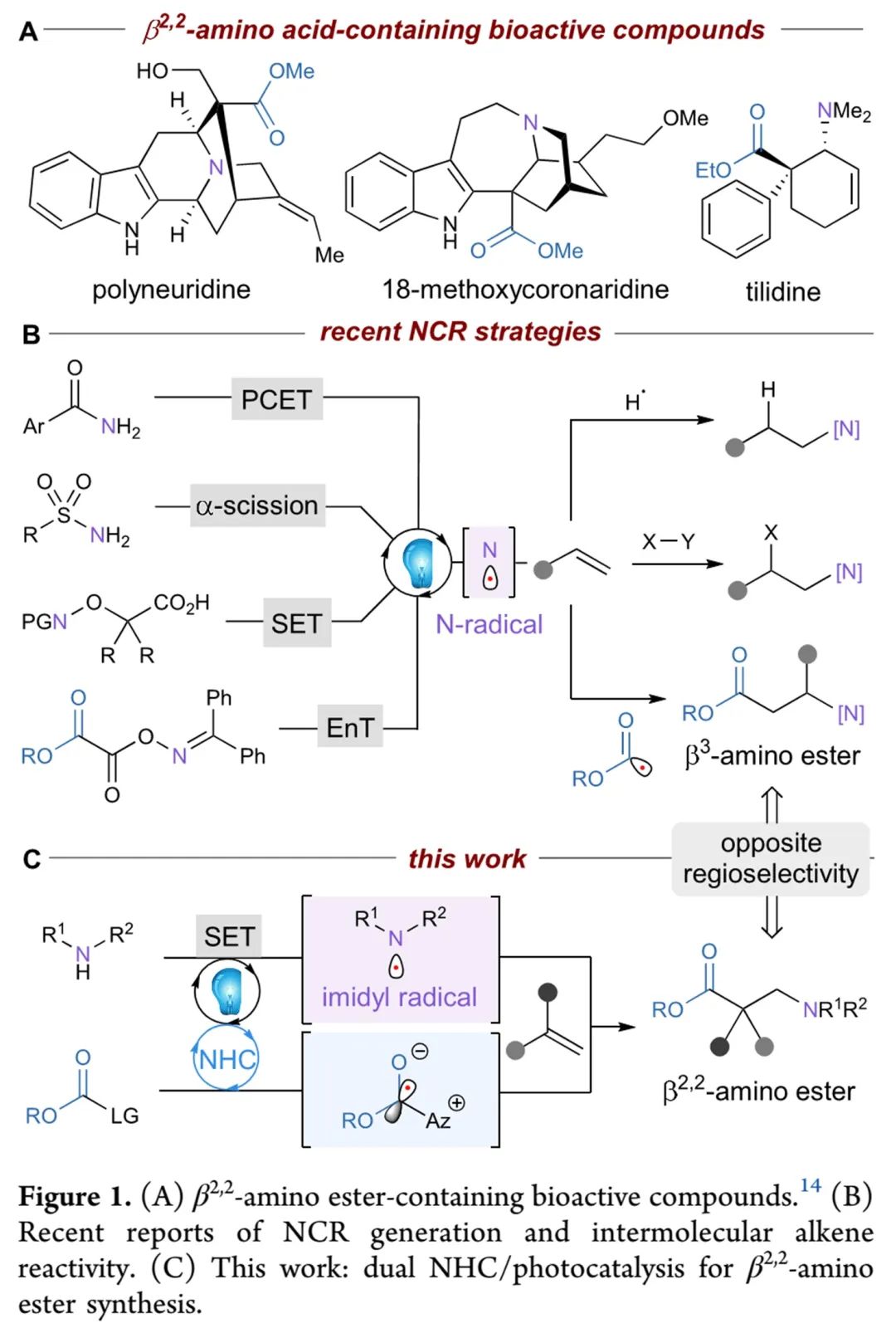
(Figure 1, 来源:J. Am. Chem. Soc.)
条件筛选研究(Table 1):
作者首先以 N-Boc-苯甲酰胺(1a)为酰亚胺底物、焦碳酸二乙酯(2a)为羧基源、α-甲基苯乙烯(3a)为烯烃底物开展反应可行性研究。如Table 1所示,通过对NHC催化剂Az、光催化剂PC、碱、溶剂等影响因素进行细致优化,得出如entry 1和entry 6所示最优反应条件:Az-1/PC-1作催化剂、碳酸钾或碳酸铯作碱、乙腈作溶剂、blue LEDs作光源,反应能以99%的高产率得到β2,2-氨基酸酯4a。控制实验显示(entries 11-14 in Table 1),NHC催化剂、光催化剂、光照和碱对此反应至关重要缺一不可。此外,氧气和水会显著降低反应产率,温度和光源距离也会降低反应产率。
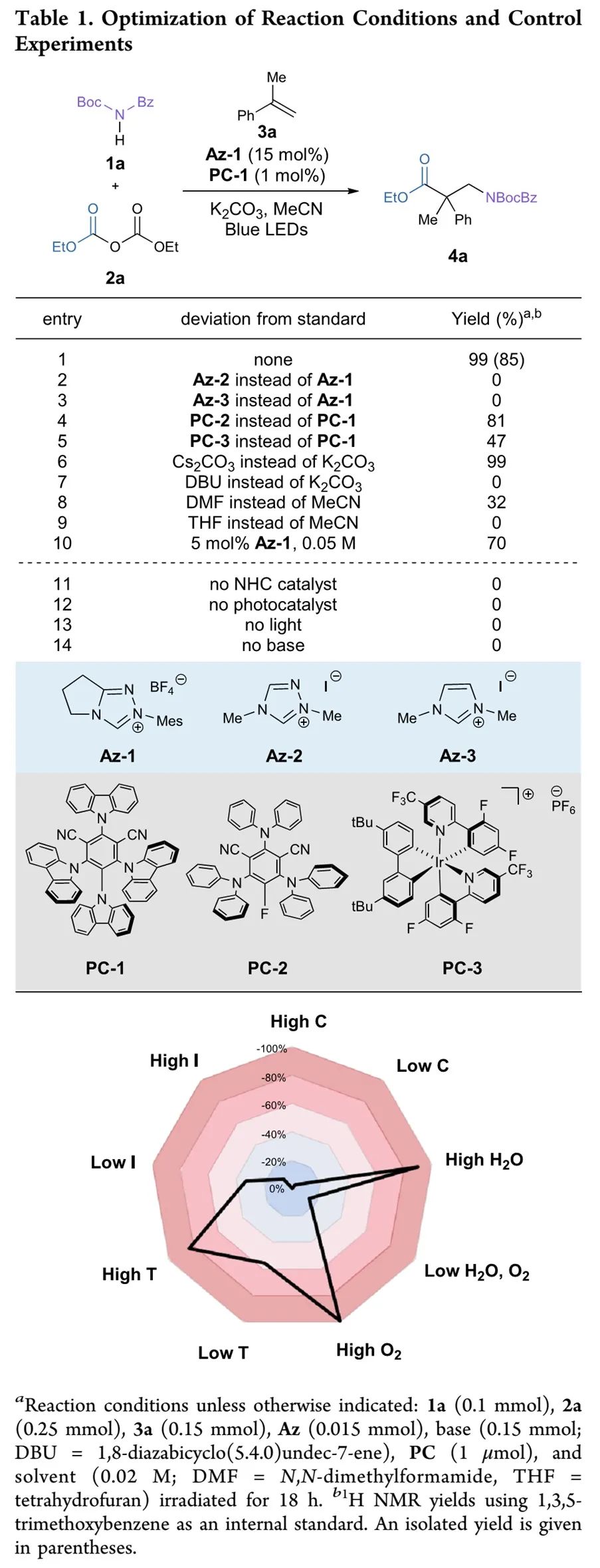
(Table 1, 来源:J. Am. Chem. Soc.)
底物拓展和应用(Table 2):
基于Table 1优化出的反应条件,作者接着开展底物拓展研究。研究结果显示,两种焦碳酸二酯2、多种芳基烯烃底物3和酰亚胺底物1都兼容该反应,能以可观产率得到对应产物4a-4z、4aa-4ab(Table 2)。所拓展的底物包括:1)焦碳酸二乙酯和焦碳酸二异丙酯;2)苯乙烯,带供电子或吸电子基团的α-甲基苯乙烯,α-位带乙基、正丁基、乙酰氧基的苯乙烯,双环类苯乙烯,带萘基、吡啶基的α-甲基芳乙烯,二芳基乙烯,1,3-二烯烃,1-苯丙烯等烯烃底物;3)带多种酰基基团的酰亚胺底物,包括药物分子ataluren、probenecid。此外,4a可通过肼还原选择性脱去Bz,得到β-氨基酸酯5,也可通过氢化铝锂还原,得到γ-氨基醇6,提高了该反应应用价值。
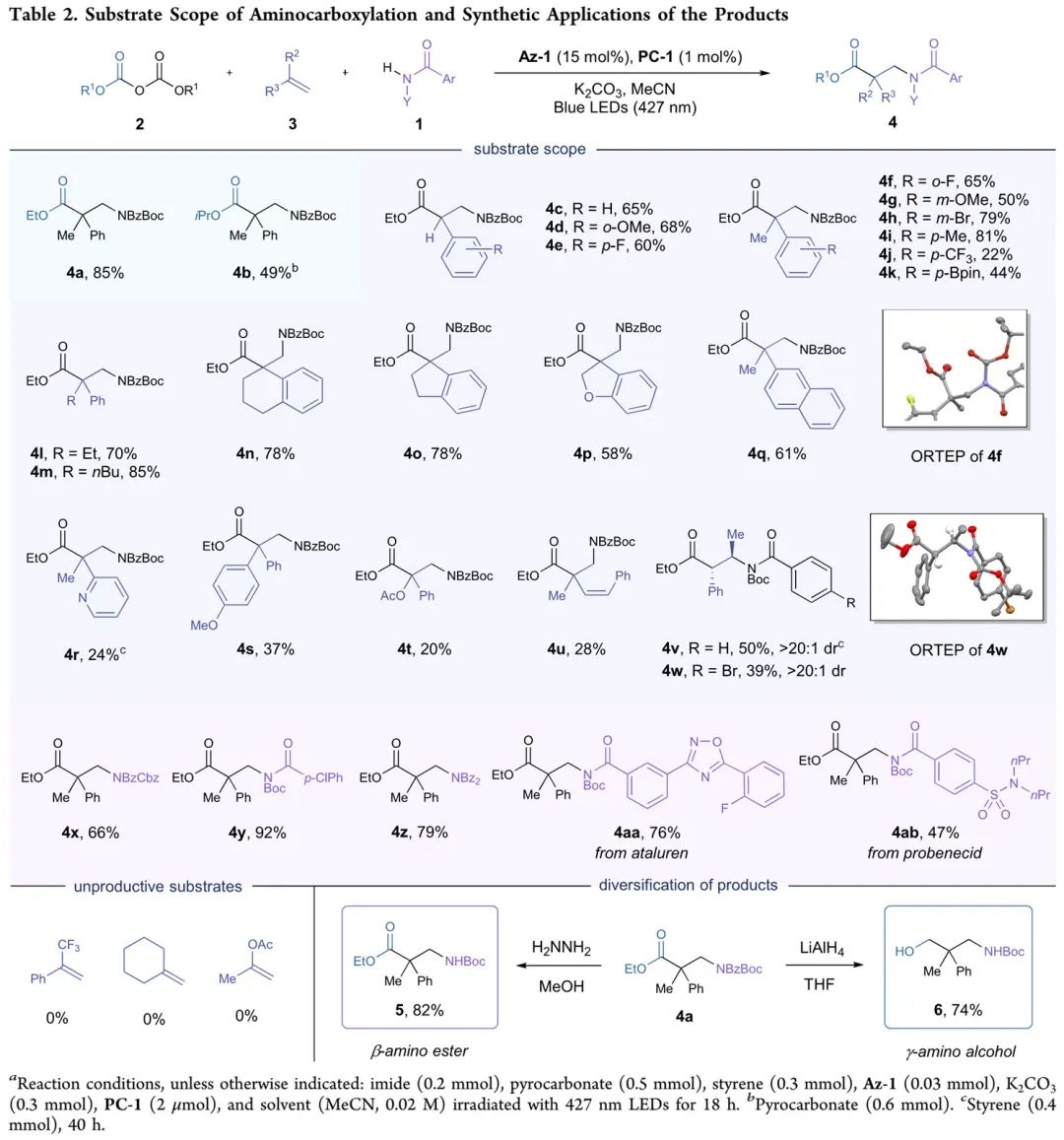
(Table 2, 来源:J. Am. Chem. Soc.)
反应机理研究(Scheme 1):
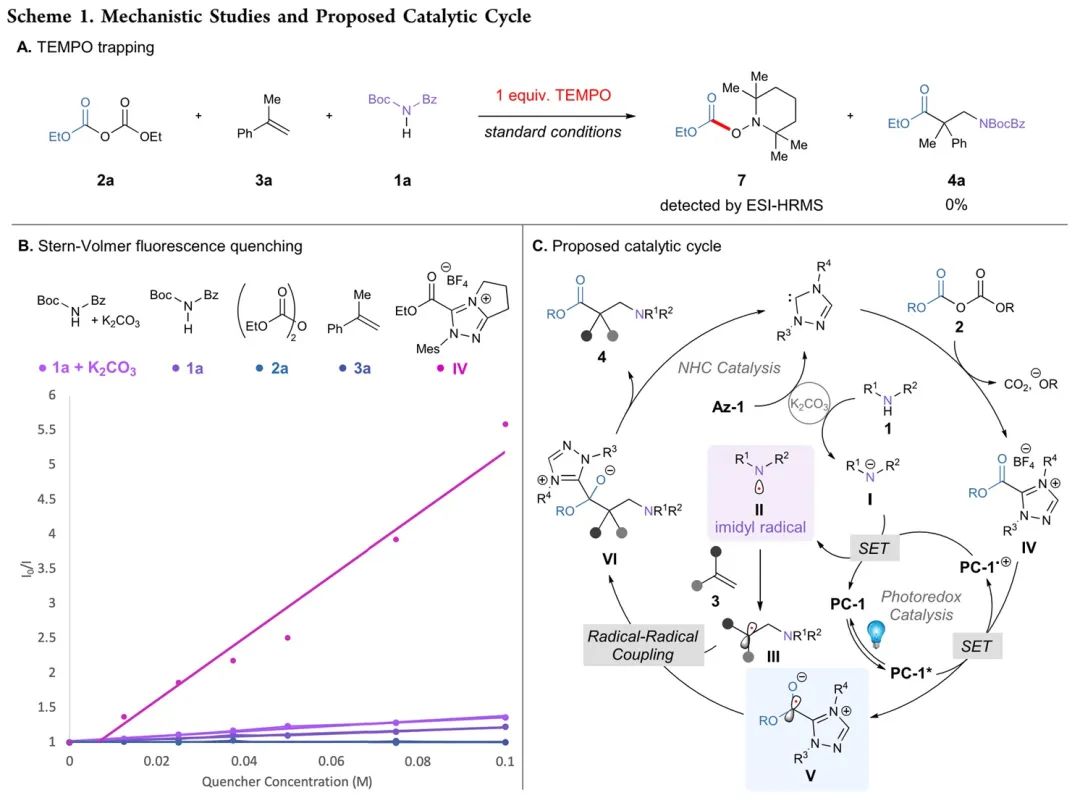
最后,作者探索了该反应的可行性反应机理。首先,Table 1中的控制实验显示,NHC催化剂、光催化剂、光照和碱对反应至关重要缺一不可(entries 11-14 in Table 1)。其次,TEMPO自由基捕捉实验显示,反应是通过自由基机理发生反应(Scheme 1A)。此外,循环伏安法研究证实,1a和K2CO3反应生成的酰亚胺负离子中间体I的氧化电势Eox比1a更低,因此中间体I更易被氧化(pp S28−S30 in SI)。最后,利用Stern−Volmer荧光淬灭实验,作者发现中间体IV最易被淬灭(比率最大),因此可能经历氧化淬灭机理;酰亚胺1a和1a/K2CO3反应物I有较小的淬灭比值,因此也不能排除还原淬灭途径。2a和3a底物则无法淬灭,因此反应不会由2a或3a先生成自由基。
基于这些探索实验,结合已报道研究工作,作者提出了如Scheme 1C所示可行性反应机理:NHC催化剂和焦碳酸二乙酯2a发生去质子化/亲核加成反应,生成中间体IV;IV被激发态光催化剂还原(SET),生成自由基V;同时,酰亚胺底物1和碱所生成的酰亚胺负离子I,可被氧化成氮中心自由基II;II会被烯烃3快速捕获,生成苄基自由基III;自由基III和V可发生自由基偶联,生成中间体VI;VI裂解生成β2,2-氨基酸酯4,并再生NHC催化剂,完成这个循环。
(Scheme 1, 来源:J. Am. Chem. Soc.)
总之,Karl A. Scheidt课题组以苯乙烯、酰亚胺、焦碳酸二乙酯三种化合物为原料,实现β2,2-氨基酸酯的温和模块化光化学合成。该研究工作利用了分子间氮中心自由基接力策略,并首次将NHC/光催化剂体系应用于羧基化合物的合成。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





