南京大学王毅、潘毅课题组:光催化不饱和烃高立体和区域选择性的磺酰氟邻位硼化物的构建
硫(VI)氟化物交换(SuFEX)化学作为新一代点击反应,依赖于高价有机硫独特的反应活性-稳定性平衡,在近几年引起了广泛的研究兴趣。近年来,在有机分子中快速安装单个磺酰氟基团的方法已经发展的较多了;然而,含有磺酰氟基团的双功能分子的构建,其合成多功能性可能为药物发现提供了巨大的合成价值和机会,目前还很少被报道。磺酰氟邻位的硼化物作为一种潜在的含磺酰氟基团的双功能分子,由于系统的不兼容性和有限的合成策略,直接光氧化催化的磺酰氟-硼化过程仍未被开发,且很具有挑战性。基于此,南京大学王毅、潘毅课题组发展了一种顺序光催化自由基双官能化策略,利用一种集成的氧化还原活性 SO2F 自由基试剂(IMSF)高效立体选择性地合成了磺酰氟硼化物(VFSB)。通过 C-B 键和 S(VI)-F 键的裂解,磺酰氟硼化物(VFSB)作为正交合成子进行了一系列便捷的转化,包括卤化、铃木偶联、氢化和 SuFEX 点击反应,这表明磺酰氟硼化物(VFSB)分子在骨架连接和药物改性方面具有巨大的潜力。相关成果在线发表于Chem. Sci.(DOI: 10.1039/D3SC03101B)。
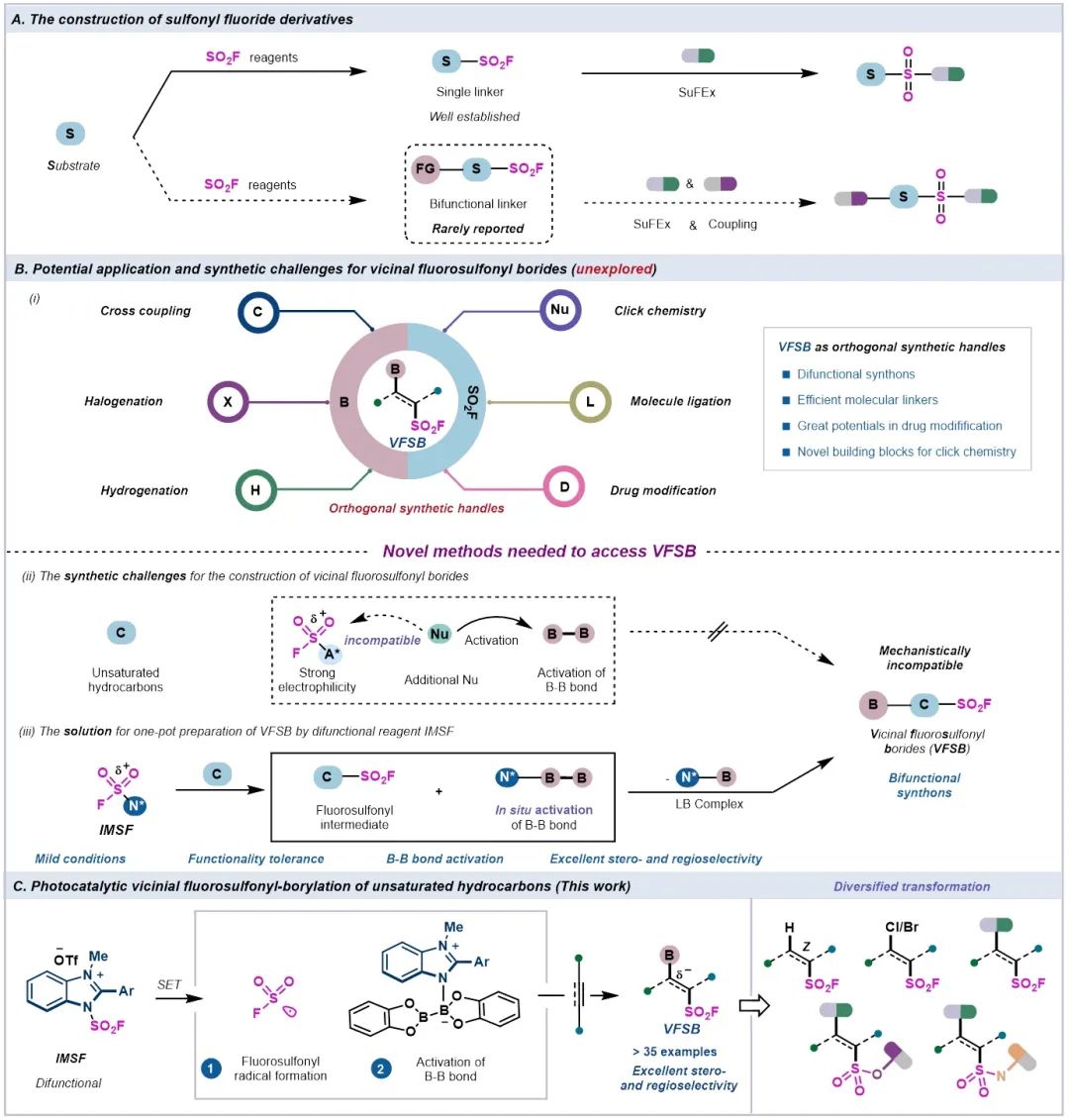
王毅、潘毅教授课题组一直致力于有机氟化学的研究,在廉价氟源的活化方面取得了一系列研究进展(Angew. Chem. Int. Ed. 2019, 58, 624–627; Org. Lett. 2019, 21, 1857-1862; Nat. Commun. 2020, 11; Chem. Sci. 2021, 12 , 2509-2514, 2572; Nat. Commun. 2022, 13, 3515; Chem. Sci. 2022, 13, 11312-11319; J. Fluorine Chem. 2023, 268, 110114.)。近期,该课题组利用廉价的硫酰氟(SO2F2)气体设计并合成了一种稳定、廉价、高活性的磺酰氟咪唑盐试剂(IMSF)。利用这种氧化还原活性盐试剂作为磺酰氟自由基源,在光催化条件下,试剂产生磺酰氟自由基的同时也代谢了相应的咪唑残基,咪唑残基可以高效的活化B2Cat2,从而首次实现了一系列磺酰氟邻位硼化物(VFSB)的构建,且利用磺酰氟-硼化物进行了一系列分子的修饰和拼接;这为分子的骨架连接和药物改性方面提供了新思路(Figure 1)。
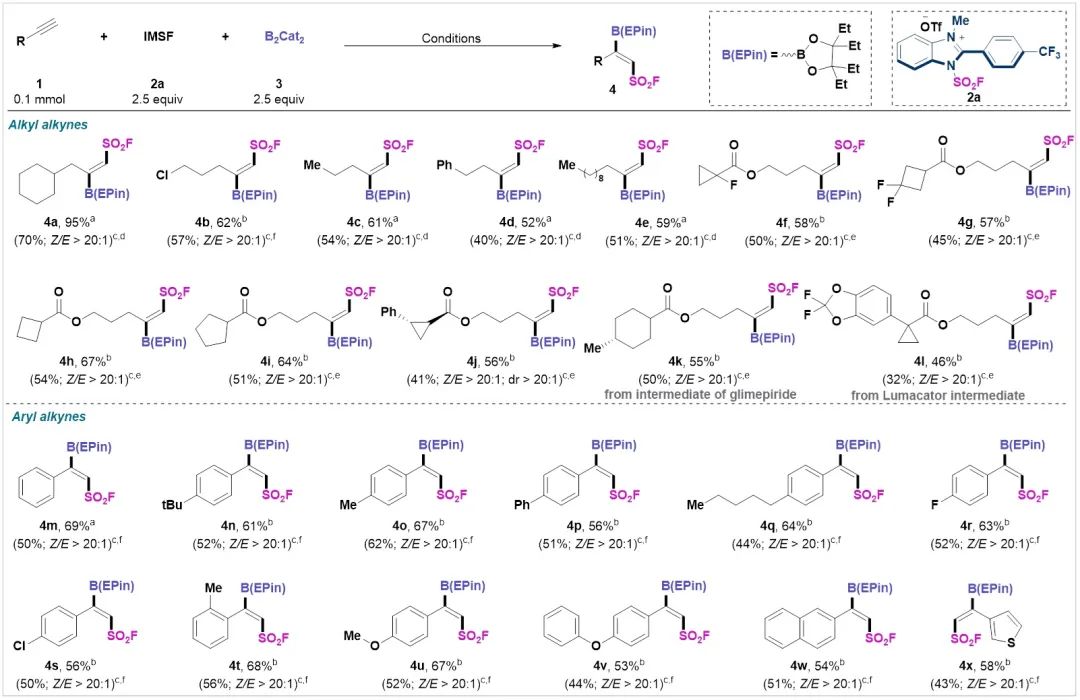
首先,作者通过对咪唑盐试剂、溶剂、光催化剂等一系列反应条的优化,最终确定了该反应的最优条件,在最优条件下作者对底物的适应范围进行了考察,如图Figure 2所示。含有卤化物、芳烃和脂肪族的末端炔烃可以均匀地提供目标产物(4a-4e),收率适中(52%-62%),且立体选择性高。随后,作者扩展了各种含有饱和碳环结构的炔烃的底物范围;对于环丙基和环丁基衍生化底物,特别是氟化环丙基和环丁基衍生化炔烃,可以以中等至良好的收率提供相应的磺酰氟硼化物(4f-4h,4j)。该反应还可用于饱和五元碳环衍生化炔烃,并以64%的收率得到(Z)-选择性磺酰氟硼酸酯4i。作者还选择了许多含有天然药物分子的炔烃来测试磺酰氟硼化过程。格列美脲、鲁马卡托衍生的末端炔烃以中等收率和高立体选择性提供磺酰氟硼化产物(4k-4l)。同时,作者还将这种磺酰氟硼化方案扩展到一系列芳基炔烃上;具有吸电子或给电子取代基的芳基炔烃可以以高立体和区域选择性(Z /E > 20:1)和高收率生成所需的产物4m-4v。萘基和噻吩基取代的炔烃也很容易转化为磺酰氟硼化产物4w和4x,且产率中等。
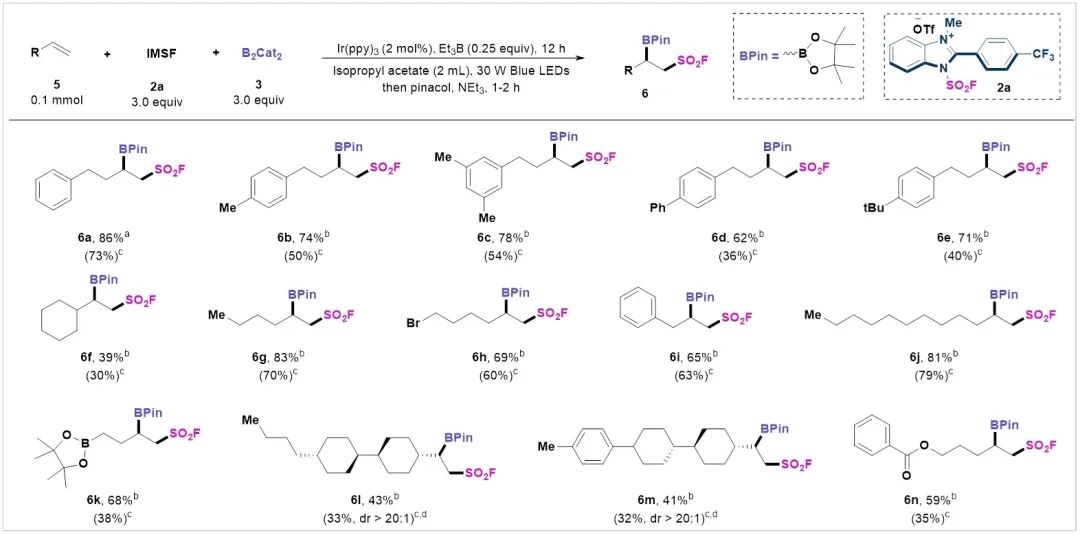
磺酰氟邻位的烷基硼化物在药物设计和生物偶联的相关领域也是有用的双功能合成子。因此,作者还将这种自由基磺酰氟硼化方案应用于了磺酰氟邻位烷基硼化物的构建。通过对条件的进一步优化,作者将这种自由基磺酰氟硼化策略扩展到一系列未活化的烯烃(Figure 3)。首先,芳基取代的丁烯衍生物可以得到目标产物6a-6e且收率达到中等至良好(62%-86%)。1-乙烯基环己烷、烯丙基苯和十二烯也与反应体系相容,并以中等至良好的收率(39%-81%)生成所需的产物(6f,6i-6j)。含有硼酸盐取代基的烯烃也可以被耐受并转化为所需的产物6k。值得注意的、源自液晶砌块的单取代烯烃,如反式、反式-4-丁基-4'-乙烯基双环己基和4-对甲苯基-4'-乙烯基双(环己烷),可提供中等产率的磺酰氟烷基硼化物(6l和6m)。此外,在该反应条件下还耐受末端烯烃的含酯官能团,并且可以顺利获得所需的产物(6n)。
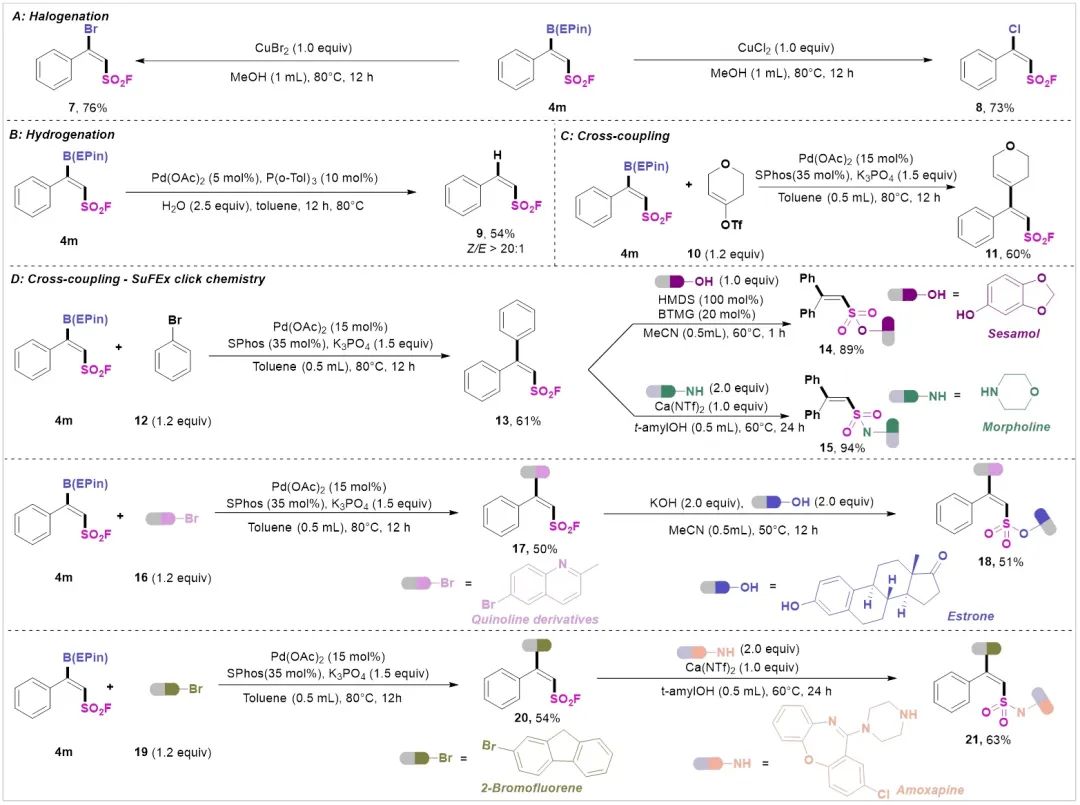
为了证明VFSB的合成价值,作者还进行了磺酰氟硼化物的衍生化反应(Figure 4)。用溴化铜或氯化铜和4m反应,可以得到β-溴烯基磺酰氟7或β-氯烯基磺酰氟8。钯催化加氢反应可以使4m以高Z/E比(>20:1)提供所需产物9。钯催化的Suzuki-Miyaura使吡喃酮衍生的三氟甲磺酸酯10及溴苯12与4m的交叉偶联反应顺利发生,且可以得到相应的三取代烯烃11(60%)和13(61%)。众所周知,磺酰氟物种还可以很容易地发生各种SuFEX反应以连接其他分子,因此,作者尝试了磺酰氟产物13与芝麻酚和吗啉的连接,并获得了理想的磺酸酯产物14和磺酰胺产物15,且收率极高。最后,为了验证VFSB的连续功能化,作者将4m与喹啉衍生物和雌酮进行了序列偶联,获得了双官能团化作用的产物18。此外,4m与2-溴芴和阿莫沙平的顺序连接以高效率提供了产物21。
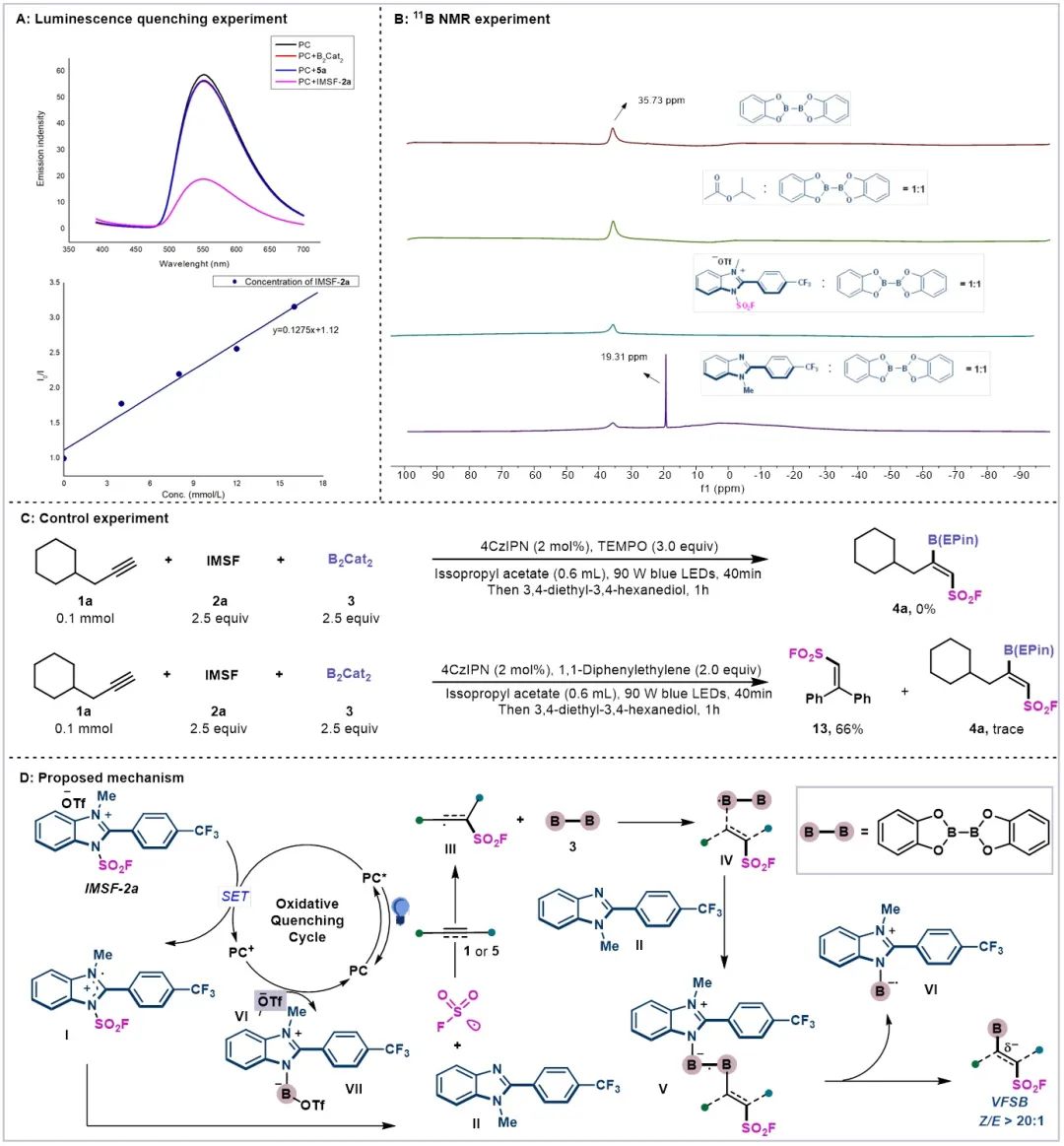
Figure 5. Mechanistic studies and proposed mechanism.
为了深入了解这种反应,作者进行了机理实验(Figure 5)。首先,荧光猝灭实验揭示了光激发PC*可以被IMSF-2a猝灭,因此催化循环可能涉及氧化猝灭催化循环(Figure 5A)。然后,11B NMR实验表明,只有原位生成的咪唑残基才能活化二硼试剂,新生成的峰为19.31 ppm(Figure 5B)。最后,使用3个当量的TEMPO的自由基捕获实验抑制了自由基加成。同时,在标准条件下加入1,1-二苯乙烯仅得到微量产物4a;并且以66%的收率分离自由基捕获产物13(Figure 5C)。从上述机理实验中,作者推测了反应可能的机理(Figure 5D):首先,在光照下,阳离子试剂2a可以通过激发态光催化剂(PC*)还原生成自由基中间体I,并释放出SO2F自由基和咪唑残基II。然后,在炔烃和SO2F自由基的自由基加成反应区域选择性地提供乙烯基自由基中间体III。随后乙烯基自由基III与B2Cat2作用得到Z-乙烯基二硼自由基物种IV。中间体的立体选择性的控制受氟磺酰基和硼酸盐之间的空间排斥作用影响。然后,通过原位生成的咪唑残基II活化二硼试剂,形成高反应性B-N中间体V,从而产生所需的双功能产物4或6和咪唑稳定的硼基自由基物种VI。最后,VI被光氧化,然后与−OTf偶联,得到硼基咪唑盐VII并再生光催化剂。
综上所述,王毅、潘毅课题组首次在温和条件下成功实现了使用磺酰氟咪唑盐作为双功能试剂,去完成了不饱和烃的磺酰氟硼化反应。高活性阳离子试剂IMSF可通过SET过程生成SO2F自由基,同时原位生成咪唑残基,可以使B-B键活化。磺酰氟硼化物(VFSB)作为磺酰氟与硼酸盐的组合分子,可为不同药物分子的选择性组装提供强大方案。基于VFSB的多功能性,使其可以很容易地实现硼化物和磺酰氟的衍生化,这显示了VFSB在合成、生物偶联和药物工具开发中的优越相容性和潜在的广泛应用性。
本文第一作者为博士研究生李和寅,通讯作者为张为钢博士和王毅教授。该工作得到国家自然科学基金(21971107, 2201101, 22271147)、中国博士后科学基金(2021T140309、2021M691511)、配位化学国家重点实验室、江苏省先进有机材料重点实验室的经费资助。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





