ACS Catal.:光诱导Ni(II)催化芳基溴的选择性氰化或氰甲基化
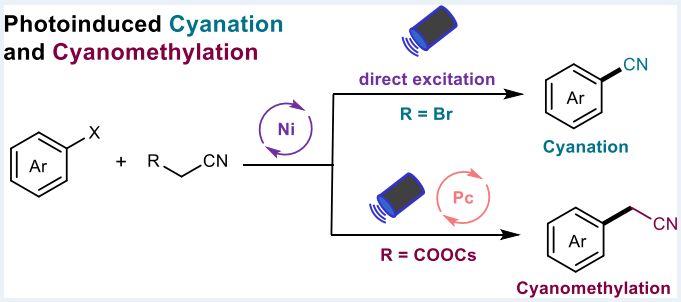
前言
氰基作为一类重要的官能团,普遍存在于药物分子、农药分子及功能材料分子中。传统合成腈类化合物的方法有:(i)由Rosenmund von Braun 反应和Sandmeyer 反应合成芳基腈;(ii)过渡金属催化芳基亲电试剂与氰化试剂的偶联反应(图1b)。然而,这类催化体系需要使用有毒的氰化试剂,而且容易导致催化剂失活。因此,寻找新型氰化试剂用于腈类化合物的合成具有重大挑战。基于此,阿卜杜拉国王科技大学Magnus Rueping团队在其前期光催化反应研究基础上,报道了光诱导Ni(II)催化芳基溴的选择性氰化或氰甲基化反应DOI:10.1021/acscatal.3c04745(图1)。
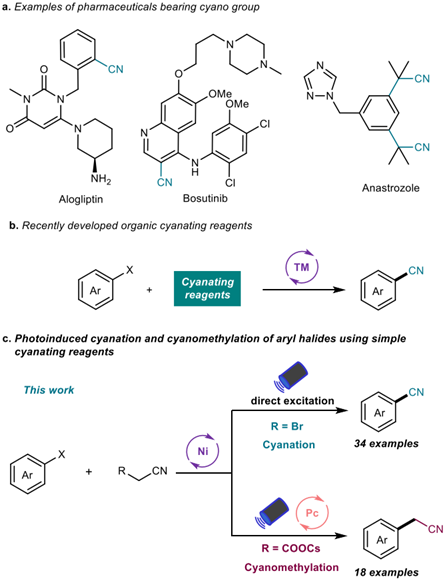
图1来源ACS Catal.
实验结果
作者在实验过程中发现,以市售的溴乙腈为氰基源,NiBr2·dtbbpy 为催化剂,440 nm蓝色LED为光源,能够实现溴乙腈的脱甲基氰化反应,并对底物进行了普适性考察(图2)。
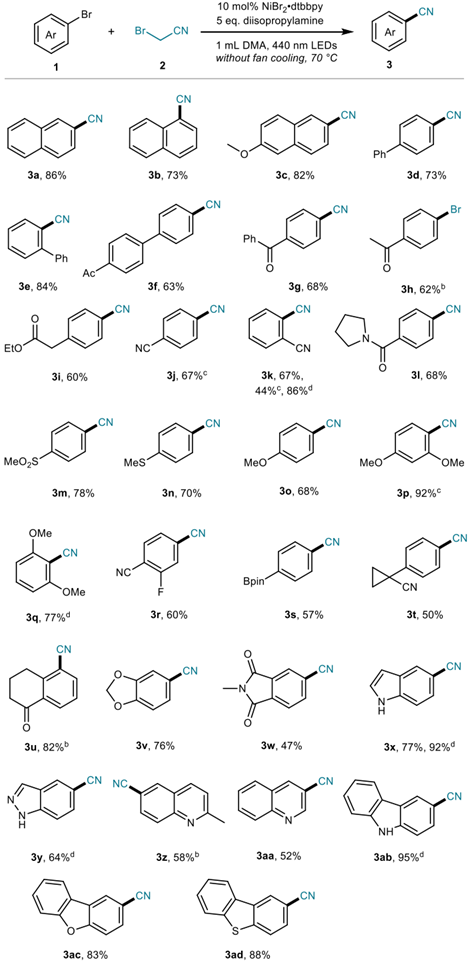
图2来源ACS Catal.
当以氰乙酸铯为氰基源,Ni(cod)2 为催化剂,4CzIPN 为光催化剂,440 nm蓝色LED为光源,能够实现氰乙酸铯的脱羧氰甲基化反应,并对底物普适性进行了考察(图3)。
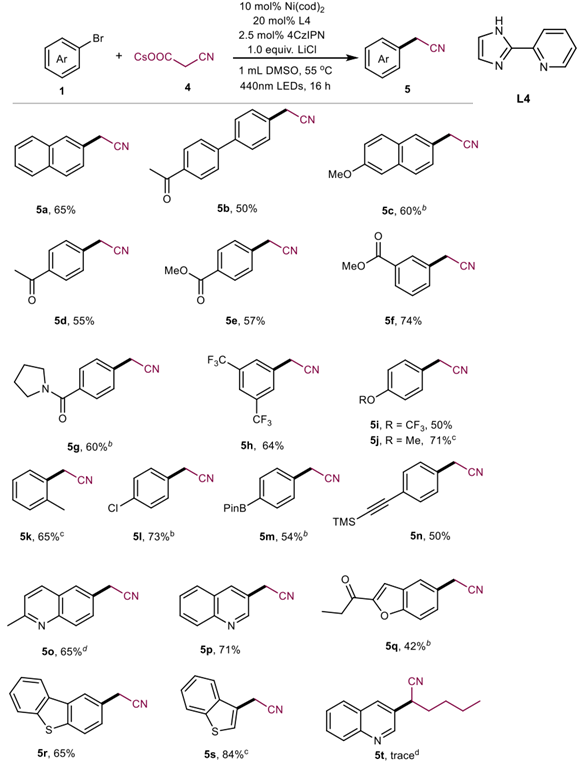
图3来源ACS Catal.
最后,作者对该反应提出了可能的机理。(1)溴乙腈的脱甲基氰化反应,Ni(II)催化剂经历了配体-金属电荷转移(LMCT)历程,生成了活性Ni(I)催化剂,并且iPr2NH 与溴乙腈作用生成iPr2N(CH2CN) 中间体D,其通过配体交换释放氰基(图4a)。(2)氰乙酸铯的脱羧氰甲基化反应,氰乙酸铯经历单电子氧化历程,生成氰甲基自由基,随后经历氧化加成/还原消除反应历程得到目标化合物(图4b)。
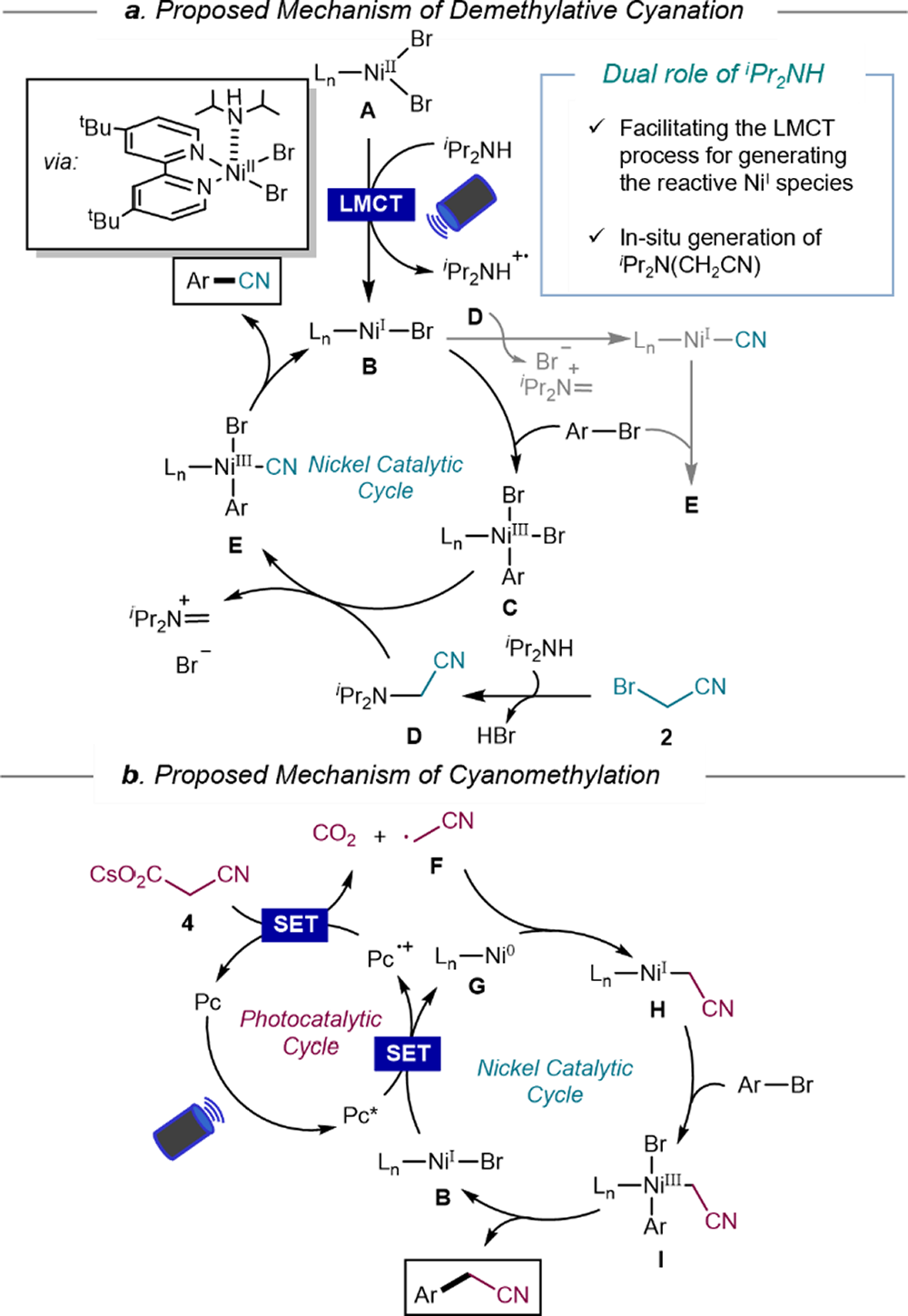
图4来源ACS Catal.
编者结语
阿卜杜拉国王科技大学Magnus Rueping团队利用溴乙腈和氰乙酸铯为氰基源,在光/镍协同催化体系下分别实现其与芳基溴的溴乙腈的脱甲基氰化反应,氰乙酸铯的脱羧氰甲基化反应合成芳基腈及苄腈化合物。
文献信息:
Photoinduced Nickel-Catalyzed Demethylative Cyanation and Decarboxylative Cyanomethylation of Aryl Halides
Shao-Chi Lee,* Chen Zhu,* Kun Huang, Jeremy A. Bau, Jiaqi Jia, Huifeng Yue,* and Magnus Rueping*
参考文献:
1. J. Am. Chem. Soc. 2005, 127, 15824-15832
2. Angew. Chem., Int. Ed. 2003, 42, 5051-5053
3. Angew. Chem., Int. Ed. 2011, 50, 4470-4474
4. Chem. Commun. 2020, 56, 4240-4243
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





