深职大程斌/汪太民课题组Org. Lett.:光催化[2+2+1]反应构建2,3-二氢苯并吡喃-4-酮并吡咯烷类化合物
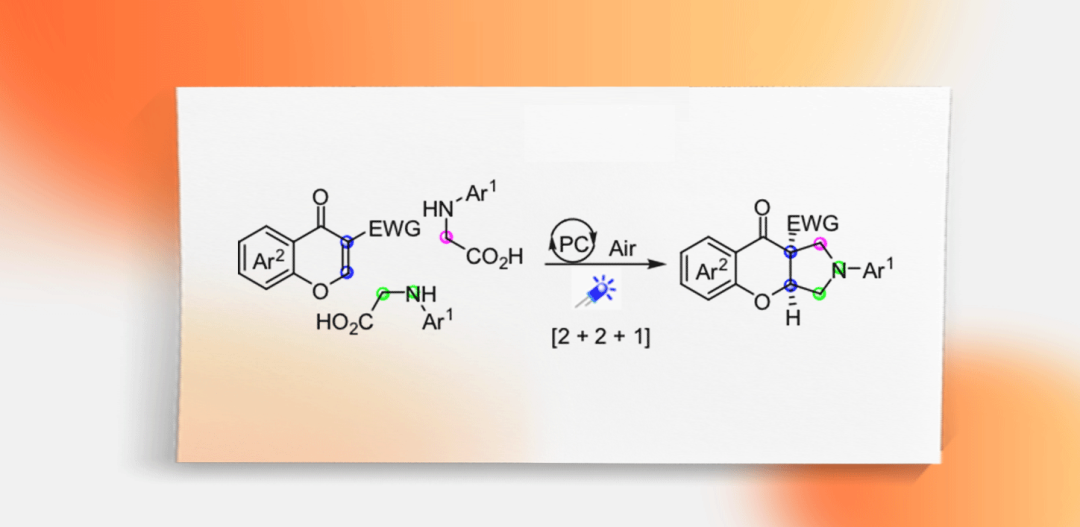
吡咯烷是一类最常见的氮杂环,普遍存在于数量众多的具有生物活性的生物碱和药物分子中。吡咯烷与色满等一些有用的药效基团结合,可产生许多具有药学价值的分子。例如,化合物1’对5-脂氧合酶有明显的抑制作用,螺环吡咯烷2’-6’对K562细胞有细胞毒性,而氟代色满并吡咯烷7’-8’可用于治疗勃起障碍(图1a)。激发态光催化剂引发的单电子转移(SET)或能量转移(EnT)过程,能够实现常规条件无法实现的化学转化。可见光催化的合成已经发展成为目前最流行的绿色、可持续的合成方法之一。文献中构建色酮并吡咯烷类化合物的方法主要是利用色酮与亚胺叶立德发生[3+2]环加成反应(图1b)。然而,这类方法通常使用活性较高的羰基化合物,如甲醛或者α-活化的酮,并且需要过渡金属催化剂、酸或路易斯碱催化。
尽管在许多光催化报道中色酮被广泛用作反应物,但它们仅仅被用作Giese加成受体来合成2-官能团化的色满-4-酮类化合物,而色酮的光催化环加成反应很少被披露。另一方面,N-芳基甘氨酸在光催化研究领域中受到越来越多的关注,常见其作为自由基前体或者亚甲基源,在合成氮杂环方面刚刚显露头角。但到目前为止,用这种策略实现合成的五元氮杂环仅限于咪唑啉和1,2,4-三唑啉,吡咯烷的合成尚未见报道(图1c)。
基于此,近日,深圳职业技术大学程斌/汪太民团队利用光催化策略,成功实现了色酮衍生物与N-芳基甘氨酸的[2+2+1]环化反应,合成一系列2,3-二氢苯并吡喃-4-酮并吡咯烷类化合物(DOI:10.1021/acs.orglett.3c02801)。
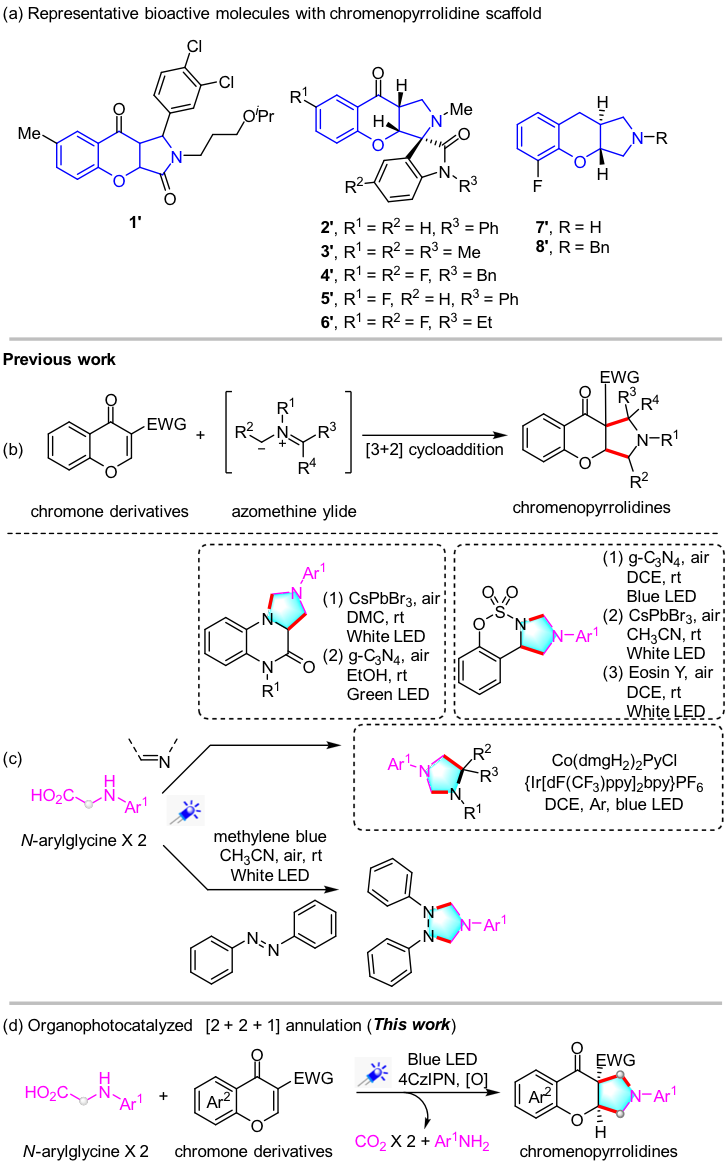
图1 研究背景(来源Org. Lett.)
利用3-氰基色酮和N-苯基甘氨酸作为模型底物,经过对反应细节的深入筛查,作者确定了空气作为氧化剂的最优反应条件。随后作者对该反应的底物普适性进行了研究(图2)。该反应色酮可以兼容多种常见的取代基,例如卤素、甲基、甲氧基,甚至羟基,各种底物都能以较好的收率得到目标产物。色酮底物中,3-位吸电子基也不局限于氰基,酯基和羧基(部分会发生脱羧)也可兼容。而在N-芳基甘氨酸底物中,苯环上带有吸电子基(如三氟甲基)则明显不利于反应。
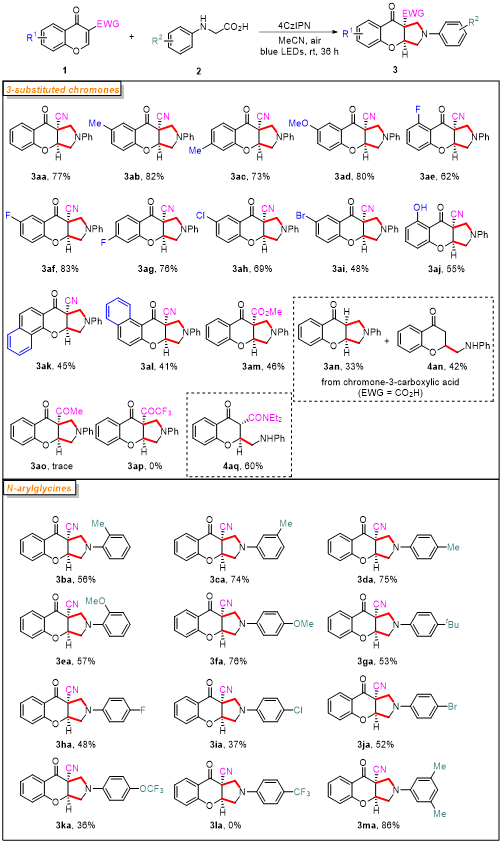
图2 底物适用范围研究(来源Org. Lett.)
此外,作者对反应还进行了类似底物进行了扩展研究。作者合成了一些与色酮类似物(5a-5d,图3),使其在标准条件下与N-苯基甘氨酸反应,然而总体结果并不令人满意。
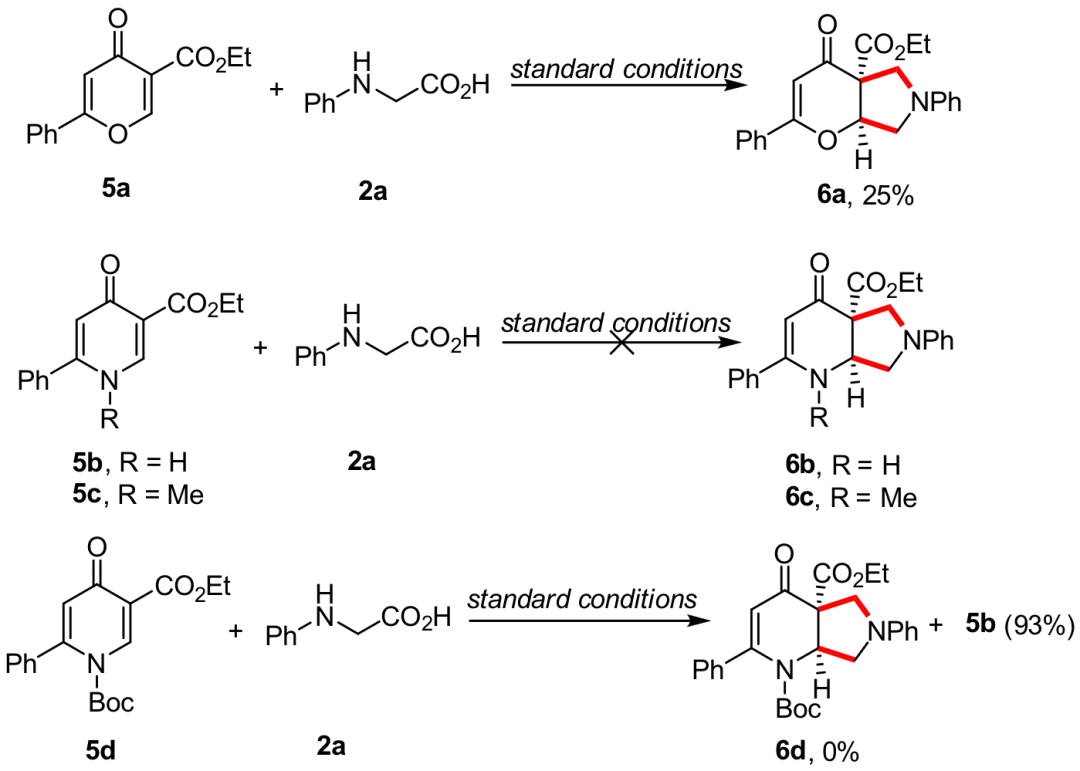
图3 拓展性研究(来源Org. Lett.)
最后,作者根据已有的文献报道和机理研究实验结果,对该反应过程提出了一个可能的机理。首先咔唑类光催化剂4CzIPN在可见光作用下被激发,随后被苯基甘氨酸2a还原淬灭得到自由基阳离子中间体A,经过脱质子/脱羧得到自由基中间体B,再与1a发生Giese加成反应得到中间体C,并进一步发生质子化得到中间体D。另一方面,还原态的光催化剂被空气中的氧气单电子氧化实现催化剂的重生,而产生的氢过氧自由基则夺取氨甲基自由基B的一个电子产生亚胺E和双氧水。亚胺E被苯胺D亲核加成反应并脱除一分子苯胺得到亚胺离子中间体G,最后引发分子内的Mannich反应得到最终产物(图4)。
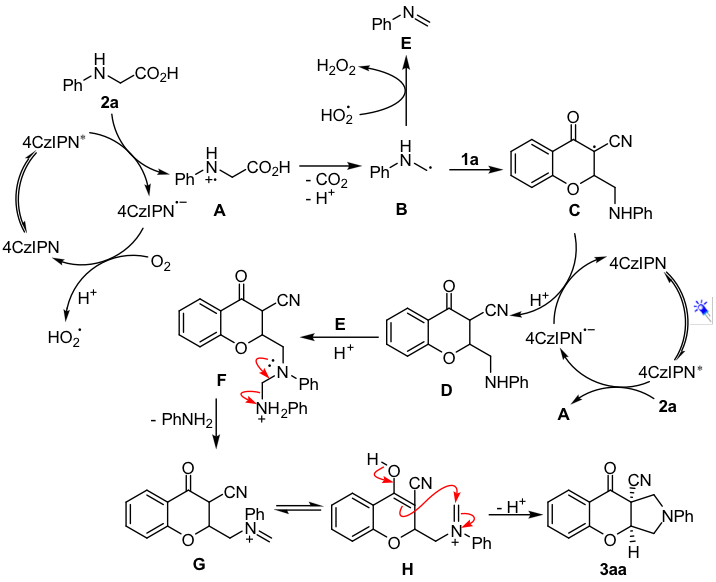
图4 反应机理(来源Org. Lett.)
总结:综上所述,深圳职业技术大学程斌/汪太民研究团队利用空气参与的光催化策略,发展了色酮和苯基甘氨酸的脱羧[2+2+1]环加成的新颖方法学,成功实现一系列具有潜在药用价值的2,3-二氢苯并吡喃-4-酮并吡咯烷类化合物的合成。值得一提的是,该工作首次利用N-芳基甘氨酸作为光化学合成子实现吡咯烷环构建。在这一转化过程中,N-芳基甘氨酸扮演了双重角色,即自由基前体和亚甲基提供者。该转化进一步展示了N-芳基甘氨酸作为自由基前体在合成杂环类化合物中的巨大应用潜力。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





