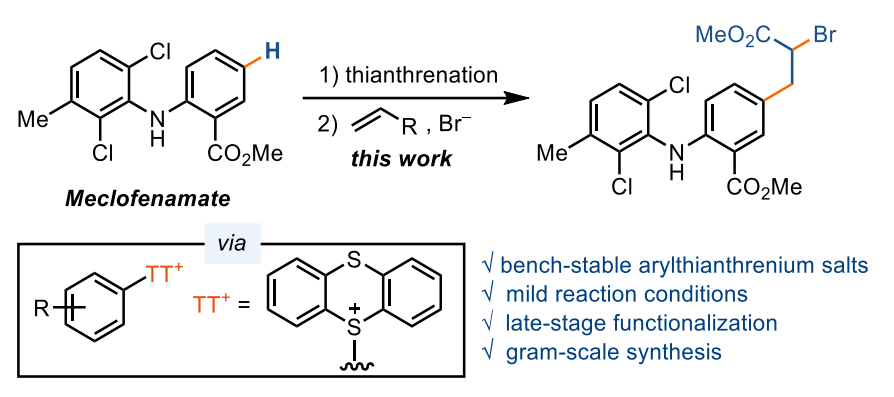
Angew:首例基于芳基噻蒽鎓盐的烯烃光催化Meerwein型溴芳基化反应
导读
近日,德国马普所的Tobias Ritter教授课题组报道了一种以稳定芳基噻蒽鎓盐为芳基化试剂的光催化烯烃Meerwein型溴芳基化反应。他们通过芳烃区域选择性C-H键官能团化获得芳基-噻蒽鎓盐,随后以PTH为光敏剂、TBAB为溴源,成功实现了烯烃的溴芳基化。该反应具有优异的官能团兼容性,反应条件温和并可应用于众多复杂分子的后期功能化。
正文
图片来源:Angew. Chem. Int. Ed.
自1939年Meerwein芳基化反应首次报道以来,烯烃的自由基芳基化被广泛应用于合成化学中,其用途涉及众多有价值的C-C键形成反应。然而,Meerwein 反应需要使用热稳定性较差甚至易爆的芳基重氮盐作为芳基化试剂。此外,众多副反应,如Sandmeyer反应以及生成偶氮化合物,也会导致传统的Meerwein芳基化反应具有较低的收率,且目前没有相关复杂小分子后期官能团化的报道。
截至目前,化学家们已经发展了众多关于诱导产生芳基自由基参与转化的策略,其可用作传统过渡金属催化芳基卤代物偶联反应的补充。例如Gaunt 教授课题组发展的基于Cu-催化二芳基碘鎓盐的模块化Meerwein型叠氮基芳基化和溴芳基化(Nature. 2021, 598, 597)。该三组分反应中的芳基自由基源、烯烃和捕获剂都可进行衍生化,得到结构多样的偶联产物。传统的Cu-催化的Meerwein卤代芳基化反应通常会因众多副反应而复杂化。例如,铜也会引发 Sandmeyer反应,卤原子从 CuX2转移到芳基自由基上的速率通常比芳基自由基进攻烯烃的速率更快,因此会有较多卤代芳烃副产物生成。而稳定的芳基卤化物由于具有较高的还原电位,难以作为芳基自由基源,这限制了其在Meerwein 芳基化中的应用。仅有少数几例由芳基卤代物出发的自由基芳基化反应被报道,例如陈庆安教授发展的光催化卤代吡啶和未活化烯烃的交叉偶联反应(Nat. Commun. 2021, 12, 6538)。
Tobias Ritter教授课题组近年来开发了一系列基于噻蒽鎓盐的活性试剂以及新反应(J. Am. Chem. Soc. 2021, 143, 7623; Nat. Chem. 2022, 14, 898; Angew. Chem. Int. Ed. 2021, 24, 13609.)。最近,他们报道了一种可用于复杂结构芳烃区域选择性噻蒽化的方法,以提供稳定的芳基噻蒽鎓盐,并将其作为芳基自由基前体实现后期C-CF3、C-N、C-O以及C-F键的形成(Nature. 2019, 567, 223)。由于芳基噻蒽盐相比于芳基重氮盐和二芳基碘鎓盐更易获得且具有良好的稳定性,较低的还原电位使其成为理想的芳基自由基前体,因此作者考察了其在Meerwein芳基化反应中的应用潜力。首先作者尝试结合光氧化还原和铜催化,以噻蒽鎓盐为自由基前体对丙烯酸甲酯进行溴芳基化反应。然而在该条件下,Sandmeyer副反应占据主导,主要生成了芳基溴化物。随后作者发现,在不添加铜催化剂条件下溴芳基化能以较低的收率完成。通过对光敏剂、溶剂和反应温度等参数进行优化,最终确定了以PTH为光敏剂、乙腈为溶剂、-20 ℃低温下使用白光LED照射为标准反应条件。在该条件下,副产物芳基溴化物的生成几乎被完全抑制,且噻蒽能以93%的分离收率完成回收。
作者基于相关文献报道以及条件筛选实验和Stern-Volmer荧光淬灭实验,提出了可能的反应机理。首先芳基噻蒽盐Ar- TT+被激发态的光敏剂PTH*(-1.92 V vs SCE in DMA)单电子还原生成噻蒽和芳基自由基。同时未观察到芳基噻蒽盐和PTH之间形成的电子供体-受体(EDA)复合物。芳基自由基随后与烯烃发生自由基偶联生成相应烷基自由基,与此同时溴离子会被光敏剂氧化态PTH•+氧化再被烷基自由基捕获得到最终溴芳基化产物。
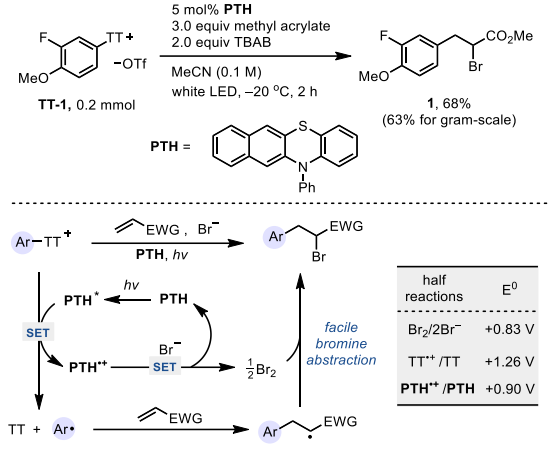
图片来源:Angew. Chem. Int. Ed.
随后,作者在标准反应条件下开展了底物普适性研究。结果表明该反应具有优异的区域选择性,包括芳烃的C-H键噻蒽化以及对烯烃的溴芳基化均没有观察到其它结构异构体的生成。缺电子(17)、电中性(12, 23)和富电子(2)芳烃都能以良好的产率得到溴芳基化产物。另外,作者还实现了多取代芳基-噻蒽鎓盐的合成并成功应用于此反应(14, 18, 26),而传统的Meerwein溴芳基化反应中使用的大多数芳基重氮盐仅限于单卤代或多卤代。该反应对多种官能团都具有良好的兼容性,包括环丙基、烷基氯、芳基卤化物、芳基拟卤化物、醚、醛、酮、酯、酰胺、磺酰胺、腈和硝基。同时还兼容众多杂芳烃,如吡啶(7)、苯并呋喃(21)、吲哚(26)。对于苄氧基(22, 25)和邻位烷氧基取代的芳烃(16, 18, 26),产率出现明显下降并生成大量加氢去官能团化副产物。另外,众多其它Michael受体也能成功完成该溴芳基化反应,如丙烯酸苄酯(27)、丙烯酸叔丁酯(28)、丙烯腈(29)、甲基乙烯基酮(30)、乙烯基砜(31)、磷酸乙烯酯(32)、α-乙烯基内酯(33)、氟代丙烯酸酯 (34)、甲基丙烯醛(35)和丙烯酰胺(36, 37)。单取代苯乙烯(38, 39)也可顺利完成此转化,且未观察到芳基-烯烃偶联副产物生成。一般情况下,由于未活化烯烃发生的自由基加成步骤缓慢,会导致芳基自由基发生其它副反应。而在此反应中,作者成功实现了未活化的 4-溴-1-丁烯(40)的溴芳基化反应。
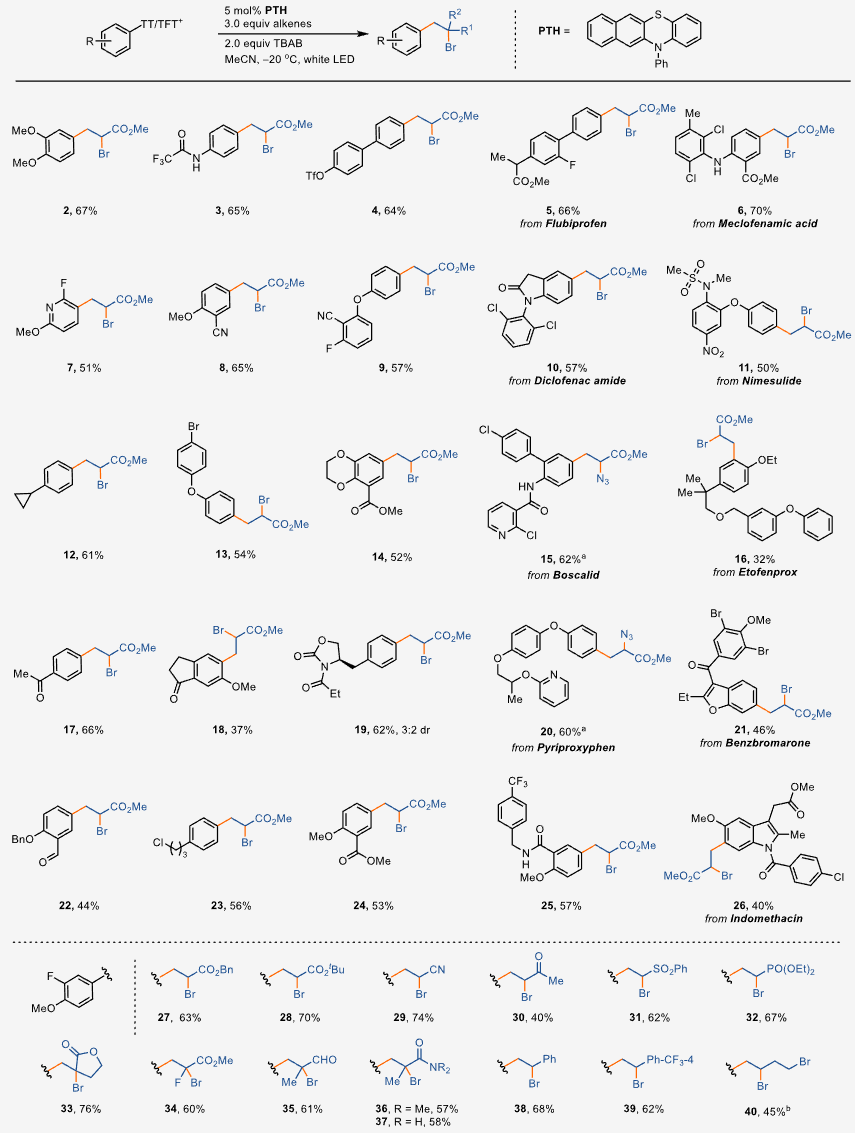
图片来源:Angew. Chem. Int. Ed.
Meerwein溴芳基化除了形成新的 C(sp2)-C(sp3)键外,还引入了一个活性碳卤键,可用于后续的进一步转化。为了证明该反应的潜在合成应用,作者使用了多种亲核试剂进行后续转化,得到了一系列复杂分子以及药物骨架,例如苯丙氨酸(15、20、41)和降血糖药物噻唑烷二酮(49)。
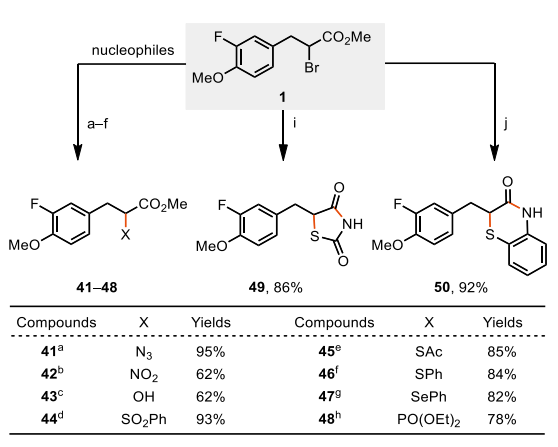
图片来源:Angew. Chem. Int. Ed.
总结
Tobias Ritter课题组以芳基噻蒽鎓盐为芳基自由基前体,在光催化条件下实现了烯烃的Meerwein型溴芳基化。该反应结合芳烃C-H键的区域选择性噻蒽化,实现了众多复杂有机小分子的溴芳基化,其中包括一些生物活性分子和药物骨架,具有良好的底物普适性且反应条件温和。
文献详情:
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




