Angew:深度电还原下Ar-CF3的可控脱氟氢化合成多种含氟化合物
近日,英国布里斯托大学的Alastair Lennox教授课题组报道了一种Ar-CF3化合物电化学下可控的直接加氢脱氟反应。他们利用电化学反应的电极电势可调性以及镍阴极的选择性,实现了Ar-CF3的深度电还原并以高选择性获得ArCF2H产物。此外,该策略还可扩展至一步双脱氟反应用于单氟甲基化ArCH2F产物的合成。这种含-CF3底物的后期修饰反应用于构建-CF2H或-CH2F的策略,将有助于实现复杂含氟先导化合物的快速多样化。
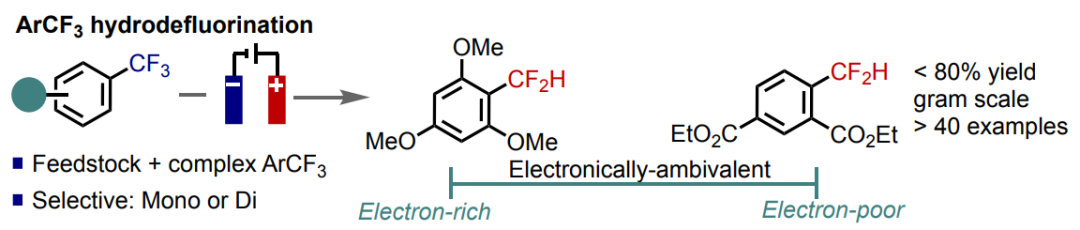
图1. Ar-CF3电化学脱氟氢化(图片来源:Angew. Chem. Int. Ed.)
二氟甲基具有独特的物理化学性质,是药物和农用化学品设计中最受关注的官能团之一。例如,CF2H可作为亲脂性氢键供体被引入药物或生物活性分子中,用于改善脂溶性及代谢稳定性等(图2A)。直接二氟甲基化反应是向分子中引入CF2H的有效手段,然而这种类型的反应一般受限于狭窄的底物适用范围以及昂贵的二氟甲基化试剂。由传统的惰性CF3出发通过脱氟加氢获得含CF2H化合物具有一定的合成和战略优势,因此近年来受到了人们的广泛关注(图2B)。此前,Perichon、Savéant以及Bordeau等人先后开发了一种通过单电子还原来实现CF3脱氟官能团化的策略,该反应通过SET诱导C-F键断裂完成脱氟。然而,随着CF3的逐步脱氟,C-F键键能依次降低,这将导致难以控制脱氟反应停留在选择性生成CF2H产物这一步。随后,Prakash课题组报道了在酸性条件下使用过量的镁作为还原剂对易还原的双(CF3)芳烃进行加氢脱氟。这种脱氟/质子化(ET/PT,图2C)策略中的还原剂必须优先还原ArCF3并避免直接质子还原,因此在很大程度上限制了ArCF3的底物范围。Jui、Gouverneur和尚睿等课题组先后实现了官能团兼容性更好的脱氟反应,他们使用光催化策略,由激发态光敏剂引发SET,然后进行氢原子转移(HAT, 图2C)。此类型的反应具有良好的加氢脱氟效率和选择性,但由于还原电势窗口由光催化剂/氢原子供体来决定,对于每个特定的ArCF3底物需要使用适当的光催化剂/氢原子供体体系。因此,如何实现高底物适用范围的ArCF3催化脱氟氢化反应依然是一个亟待解决的难题。
电化学反应具有安全可调节的电势范围,可以轻松获得传统化学还原剂和激发态光催化剂范围之外的还原电势,因此是实现深度还原(<-2.0 V vs Fc/Fc+)的理想工具。随着逐步脱氟,每个中间体的还原电位变得更负(图2D),因此仅通过控制施加还原电位,即可区分中间体,更容易避免过度脱氟。
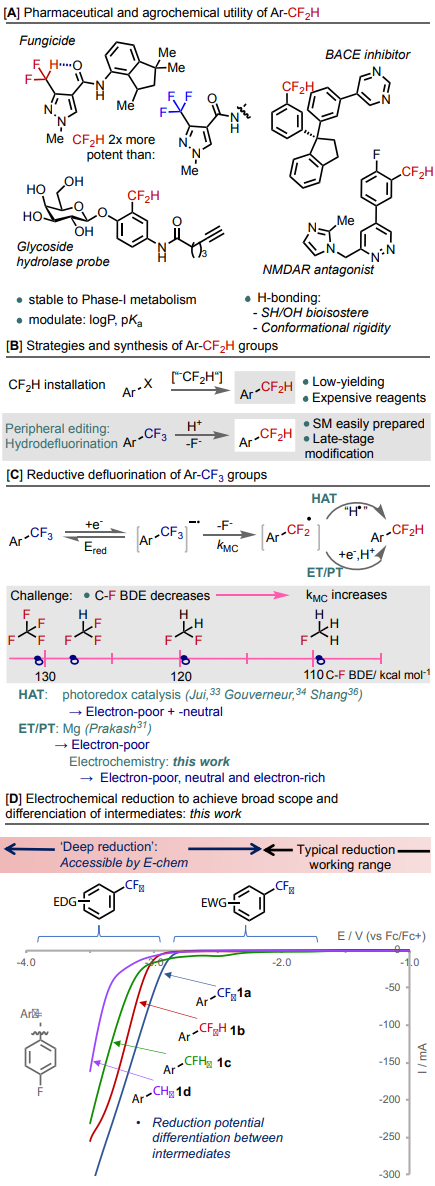
图2. 研究背景与反应设计(图片来源:Angew. Chem. Int. Ed.)
开发电还原反应的首要挑战是适应所需的深度还原电位,同时避免过度还原以及竞争性质子还原。作者首先以电中性Ar-CF3底物1a (Ered(onset) = -2.8 V vs Fc/Fc+)为模板底物。采用具有还原稳定性电解质体系的隔膜式电解池 (MeCN,Ewindow = -3.4 - +2.7 V vs. Fc/Fc+, Et4NPF6)。经过详细的反应条件优化(图3),单加氢脱氟产物1b与双加氢脱氟产物1c的选择性达到25:1,并获得了76%产率的ArCF2H产物1b。向阴极反应槽中加入氟离子捕获剂TMSCl可提高产率和选择性。阳极槽中加入的Bu4NBr可用作有机还原剂,代替了此前类似反应中使用的牺牲金属阳极,同时由于其氧化产物为Br3-阴离子,不会迁移至阴极槽导致法拉第效率下降。对照实验表明,Bu4NCl也适用于此反应,但选择性较低。Ni作为阴极比Pt或石墨具有更高的产率和反应选择性。溶剂和支持电解质的筛选结果表明MeCN和Et4NPF6为该体系下的最优选择。
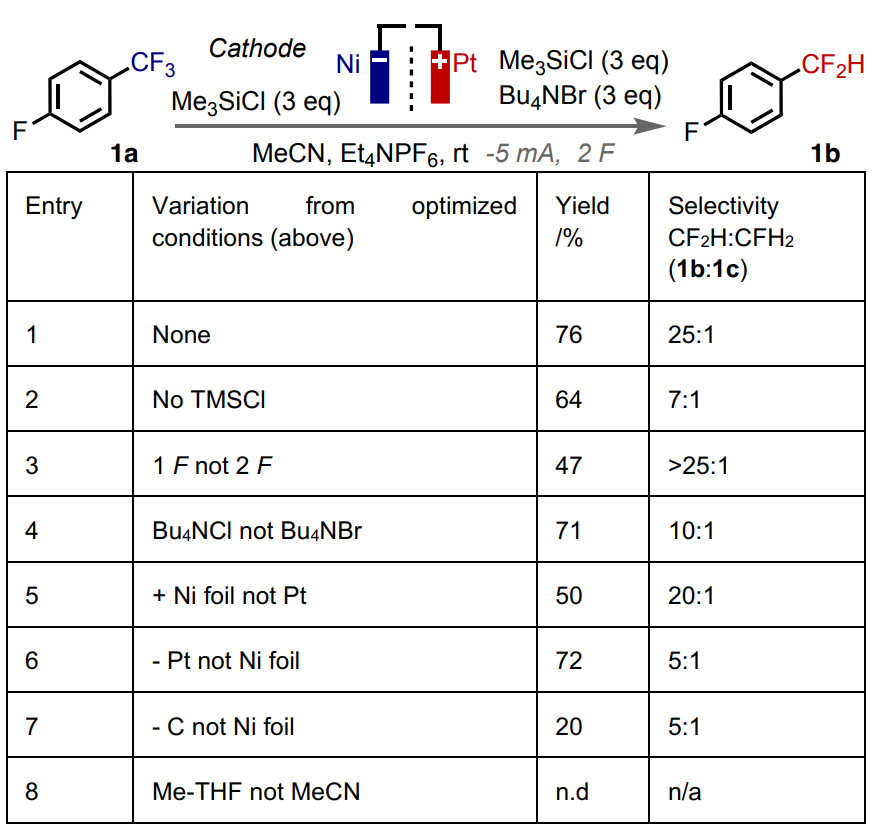
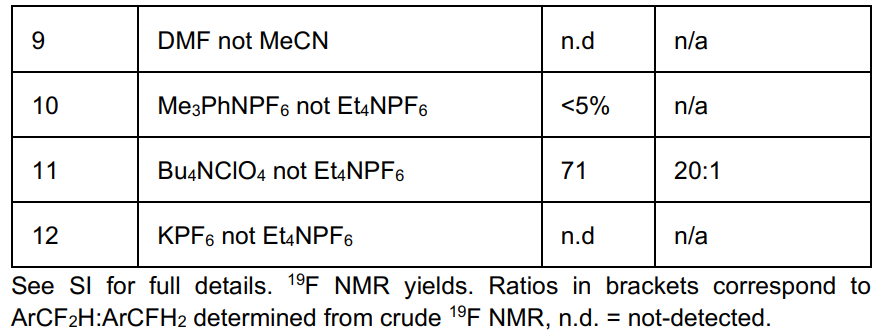
图3. 反应条件筛选(图片来源:Angew. Chem. Int. Ed.)
在优化后的标准反应条件下,作者考察了该体系对一系列不同电性ArCF3底物的适应性(图4A),同时将反应产率和选择性与文献中的报道值进行对比。首先,电中性底物1a-4a在标准反应条件下能良好地兼容,并以良好到优异的收率得到目标ArCF2产物1b-4b,与文献报道的产率值相当。对于缺电子底物5a,反应可以顺利完成,并以58%的产率得到5b,同时未观察到酯的还原。值得注意的是,该电化学条件还可以兼容还原电势更高的富电子底物6a-8a,包括2,4,6-三甲氧基-三氟甲苯8a,而目前文献中报道的方法均不能实现此类底物的还原脱氟。循环伏安实验表明,6a和8a的还原电势分别比1a高160 mV和500 mV
在此基础上,作者继续探索了更为复杂的商品化和功能化ArCF3底物的适用范围。富电子底物,包括苯胺衍生物(10-12a)、醚(13-14a)以及烷基衍生物(15-21a)均能以良好的收率和选择性得到目标产物。对于更多含缺电子芳环的底物(22-25a),也均能以中等至良好的产率完成该转化,包括高度缺电子的双酯化合物25a。作者还考察了更复杂的药物分子(26-33a)的反应性,在标准反应条件下,这些底物均可被兼容,并以中等的产率得到二氟甲基产物,证明了该方法具有优异的官能团兼容性以及应用潜力。最后,作者通过Hammett分析揭示了该反应的效率与底物上取代基电性的相关性,证明了这种深度电还原策略是目前底物适用范围最广的脱氟加氢反应(图4B)。
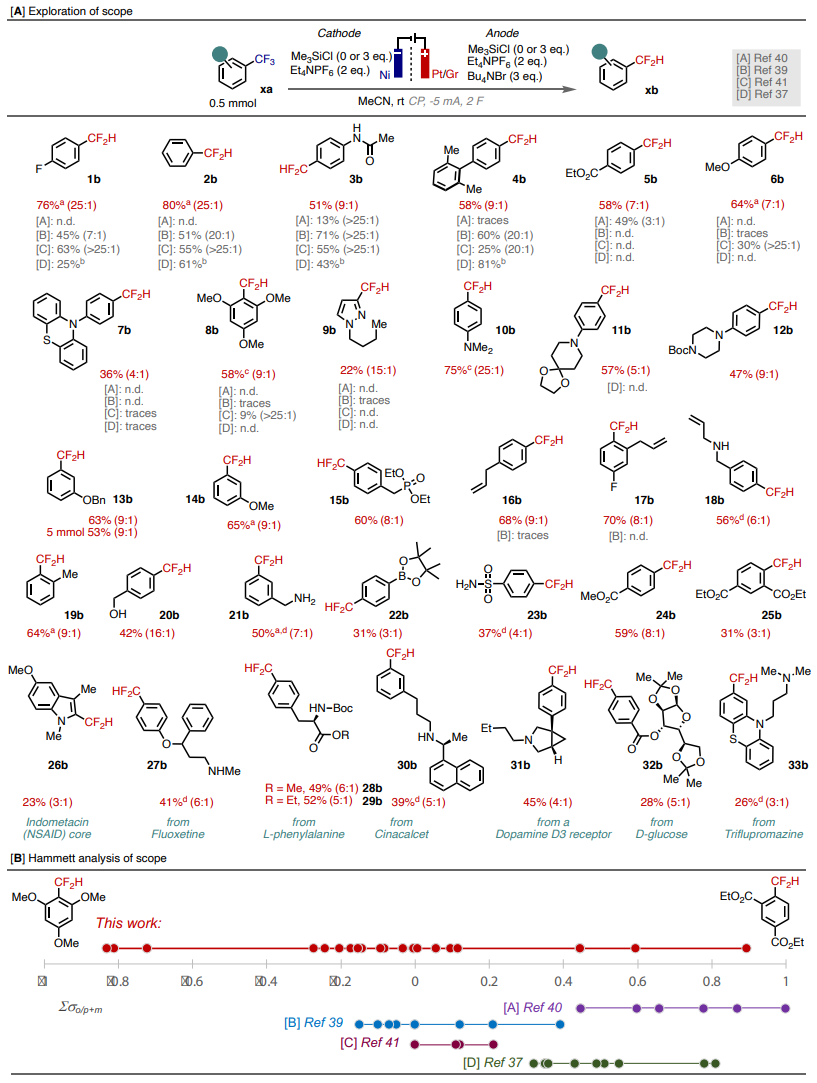
图4. 反应底物拓展与Hammett分析(图片来源:Angew. Chem. Int. Ed.)
为了深入了解该脱氟加氢反应的机理,作者进行了一系列控制实验(图5A)。首先,作者将分子外或分子内烯烃片段引入反应体系,均未观察到ArCF2·加成到双键上的的预期产物。这表明原位单电子还原脱氟得到的ArCF2·会快速发生二次还原(即ECEC机制)得到ArCF2–,这一点不同于光催化反应中的HAT过程。由于反应溶液为无水体系,作者期望探究该转化中的质子来源。通过在无水D3-MeCN中进行该反应,1a可顺利转化为D1-1b。尽管作者未直接测定ArCF2H和MeCN的pKa,但该结果也证明了ArCF2-的碱性足以使MeCN发生去质子化。
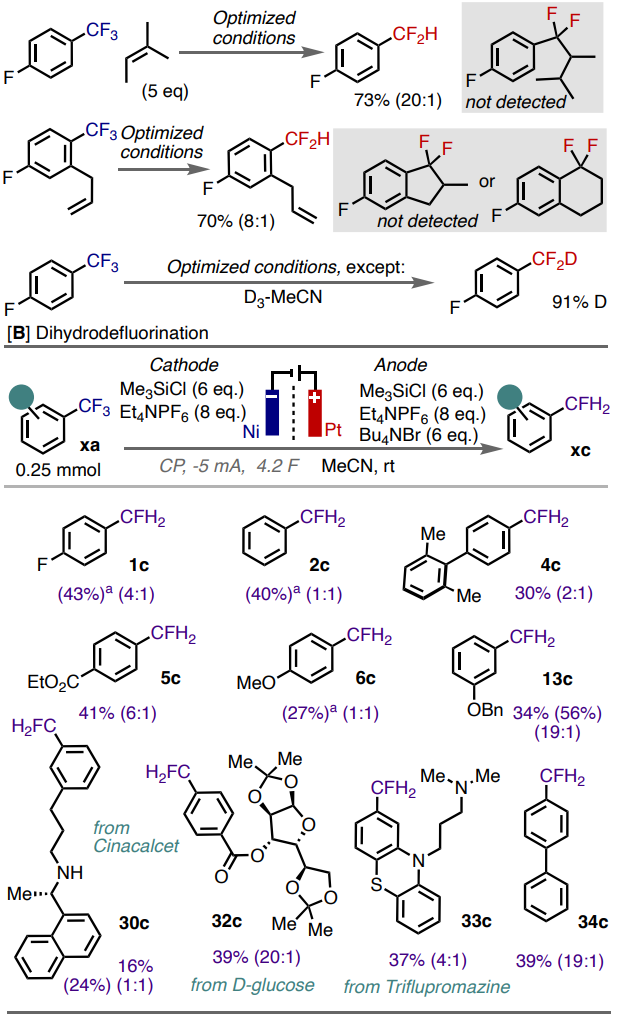
图5. 机理实验与双脱氟加氢反应拓展(图片来源:Angew. Chem. Int. Ed.)
最后,作者在上述单脱氟加氢的研究基础上,继续探究了ArCF3的直接双脱氟加氢反应(图5B)。实验结果表明通过降低底物浓度、增加电流密度以及提高电解电量,1a能以良好的产率和选择性获得双脱氟加氢产物1c。进一步的底物范围考察表明,该反应对于大多数底物均能以中等至良好的收率获得ArCFH2产物,包括电中性(2a, 4a, 34a)、富电子(6a, 13a)和缺电子底物(1a, 5a)。衍生自西那卡塞(30a)、D-葡萄糖(32a)和三氟丙嗪(33a)的复杂底物均可被该体系兼容,并以中等收率得到单氟甲基化产物。
总结
Alastair Lennox课题组开发了一种ArCF3底物的可控加氢脱氟反应。通过在深度还原电位下在镍阴极上进行电化学还原,实现了良好的反应性和选择性。该反应可用于制备广泛的ArCF2H化合物,包括药物和生物活性小分子。此外,该策略还被扩展到双脱氟加氢反应,用于合成ArCFH2化合物。这种由惰性CF3出发快速构建其它含氟甲基的策略在氟化学以及药物化学等领
文献详情:





