通过可见光介导的双催化技术合成α-氯烷基硼酸酯
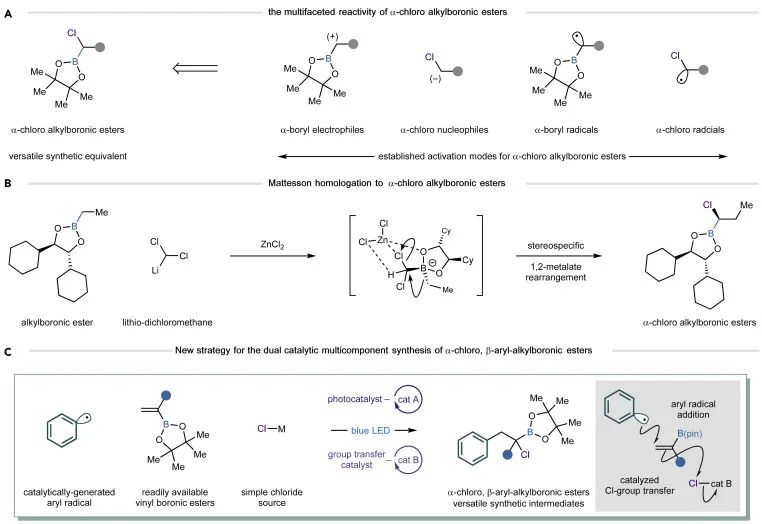
α-氯烷基硼(α-CAB)酯是一类稳定的双功能分子,其中碳-氯和碳-硼键的内在差异可通过碳亲电性、碳亲核性和碳中心自由基中间体解锁不同的反应活性(图1A)。Matteson和同事的开创性工作提供了制备α-CAB酯的最直接的方法(图1B),但完全取代的α-CAB酯不能通过这种方法获得,因为更多取代的二氯烷的相应的锂化化学反应是困难的,而且硼向碳的迁移受到额外的烷基取代基的阻碍。
本文报道了一种可见光介导的双催化系统,二芳基碘鎓盐、取代的乙烯基硼酯和氯化钾的多组分反应在可见光的引导下通过光催化剂引起芳基自由基的形成,并导致芳基自由基加成乙烯基硼酯。基团转移催化剂作用氯转移到新形成的α-硼基自由基上,形成α-CAB酯(图1C)。
作者以图2A的条件进行反应,产率为71%,考虑到两个铜催化的氧化还原平衡和关闭受到ISET过程的影响,所以考虑使用其他的光催化剂和基团转移催化剂来进行催化:并进行了一系列的条件筛选:
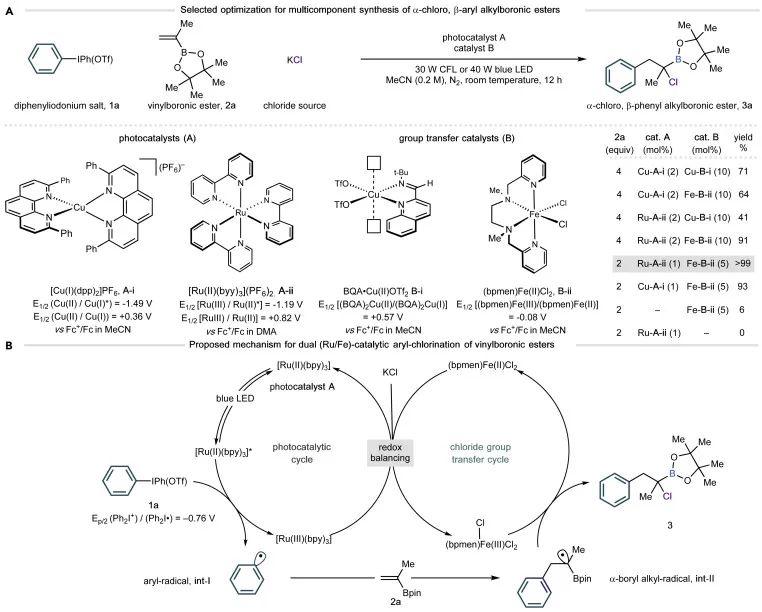
铁(II)催化剂能够影响碳-氯键的形成,作为基于原子转移的反应的一部分,所以尝试使用铁(II)催化剂作为基团转移催化剂;并且使用钌(II)催化剂作为光催化剂,这二者都可以大大提高产率。
提出了可能的机理,如图2B。
测试了取代的二芳基碘鎓盐来研究芳基部分的反应范围如图:
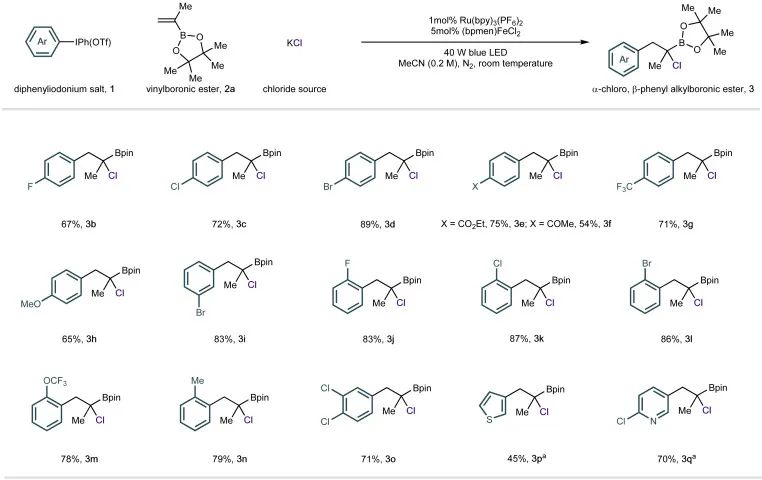
测试了乙烯基-硼酸酯成分的范围,如图:
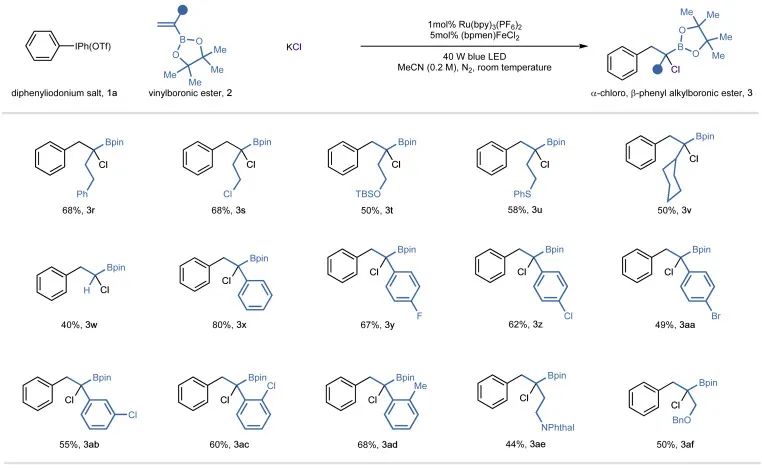
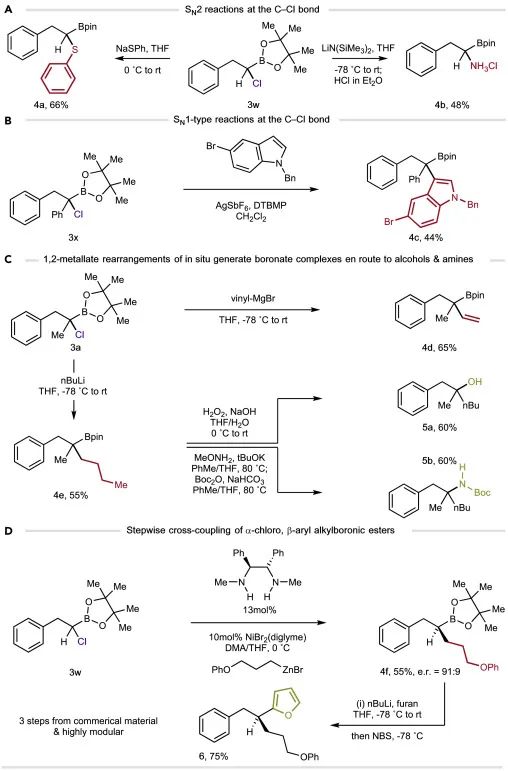
在3w中的亲电碳-氯键处用硫酸盐亲核体进行简单的SN2置换,形成α-硫醚烷基硼酸酯4a,用LiHMDS作为亲核胺的来源进行胺化反应,形成相应的α-氨基烷基硼酸酯4b(图5A)
在AgSbF6的存在下用吲哚衍生物处理3w,这有利于吲哚基团的阳离子C3-烷基化,形成高功能化的α-BPin(4c)(图5B)
此外,α-CAB酯3a与丁基锂及后续转化、以及格式试剂的转化效果也较好;在4e的情况下,使用既定的氧化方法将复杂的烷基-Bpin酯推进到相应的叔醇(5a)和α-叔胺(5b)(图5C);3u可以在镍催化下进行立体反转的Negishi偶联。产物在丁基锂、NBS的作用下,呋喃会取代BPin,据报道,该过程是完全立体的(图5D)。这个交叉耦合序列表明了α-CAB酯中亲电的碳-氯键和亲核的碳-宾键之间的正交性,可以依次利用,以形成复杂的产品。
总结:作者通过可见光介导的双催化系统合成了α-CAB酯,它可以利用c-Cl键和C-B键的差异来转化为不同的复杂分子。
doi:10.1016/j.chempr.2022.10.010
iSET过程:内球电子转移(inner-sphere electron-transfer, iSET)是氧化还原化学反应,通过反应的氧化剂和还原剂反应物之间的共价键发生。在这里,配体在反应过程中桥接氧化剂和还原剂反应物,即叠氮阴离子连接光催化生成的 [Cu(II)(dpp)2]和还原基团复合物BQA⋅Cu(I)N3,然而,大配体会抑制该反应。这是因为这些大配体可以阻止反应形成关键的桥接中间体。因此,这种类型的电子转移机制在生物系统中很少见。通常,这种机制可用于描述过渡金属配合物的反应。





