【JACS】Motomu Kanai组:光催化自由基Arbuzov反应实现酪氨酸膦酸化促进肽/蛋白质选择性修饰
最近,日本东京大学Motomu Kanai课题组,报道了一种光催化自由基Arbuzov反应,可以实现酪氨酸的温和膦酸化。该反应条件温和,具有优秀化学选择性,可以在双肽、三肽和寡肽中选择性实现酪氨酸膦酸化。相关研究成果发表在近期的《美国化学会志》上(J. Am. Chem. Soc.)。
已报道SPM方法,局限于赖氨酸和半胱氨酸这些具有独特反应性氨基酸的官能团化。最近,其它传统上较低活性氨基酸(组氨酸、色氨酸等)的官能团化,吸引了更多注意力。酪氨酸(Tyrosine)官能团化是其中一个研究领域,已报道大量相关方法,包括Barbas烯化和利用酪氨酸相对低氧化电势(Eox =0.93 V vs NHE (pH7))而发展出的自由基偶联化学。这些方法可以引入非天然基团,也能通过引入合适手柄实现化学选择性弹头和荧光标记物的构建,但却不能实现膦酸化、磺酸化和糖苷化这些蛋白质翻译后修饰(PTMs)(Scheme 1B)。酪氨酸的膦酸化修饰,在基础细胞信号传导和控制机制中普遍存在,这导致异常酪氨酸膦酸化与癌症、神经退行性疾病和感染相关。因此,酪氨酸的膦酸化具有重要研究价值。
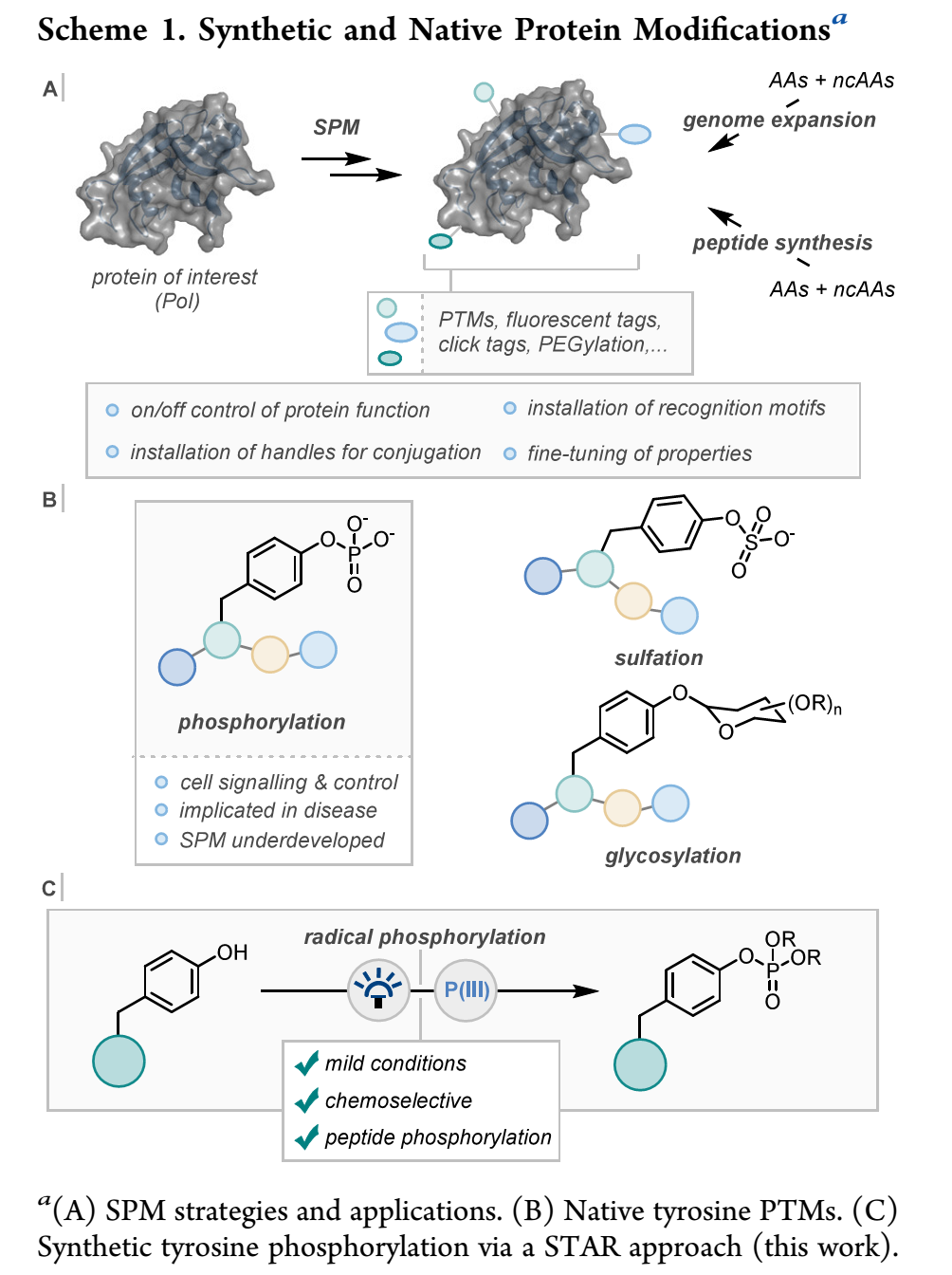
(Scheme 1,图片来源:J. Am. Chem. Soc.)
Motomu Kanai课题组近期报道过一种极性反转策略,可以实现酪氨酸的选择性膦酸化,但此方法局限于存在C-末端酪氨酸残基的肽(图1, Org. Lett. 2024, 26, 8827−8831)。为了解决这一不足,该课题组进一步开发出一种光催化自由基Arbuzov反应,可以实现酪氨酸的选择性膦酸化(Scheme 1C)。其可行性反应机理如Scheme 2所示:光催化剂PC在光激发下生成激发态光催化剂PC*,PC*可以和酪氨酸发生单电子氧化生成酚氧自由基4和PC·-;4和亚膦酸酯2发生加成反应得到膦自由基5,5发生β-裂解即可生成膦酸酯产物3和碳自由基6;6和PC·-发生单电子还原,生成碳负离子7并再生PC,完成整个循环。此反应极具挑战性,机理中所得碳自由基6易于和亚膦酸酯2发生副反应,生成C-膦酸酯化副产物8。作者认为可以通过调整亚膦酸酯2上基团,使所生成碳自由基6具有大位阻取代基,并加快6至7的单电子还原,从而降低竞争反应。
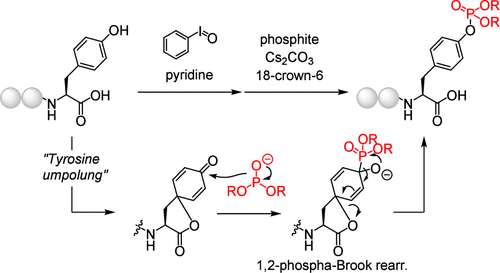
(图 1,图片来源:J. Am. Chem. Soc.)
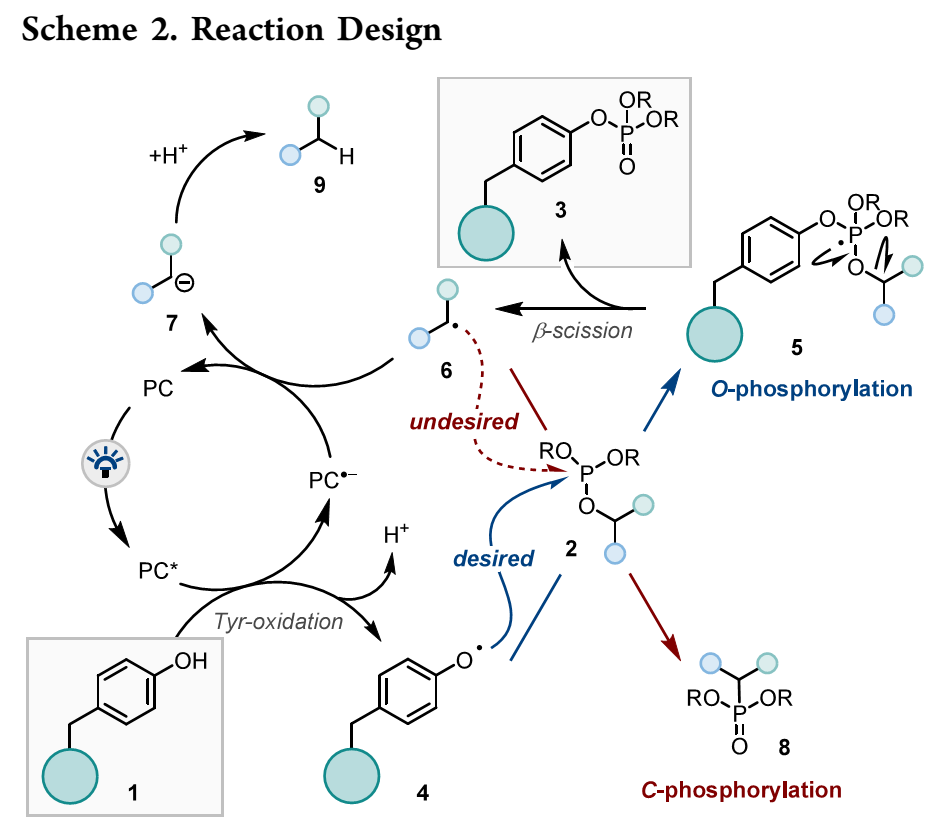
(Scheme 2,图片来源:J. Am. Chem. Soc.)
基于Scheme 2反应设计,作者选用4-CzIPN作为有机光催化剂,酪氨酸乙酯1a为模板底物,开展反应条件筛选研究。如Table 1所示,通过对光催化剂、亚膦酸酯、碱添加剂、溶剂等进行细致优化,得出如entry 10所示最优反应条件:2.5 mol% 4-CzIPN作光催化剂、5当量亚膦酸酯P6、咪唑作碱,叔丁基甲基醚(TBME)作溶剂,蓝色LED照射,反应能以90%产率得到产物3a。其中:1)亚膦酸酯苯环上基团对反应影响较大,供电子基团会降低反应性(P2、P5),吸电子基团因能降低自由基6还原电势而提高反应性(P3、P4、P6、P7);2)咪唑添加剂能通过质子耦合电子转移(PCET)加快酪氨酸氧化,从而提高反应性;3)在咪唑存在下,除TBME外,其它大极性溶剂例如乙醇、DMF、DMSO、DMF-水作溶剂,反应也能高效发生,这对大极性肽底物很适用;4)缺乏光照,反应不发生。
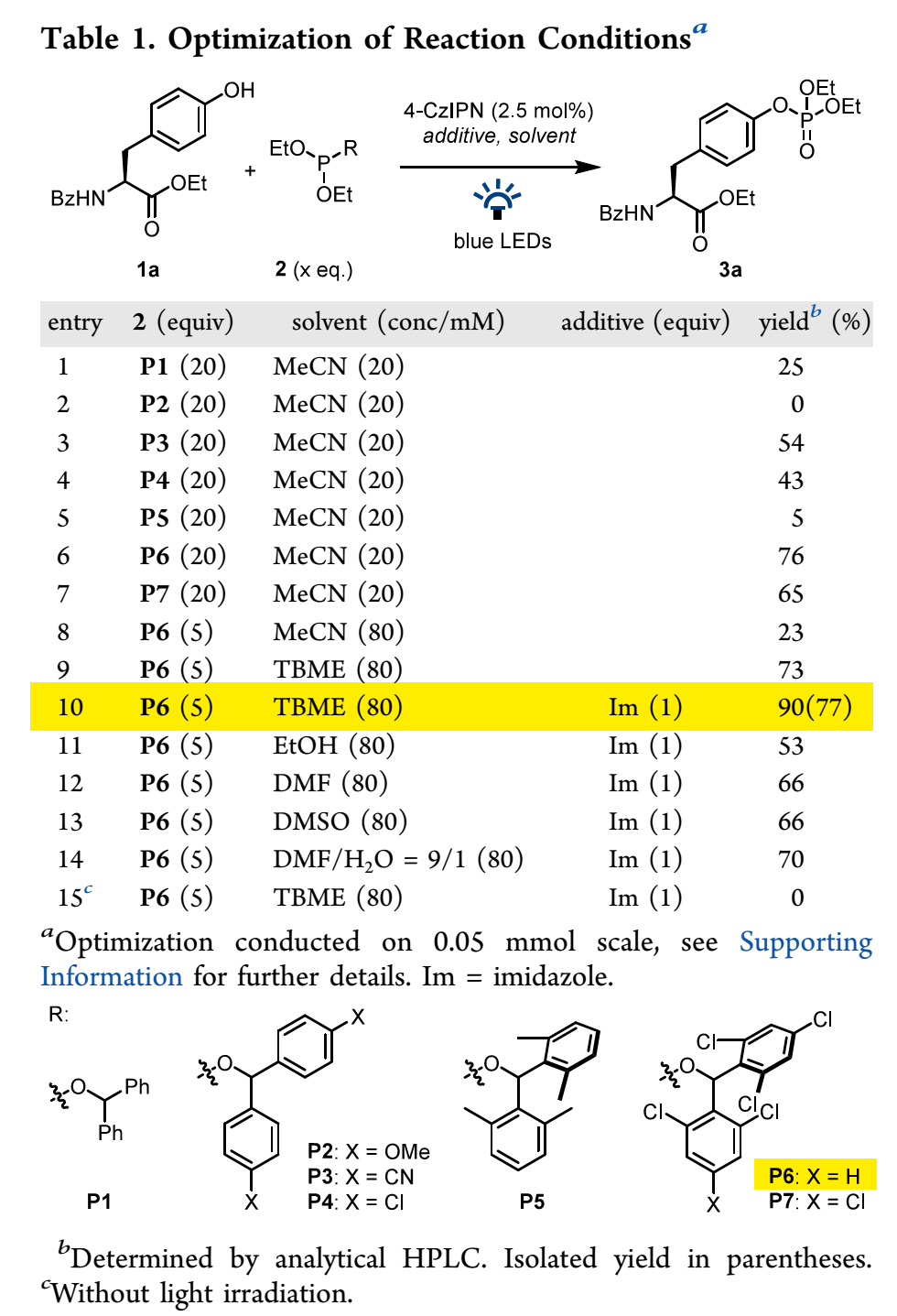
(Table 1,图片来源:J. Am. Chem. Soc.)
最后,作者开展底物拓展研究。如Scheme 3所示,1)含脂肪链二肽(3b-3d)、含易氧化氨基酸链(组氨酸、蛋氨酸、色氨酸)二肽(3e-3g)、含易发生膦酸化氨基酸链(丝氨酸、苏氨酸、赖氨酸)二肽(3h-3j),都能在最优反应条件下以可观产率和高选择性得到对应产物;2)含更大极性氨基酸链(天冬酰胺、谷氨酸)二肽(3k、3l),由于在TBME中溶解性差,需使用DMF作溶剂才能以中等产率得到对应产物;3)三肽(3m、3n)、四肽(3o、3p)、五肽(3q)、六肽(3r)、八肽(3s)也能在微调后的反应条件下发生反应,以中等产率得到对应产物。产物中的膦酸乙酯片段可以在过量TMSBr作用下水解成膦酸(SI中Scheme S1),膦酸二苄酯则可以通过钯碳氢气还原转化成膦酸(SI中Scheme S2)。
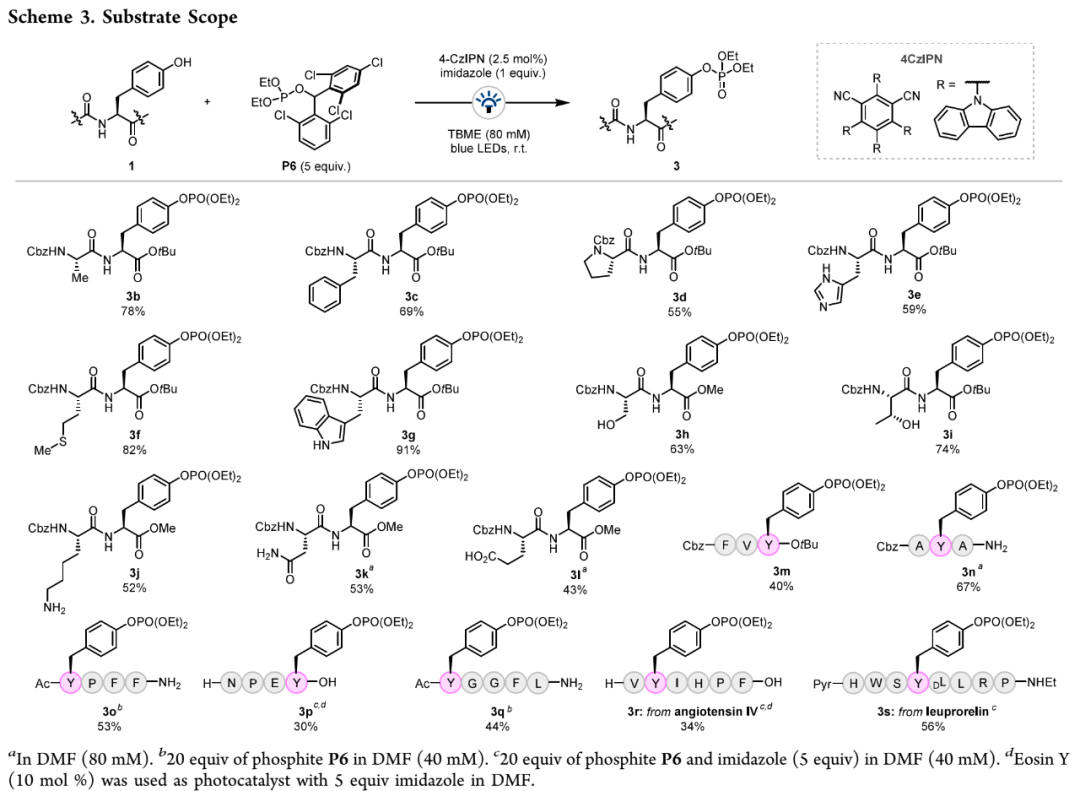
(Scheme 3,图片来源:J. Am. Chem. Soc.)
基于发展出的光催化自由基Arbuzov反应,Motomu Kanai课题组成功实现酪氨酸的选择性膦酸化。该方法为多肽中酪氨酸残基的膦酸化提供了一种新方法。
论文信息
Catalytic Phosphorylation of Tyrosine via a Radical Arbuzov Reaction
Benjamin D. A. Shennan, Tomoyuki Fukuta, Mina Yamane, Takashi Koyama, Harunobu Mitsunuma, and Motomu Kanai*
J. Am. Chem. Soc.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





