摘要:昆明学院梁德强/高树林&攀枝花学院孙绍光团队开发了一种光催化合成苯并[b]芴酮和苯并[b]芴醇的新方法。该方法以烯酮炔为原料,在无金属、无外加光催化剂和氧化剂的温和条件下,通过光诱导自催化实现了常规合成和连续流动合成。
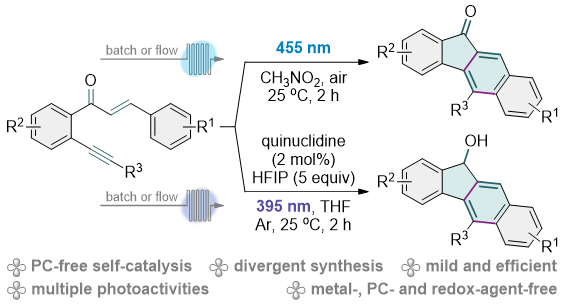
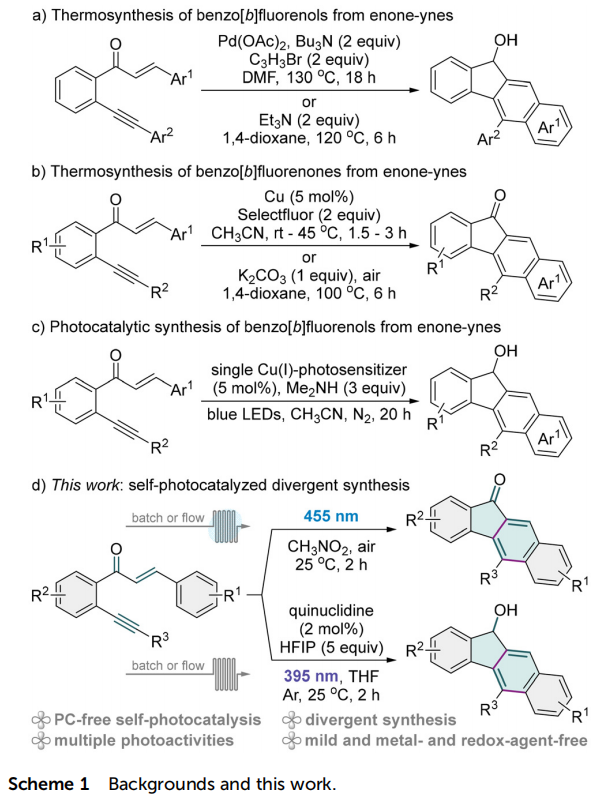
近年来,光催化作为一种高效且可持续的合成手段,在有机化学领域得到了广泛而深入的应用。然而,传统的光化学反应往往依赖于贵金属光催化剂,例如铱和钌的配合物,这无疑增加了反应的成本,限制了其广泛应用。因此,探索无需外部添加光催化剂的光反应路径,成为了当前研究的热点与前沿。近年来,尽管电子供体-受体光化学领域取得了显著的进展,但其应用仍然受到一定程度的限制,这主要是因为这类电子转移过程需要严格匹配的供体和受体。值得注意的是,一些底物分子在光激发下,能够自主参与光催化循环,实现电子、能量或原子的转移过程。这类光诱导自催化反应展现出巨大的应用潜力,但目前仍处于发展的初级阶段,有待进一步的研究与探索(图1)。
最近,昆明学院梁德强/高树林&攀枝花学院孙绍光团队开发了一种光催化合成苯并[b]芴酮和苯并[b]芴醇的新方法。该方法以烯酮炔为原料,在无金属、无外加光催化剂和氧化剂的温和条件下,通过光诱导自催化实现了常规合成和连续流动合成。该光催化体系涉及能量转移、单电子转移、氢原子转移及光化学环加成等多重反应活性。在蓝光照射下,体系通过超氧自由基和单线态氧介导的氢原子转移,实现了苯并[b]芴酮的氧化合成;而在紫光照射下,利用奎宁环作为氢原子转移催化剂,通过氧化还原中性途径合成了苯并[b]芴醇。该方法具有良好的底物普适性、流动合成兼容性,并在太阳光实验中展现出实际应用前景。相关的研究成果发表在有机化学领域知名期刊 Organic Chemistry Frontiers上 (Org. Chem. Front., 2025)。图1 研究背景和本工作(来源:Org. Chem. Front.)实验结果
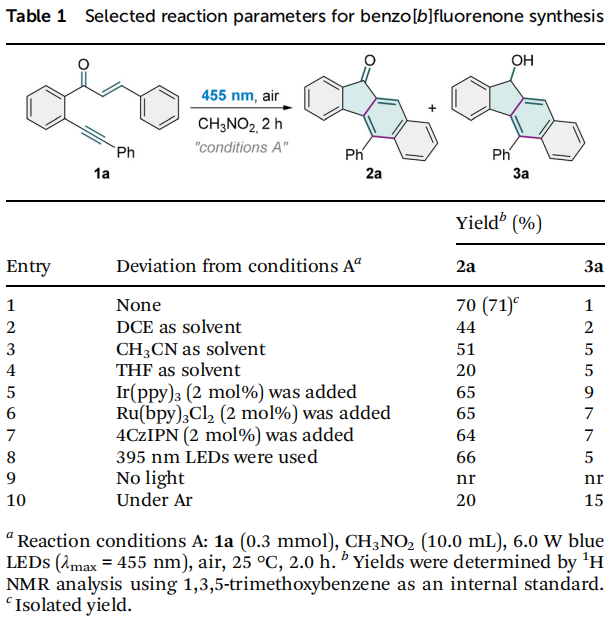
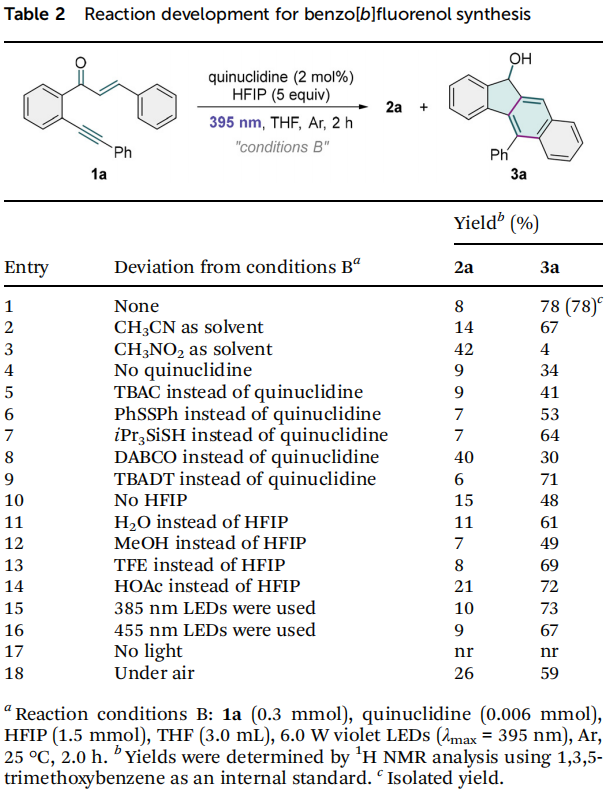
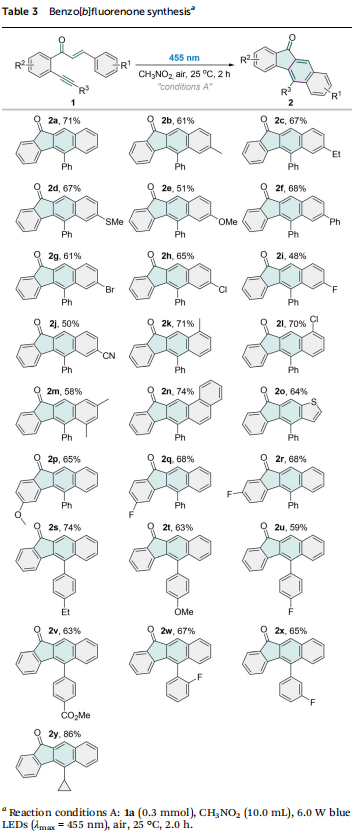
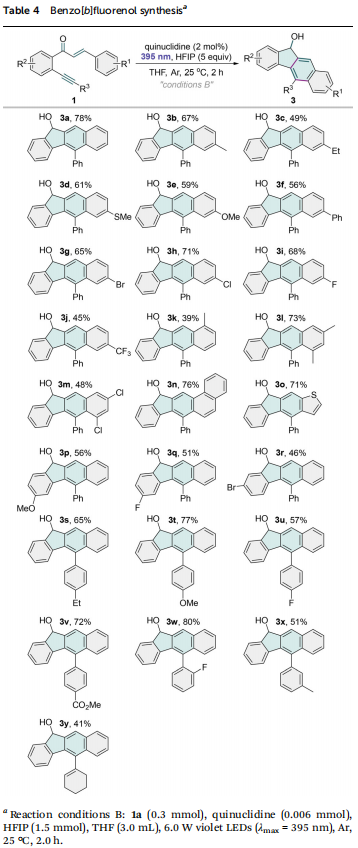
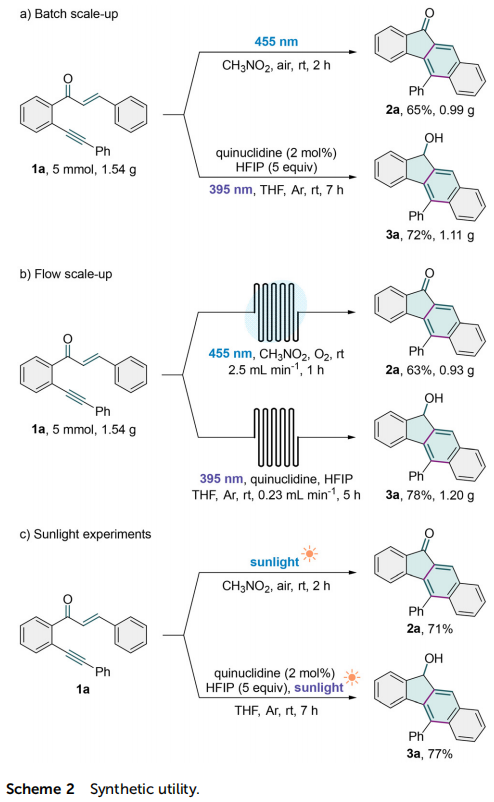
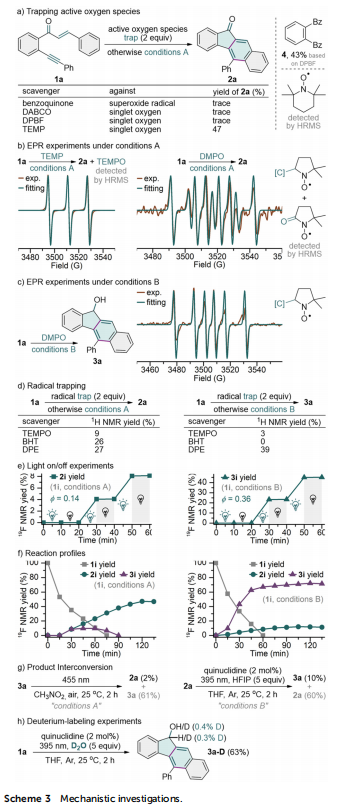
通过考察光源、溶剂、氧化剂和催化剂等要素,优化了苯并[b]芴酮2a和苯并[b]芴醇3a的合成条件。对于2a的合成,最佳条件为:在455 nm蓝光照射下,以CH3NO2为溶剂,空气为氧化剂,无需外加光催化剂,在25 °C反应2小时,此时分离产率为71%(表1)。光催化剂的加入未能提高产率。表1 苯并芴酮合成的关键反应参数(来源:Org. Chem. Front.)对于3a的合成,最优条件为:在395 nm紫光照射下,以THF为溶剂, HFIP为质子源,奎宁环为氢原子转移催化剂,在氩气氛围下反应2小时,此时分离产率为78%(表2)。HFIP和奎宁环的加入对反应至关重要,其他质子源或催化剂的使用均显著降低产率。光源波长也会影响产率,395 nm紫光效果最佳。无光条件下反应无法进行。使用空气氛围会降低3a的产率。表2 苯并芴酮合成的关键反应参数(来源:Org. Chem. Front.)在确定发散合成的两个最优条件A和B后,进行了底物适用性范围研究。A条件下,多种官能化的苯并[b]芴酮都可从烯酮炔一步合成(表3)。查尔酮β-环上的给电子基团(2b-2e)和吸电子基团(2g-2j)均与反应相容。4-苯基底物也顺利转化为7-苯基苯并[b]芴酮2f。空间位阻较大的2-甲基或2-氯查尔酮底物也转化为对应苯并芴酮2k和2l,产率未显著降低,表明反应对空间位阻不敏感。3,5-二甲基取代的1,6-烯炔的反应生成6,8-二甲基苯并[b]芴酮2m。噻吩杂环也可以被反应兼容(2o)。表3 苯并芴酮的合成(来源:Org. Chem. Front.)在B条件下,反应也能兼容查尔酮β-芳环对位上多种取代基,生成对应官能团化苯并[b]芴醇3b–3j(表4)。邻位甲基烯酮炔底物因空间位阻,对应9-甲基苯并[b]芴醇3k产率较低。6,8-二甲基或二氯取代的3l和3m也能从对应双取代烯酮炔底物合成。查尔酮β-位的1-萘基和2-噻吩基也被兼容,对应产物3n和3o产率较高。芳酰基苯环上4-位或5-位也可以被各种给电子基团(3p)和吸电子基团(3q和3r)取代。接着,本论文研究了炔基适用范围,结果表明多种取代的芳香炔烃均能有效参与该多重环化反应(3s–3x)。反应条件足够温和,可以兼容敏感的烯基基团(3y)。表4 苯并芴醇的合成(来源:Org. Chem. Front.)为了评估这两个自催化合成的实用性,首先在传统烧瓶中进行了放大反应(图2a),苯并[b]芴酮2a和苯并[b]芴醇3a的产率与0.3 mmol规模实验相当。然后,我们尝试在连续流条件下开展这两个反应(图2b)。通入氧气,在2.5 mL/min的流速下开展5 mmol级反应,苯并[b]芴酮2a的产率为63%,反应时间比常规反应缩短了2倍;氩气氛围下,在0.23 mL/min的流速下开展5 mmol级反应,苯并[b]芴醇3a的产率为78%。此外,这两个反应都可以使用自然阳光作为光源,产率几乎没有受到影响(图2c)。这些结果证明了当前方法在实际应用中的巨大潜力。图2 反应实用性研究(来源:Org. Chem. Front.)接下来研究了两个反应的机理,首先开展了活性氧物种的探测实验(图3a)。在A条件下,当向体系中引入超氧自由基捕获剂对苯醌或单线态氧捕获剂DABCO后,模型反应几乎被完全抑制。此外,DPBF捕获单线态氧生成了加合产物4,产率为43%。TEMP也与单线态氧发生反应转化为TEMPO,并被高分辨率质谱证实。基于上述实验结果,推测在A条件下,超氧自由基和单线态氧在苯并[b]芴酮的合成过程中都扮演着至关重要的角色。超氧自由基和单线态氧的存在进一步被电子顺磁共振(EPR)波谱证实。在A条件下加入TEMP捕获单线态氧,观察到明显的TEMPO信号。加入DMPO作为捕获剂,除了DMPO-碳自由基加合物信号,还观察到超氧自由基加合物被进一步氧化后的信号(图3b)。在B条件下采用DMPO作为捕获剂,也检测到DMPO-碳自由基加合物信号(图3c)。图3 机理实验(来源:Org. Chem. Front.)自由基捕获实验表明,两种条件下反应均经历自由基历程(图3d)。开关灯实验表明,光源关闭时反应停止(图3e),结合较小的量子产率,判断两个反应均经历短链的催化循环反应机理。开关灯实验和反应动力学曲线(图3f)均揭示两个反应都有明显的诱导期,可能是因为反应需要先积累某关键中间体。A条件下,醇产物3a不会高效转化为酮产物2a,B条件下,酮产物2a也不能高效转化为3a(图3g),表明两个产物的生成经历独立的反应路径,二者均不是另一产物的关键中间体。氘原子标记研究显示,产物3a羟基上的氢原子不是来自HFIP或H2O,可能来自分子内部(图3h)。
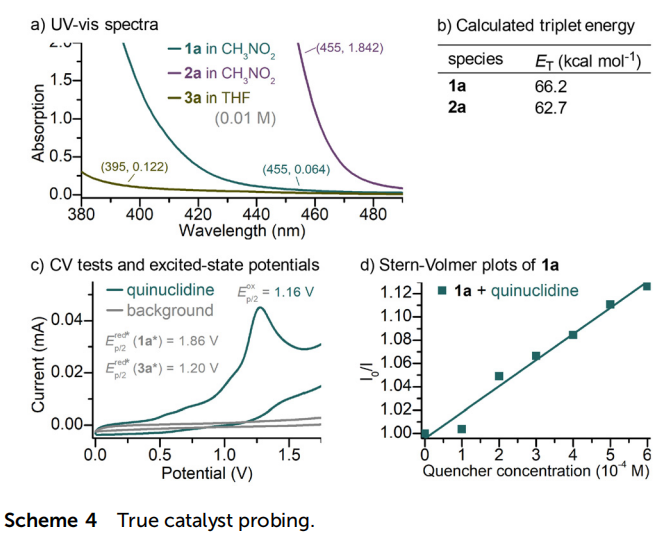
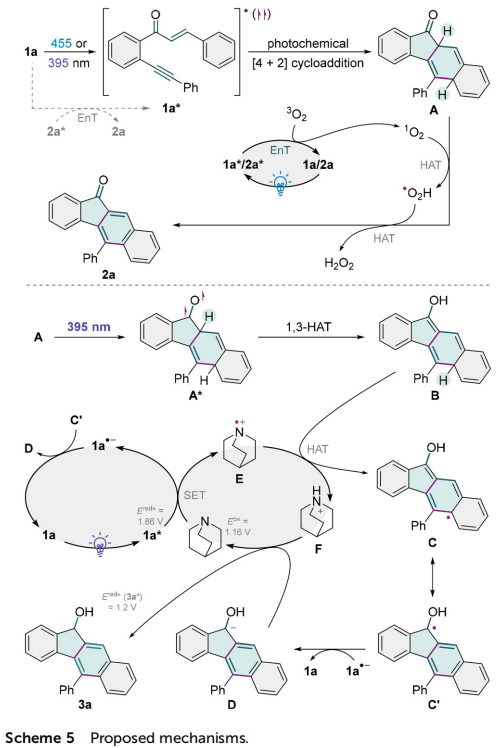
为确定真实光催化剂,本论文进行了紫外-可见光谱测试(图4a)。结果显示,产物苯并[b]芴酮2a在可见光区有明显吸收,底物烯炔酮1a在455 nm以上也有微弱吸收,表明在A条件下,1a和2a都有可能被蓝光直接激发。密度泛函理论计算表明, 1a和2a的三线态能量都较高,可以将激发态能量转移给基态氧产生单线态氧(图4b),但2a的三线态能量略低于1a,因此反应不会经历光吸收能力更强的产物2a先被激发再将能量转移给1a的过程。因此,A条件下,1a和2a都充当反应的直接光敏剂,它们受光激发后,再发生能量转移将三线态氧敏化为单线态氧。另一方面,醇产物3a在395 nm有微弱吸收。虽然计算得到的1a的激发态还原电势很高,足以氧化奎宁环(图4c),但是3a的激发态还原电势与奎宁环氧化电位相当,所以1a更可能是B条件下的光催化剂。荧光淬灭研究也证实,奎宁环能显著减弱1a的荧光(图4d)。图4 真实催化剂研究(来源:Org. Chem. Front.)本论文提出了以下反应机理(图5)。在吸收蓝光或紫光后,烯炔酮1a被激发至1a*,然后发生[4 + 2]环加成生成二氢苯并[b]芴酮A。在A条件下,1a*或2a*通过能量转移活化3O2生成1O2,后者与A发生两次氢原子转移,最终生成苯并[b]芴酮2a。在B条件下,中间体A经紫光激发后发生分子内1,3-氢转移,生成5aH苯并[b]芴醇B。同时,另一分子1a吸收光子形成1a*,氧化奎宁环生氮鎓离子自由基E和还原态催化剂1a•−。E与B发生分子间氢转移,生成碳自由基C和质子化奎宁环F。C的共振结构中,芳环α-碳自由基C'占主导,其被1a•−还原生成芳环α-碳负离子D和基态1a,实现光催化剂的再生。DFT计算表明,F的酸性强于HFIP、H2O和D2O,因此F优先对中间体D进行质子化,生成苯并[b]芴醇3a并实现奎宁环的再生。图5 反应机理 (来源:Org. Chem. Front.)
总结
昆明学院梁德强/高树林&攀枝花学院孙绍光团队开发了一种光催化合成苯并[b]芴酮和苯并[b]芴醇的新方法。该方法以烯酮炔为原料,在无金属、无外加光催化剂和氧化剂的温和条件下,通过光诱导自催化实现了常规合成和连续流动合成,具有高效率和良好的官能团耐受性。该光催化体系涉及能量转移、单电子转移、氢原子转移及光化学环加成等多重反应活性,这项工作为光诱导自催化的发展提供了新的见解。
文章通讯作者为昆明学院化学化工学院梁德强教授,高树林副教授和攀枝花学院孙绍光博士,第一作者为昆明学院硕士生史吉富。该项工作得到了国家自然科学基金项目,云南省贵金属实验室开放项目等项目支持。声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。