南京工业大学褚雪强/沈志良团队Org. Lett.:光催化多氟烷基四氢萘酮与亚磺酸盐的脱氟环化反应
为了高效合成高度官能化的γ-吡喃酮,南京工业大学褚雪强与沈志良团队报道了一种钌催化多氟烷基四氢萘酮脱氟环化的反应。该反应在可见光的照射下,利用亚磺酸盐(如苯亚磺酸钠)作为氧源和脱氟促进剂,通过选择性活化全氟烷基链上三个碳位点的五个C(sp3)-F键,实现了具有α-全氟烷基和β-氟取代的γ-吡喃酮的精准合成。此方法具有优异的化学选择性和区域选择性,且反应条件温和,为促进多氟烷基四氢萘酮合成有机氟化物提供了一种新的方法。相关成果在线发表于Organic Letters。
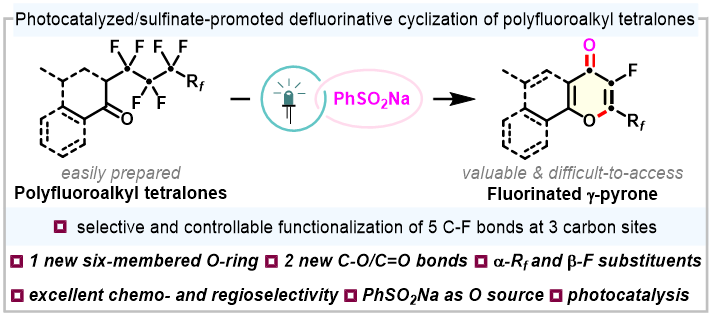
(来源:Org. Lett.)
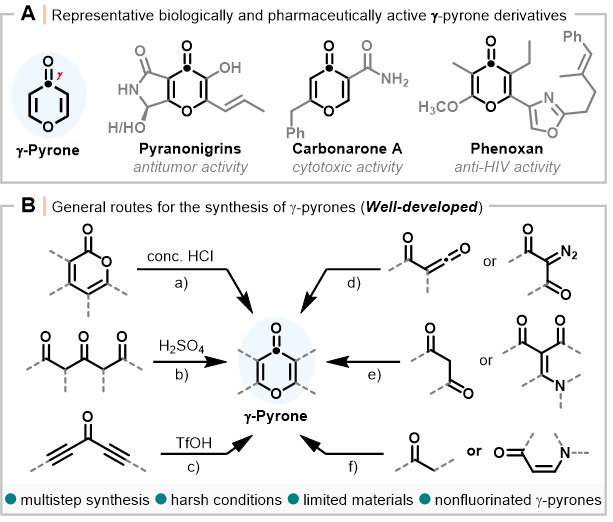
图1合成多取代γ-吡喃酮的杂环化方法
Scheme 1 Methods for the heterocyclization of polysubstituted γ-pyrones(来源:Org. Lett.)
γ-吡喃酮是天然产物和生物活性分子中的重要结构单元,具有抗肿瘤、抗HIV等药理活性,如吡喃尼格林、碳酮A (Scheme 1, A)。传统合成γ-吡喃酮的方法具有复杂的多步操作、对羰基底物的依赖、苛刻的反应条件以及较低的反应效率等缺点 (Scheme 1, B)。研究表明,选择性活化多氟烷基四氢萘酮多个碳位点的四个或六个C-F键,可以为难以获得的少氟杂环骨架提供方法,这些骨架在药物研发和材料科学中具有一定的潜力。然而,直接脱氟构建吡喃酮较难实现,主要是因为C-F键的高化学键能和热稳定性,以及多个C-F键官能化的选择性和可控性 (Scheme 2, C)。
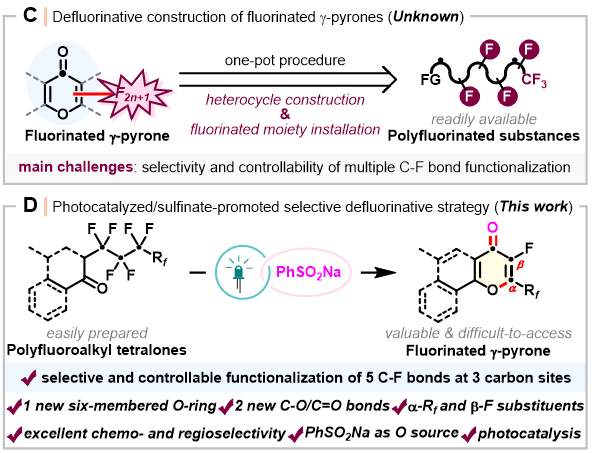
图2 合成路线
Scheme 2 Synthetic routes
(来源:Org. Lett.)
南京工业大学褚雪强团队设想了一种钌催化脱氟环化反应:在可见光照射下,多氟烷基四氢萘酮与苯亚磺酸钠合成γ-吡喃酮化合物的反应 (Scheme 2, D)。与之前建立的碱促进体系和钯催化体系不同,该反应巧妙利用温和的可见光诱导光催化策略,实现了全氟烷基链上三个不同碳位点处五个C(sp3)-F键的选择性及可控官能化,从而拓展了多氟烷基化合物脱氟的领域。该脱氟反应的优势包括:(1)对多个高度稳定的C(sp3)-F键的官能化具有良好的化学选择性,不受竞争性C-C键断裂的影响;(2)在单一过程中成功合成一个六元氧杂环和两个新的C-O/C=O键,且钌配合物的负载量低;(3)能够精确地引入α-全氟烷基和β-氟取代基,获得γ-吡喃酮骨架;(4)亚硫酸钠具有作为羰基的氧源以及脱氟促进剂的双重作用;(5)具有进一步衍生化的潜力,可转化为其他结构上有用的有机氟化物。该反应通过光催化与亚磺酸盐的协同作用,解决了多氟烷基四氢萘酮的选择性脱氟环化的难题。
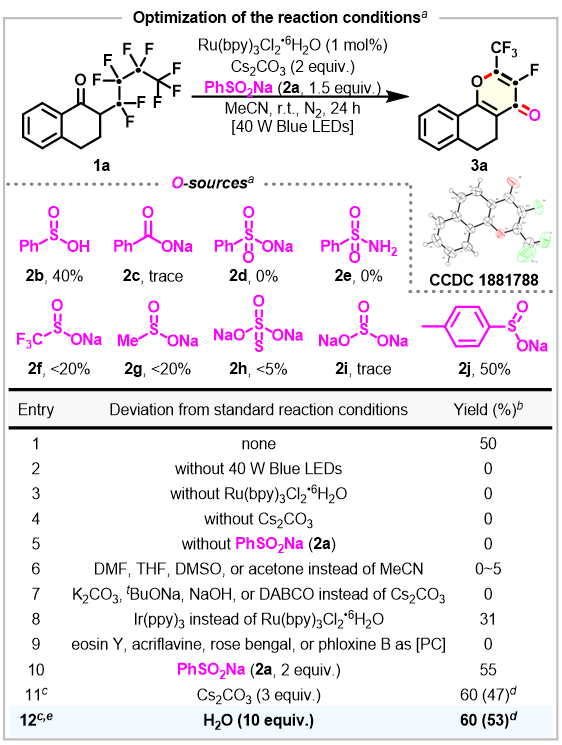
图3 反应条件的优化
Scheme 3 Optimization of the reaction conditions
(来源:Org. Lett.)
首先,作者用2-(全氟丁基)-3,4-二氢萘-1(2H)-酮(1a)和苯亚磺酸钠(2a)在光催化剂Ru(bpy)3Cl2·6H2O的存在下,以Cs2CO3作为碱,MeCN作为溶剂,在蓝色LED灯照射下反应24小时,以50%的核磁产率得到了3-氟-2-(三氟甲基)-4-吡喃酮(3a) (Scheme 3)。作者发现在该反应中苯亚磺酸钠起到了一个提供氧源和脱氟剂的作用,所以又筛选了其他氧源2b-2j,效果都不如苯亚磺酸钠好。之后进行反应条件的优化,筛选了不同的溶剂(如DMF、THF、DMSO、丙酮等)、碱(如K2CO3、tBuONa、NaOH、DABCO等)、光催化剂(Ir(ppy)3、曙红Y、吖啶黄、玫瑰红等),发现还是以钌作为光催化剂,Cs2CO3作为碱,在乙腈溶剂中产率最高。另外,作者将PhSO2Na和Cs2CO3的当量增加后发现产率有所提高,可能是由于Cs阳离子与C-F键之间的相互作用更有利于脱氟。值得注意的是,作者考虑到由于盐的溶解度差可能导致反应的重复性不一致,所以选择加入10当量的水来缓解这一问题,最终得到核磁产率60%,分离产率53%的3a。
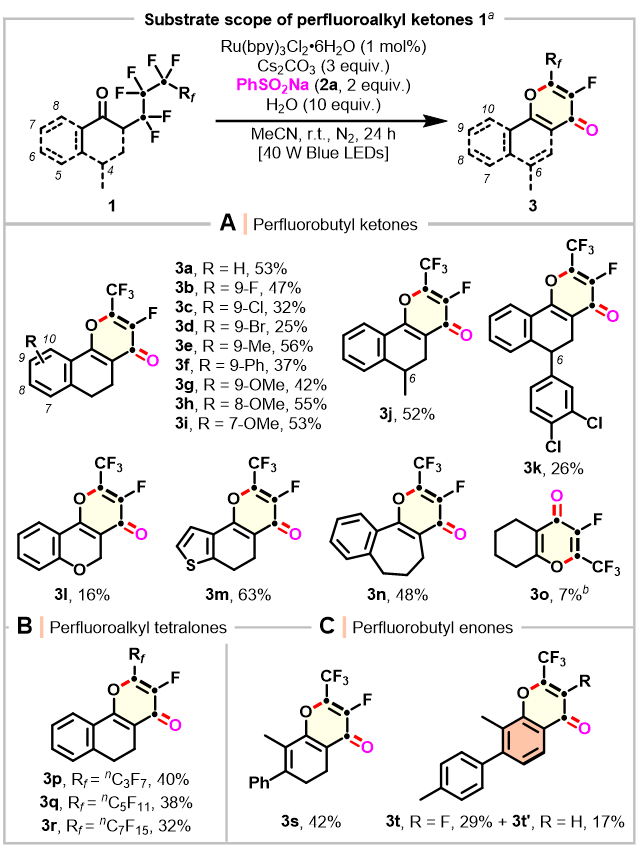
图4 多氟烷基酮底物范围的拓展
Scheme 4 Substrate scope of polyfluoroalkyl ketones
(来源:Org. Lett.)
在确定了最优反应条件后,作者对各种多氟烷基四氢萘酮进行底物拓展。首先是苯环C7-C9上具有不同电子效应和空间效应的取代基,如F、Cl、Br、OMe等,可以以中等的产率得到相应的目标产物3b-3i (Scheme 4)。在温和的光催化反应条件下,这些官能团均有良好的耐受性,具有进一步合成修饰的潜力。同样,C4位置被烷基或芳基部分取代的多氟烷基四氢萘酮1j和1k也可以顺利转化为产物3j和3k,产率分别为52%和26%。尽管当底物1l被氧原子取代时反应性降低,产率为16%。此外,杂环和七元环的底物1m和1n并未干扰脱氟反应,以中等产率得到目标产物3m和3n。然而,底物1o对于这种转化效率降低。此外,作者发现不同全氟烷基链的链长(C3-C7)对反应效率的影响微乎其微,生成了相应的全氟烷基化产物3p-3r,产率为32-40%。值得注意的是,通过使用全氟丁基环己烯酮作为反应底物,可以以中等的产率生成目标产物3s和意外的芳香化产物3t/3t’。
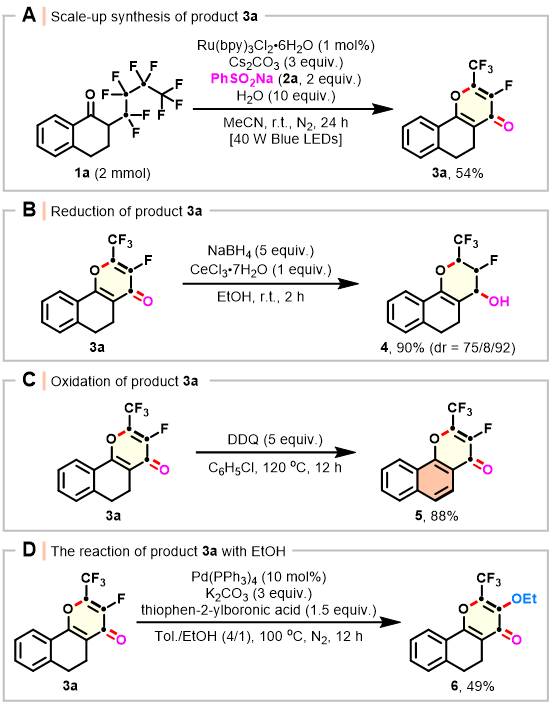
图5 放大合成和进一步转化
Scheme 5 Scale-up synthesis and synthetic transformations
(来源:Org. Lett.)
然后作者进行了2 mmol的放大反应,反应产率和选择性并没有降低,能以54%的分离产率得到目标产物 (Scheme 5, A)。接下来是对3a的进一步后期官能化,首先,通过Luche还原3a上的不饱和C-C双键和羰基,以90%的产率得到还原产物4 (Scheme 5, B)。此外,通过DDQ对3a进行氧化,可以以88%的产率得到芳构化产物5 (Scheme 5, C)。最后,在钯的催化下,3a与乙醇进行反应,可以以39%的产率得到脱氟产物6 (Scheme 5, D)。
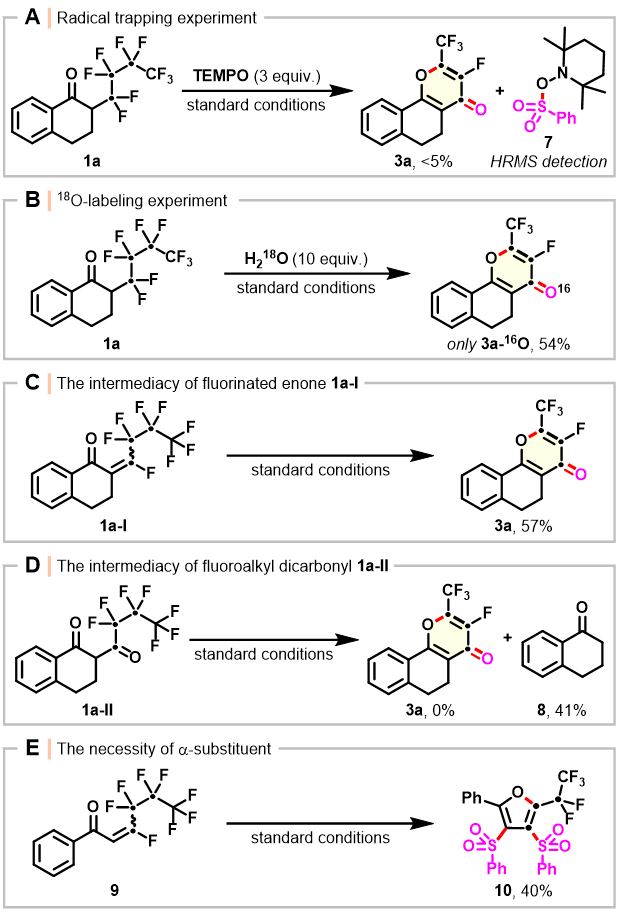
图6 机理研究
Scheme 6 Mechanistic studies
(来源:Org. Lett.)
为了进一步了解多氟烷基四氢萘酮的光催化脱氟环化机理,作者进行了一系列的机理研究。首先,作者发现加入TEMPO后,模板反应几乎被抑制,并且可以通过高分辨质谱(HRMS)检测到TEMPO-SO2Ph加成物7,这一结果表明该反应是个自由基反应 (Scheme 6, A)。随后,在标准条件下,用18O标记的水与1a反应,产物只得到了16O的3a。这一结果表明了水不是脱氟环化的氧源 (Scheme 6, B)。接下来,将预合成的多氟烯酮1a-I,在标准条件下进行反应,可以以57%的产率转化为所需的产物3a,所以作者推测1a-I可能是该反应的中间体 (Scheme 6, C)。相比之下,使用1,3-二羰基化合物1a-II作为底物则不能得到产物3a,并分离出了脱羰基的四氢萘酮8,产率为41%,因此排除了1,3-二羰基中间体的参与 (Scheme 6, D)。最后,为验证多氟烷基四氢萘酮上羰基相邻的α-烷基取代基对该转化的重要性,作者将氟化烯酮在标准条件下进行反应,发现仅以40%的产率得到了二磺酰化呋喃,并未得到目标产物3a (Scheme 6, E)。
综上所述,南京工业大学褚雪强团队开发了一种在可见光照射下钌催化多氟烷基四氢萘酮脱氟环化的方法。该反应通过选择性活化全氟烷基链上三个不同碳位点的五个C(sp3)-F键,能以中等至良好的产率合成γ-吡喃酮。此外,该方法具有良好的官能团耐受性和可扩展性。值得注意的是,亚磺酸盐在光催化条件下兼具双重功能:既作为产物羰基的氧源,又作为脱氟的促进剂。这种独特的双重作用为促进多氟烷基四氢萘酮合成有机氟化物提供了一种新的方法。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





