山东大学史大永教授课题组Org. Lett.:借助光活化硝基芳香化合物对非活化烯烃完成厌氧型1,2-/1,3-三氟甲基羟基化反应
第一作者:石聪
通讯作者:山东大学史大永教授、刘瑞华副研究员
β-/γ-三氟甲基醇是两类重要的分子结构,广泛存在于多种活性分子之中。因此,合成化学工作者一直致力于开发新颖的合成方法来构建此二种功能分子。基于烯烃的廉价易得性,且可在一步反应中引入两种官能团的高效性,烯烃的三氟甲基羟基化成为构建β-/γ-三氟甲基醇的常用的有效手段。但是,目前关于烯烃三氟甲基羟基化反应的合成办法存在着诸多缺点,如:(1) 依赖于光催化剂或过渡金属催化剂;(2) 外加酸碱造成的苛刻的反应条件;(3) 氧气与有机溶剂的混合造成潜在的爆炸风险;(4) 拘泥于活化类烯烃底物;(5) 有待开发的1,3-三氟甲基羟基化反应。近年来,硝基芳香类化合物作为烯烃羟基化试剂的相关工作被不断报道,但是,借助于此类廉价易得的化学品在烯烃官能团化过程中引入多样取代基的工作,还未有报道。
基于上述研究背景,作者希望通过在反应体系中引入还原性三氟甲基试剂CF3SO2Na (Langlois reagent),借助于硝基芳香化合物的光化学特性,对非活化烯烃类底物完成三氟甲基羟基化,构建三氟甲基醇类分子。工作伊始,作者首先为此反应寻找一个最优的硝基芳香化合物作为氧源。经过系统性的筛查,作者发现芳环上带有吸电子基团的硝基芳香试剂效果优于带给电子基团的。可能是由于吸电子基团会增加光活化硝基芳香化合物的亲电性,且使电子转移后的硝基自由基负离子更加稳定,利于电子转移过程,从而促进三氟甲基自由基的产生。其中,又以对乙酯基硝基苯效果最佳。而后,作者又对其他反应条件进行系统性筛选,从而确定最优反应条件:在1.5倍当量CF3SO2Na,2.0倍当量对乙酯基硝基苯参与下,在405 nm蓝光灯照射下,氩气环境,室温搅拌16小时,模型产物4a(结构见图2, a)可以69%分离收率获得。接下来,作者又对反应的底物适用性以及官能团兼容性进行考察(图1)。发现,带有各种官能团(如:酯基、酰胺、酰亚胺、三级胺及砜)的末端烯烃,均可很好兼容于反应体系,以48%-64%分离收率得到相应产物4b–4f。烯丙基芳香底物也可参与反应,以35%分离产率得到产物4g。此外,此反应也可适用于1,1-/1,2-双取代和1,1,2-三取代烯烃,相应产物4h–4j可以32%-52%产率分离得到。作者还完成了11例功能分子的后期修饰,1,2-三氟甲基羟基化产物4k-4u分别以33%-73%分离产率获得。但是,芳基乙烯类底物对此反应不兼容。基于此前作者课题组关于1,2-酰基迁移策略的相关工作 ,作者尝试将反应体系应用于烯丙基酮类底物。通过自由基介导的1,2-酰基过程,可以30%-75%分离产率得到1,3-三氟甲基羟基化产物4v–4ae。据作者所知,这是首次通过烯烃的1,3-三氟甲基羟基化构建γ-三氟甲基醇类分子。
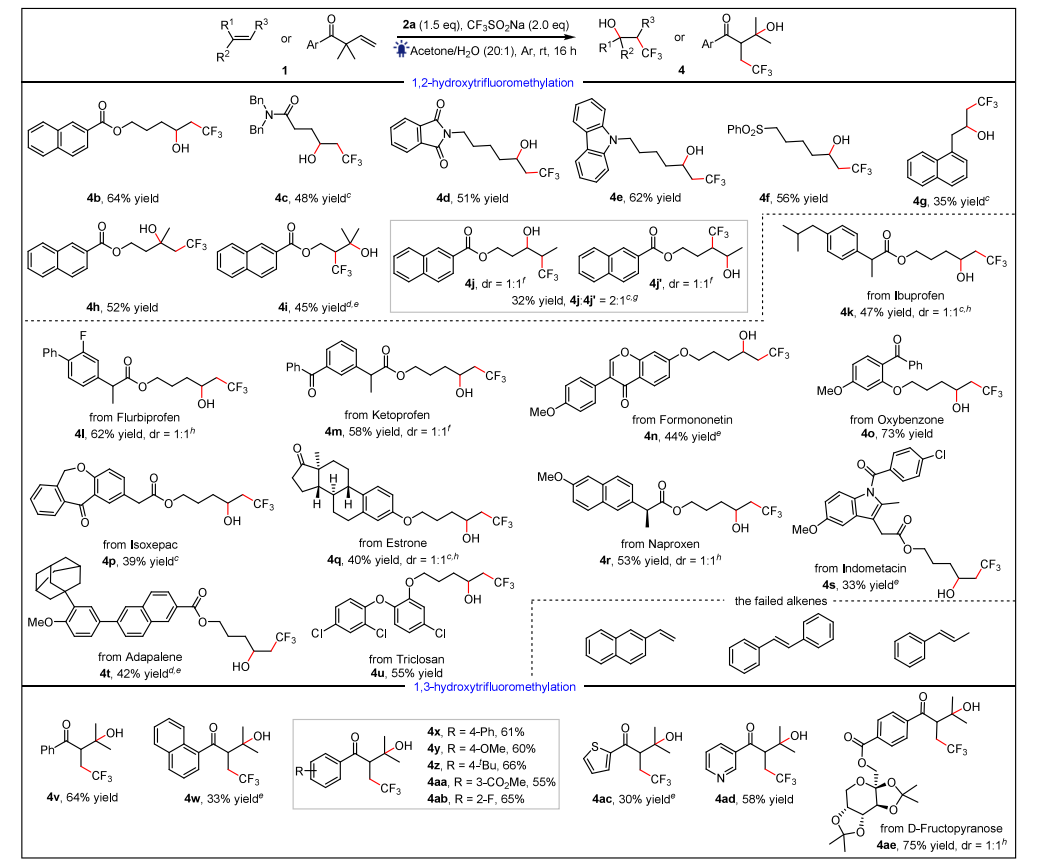
图1. 1,2-/1,3-三氟甲基羟基化底物适用性(来源:Org. Lett.)
为了说明此反应的应用性,作者进行了克级实验。在10 mmol级别放大时,可以61%分离收率得到2.16克模型产物4a(图2, a)。 此外,4a中羟基可以向其他多种官能团进行衍生,如脱氧氟化(5a, 70%收率)、酯化(5b, 81%收率)及脱氧氯化(5c, 54%收率)。为了探究反应历程,作者又进行了一系列机理验证实验。在反应体系中加入2倍当量TEMPO试剂,反应被完全抑制,取而代之的是,可通过核磁氟谱检测到157%自由基加合物6a和35%的6b产生(图2, b)。而进行紫外-可见吸收实验时,CF3SO2Na和对乙酯基硝基苯的混合物吸收曲线相较于单一组分,并没有明显的红移(图2, e);可排除在反应体系中,CF3SO2Na和对乙酯基硝基苯之间形成电子给体-受体复合物(EDA),而反应的进行是借助于光活化产生的三线态硝基苯类物种。结合自由基加合物6b的产生、文献报道的氧化还原电势{E1/2red = [ArNO2*/ArNO2•−] = +1.50 V vs SCE, Eoxd = [CF3SO2−/CF3SO2•] = +1.05 V vs SCE},作者合理地提出:在反应过程中,三线态硝基芳香化合物与三氟甲基亚磺酸根之间发生单电子转移,伴随着SO2的离去而产生三氟甲基自由基。为了捕捉反应中间体,在以底物1v进行反应仅4小时后将反应停掉,通过高分辨质谱检测到羟胺中间体7的存在(图2, c)。为了说明氧源,用H218O进行反应,并未检测到18O标记的产物,从而排除水作为氧源的可能,而说明羟基化氧源为硝基芳香化合物(图2, d)。开关灯实验说明持续光照对反应的进行是必要的(图2, f)。
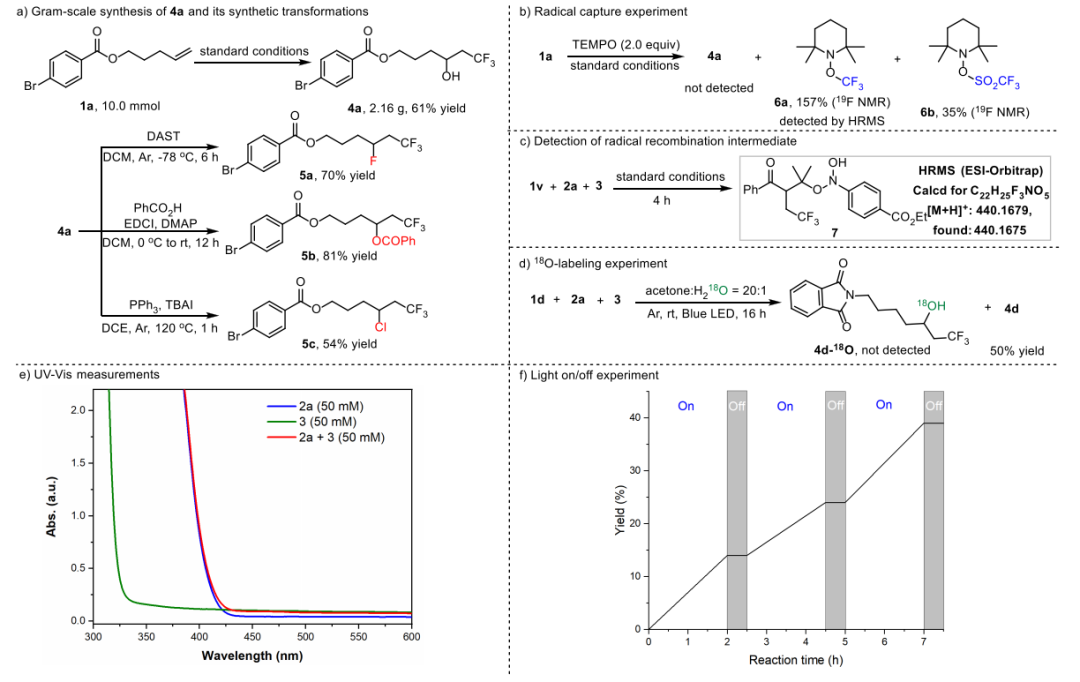
图2. 克级实验、衍生化、机理验证(来源:Org. Lett.)
基于上述机理实验以及相关文献报道,作者对此反应提出以下机理(图3, a):硝基芳香化合物经光激发成为三线态物种T-2,T-2与CF3SO2Na发生单电子转移后得到自由基负离子8和三氟甲基自由基(伴随SO2的离去),三氟甲基自由基对烯烃底物碳碳双键部分进行加成后得到烷基自由基中间体9。9与8经自由基偶联生成自由基氧负离子10,后者经质子化得到羟胺中间体11。除此之外,11还可由8先经质子化生成氧自由基12,再与烷基自由基9偶联得到。值得注意的是,当使用烯丙基酮底物进行反应时(图3, b),三氟甲基自由基对烯烃进行自由基加成后得到二级烷基自由基中间体13,经环氧化生成烷氧自由基14,伴随着1,2-酰基迁移,得到更为稳定的三级烷基自由基9,继续进行图3, a中反应路径。
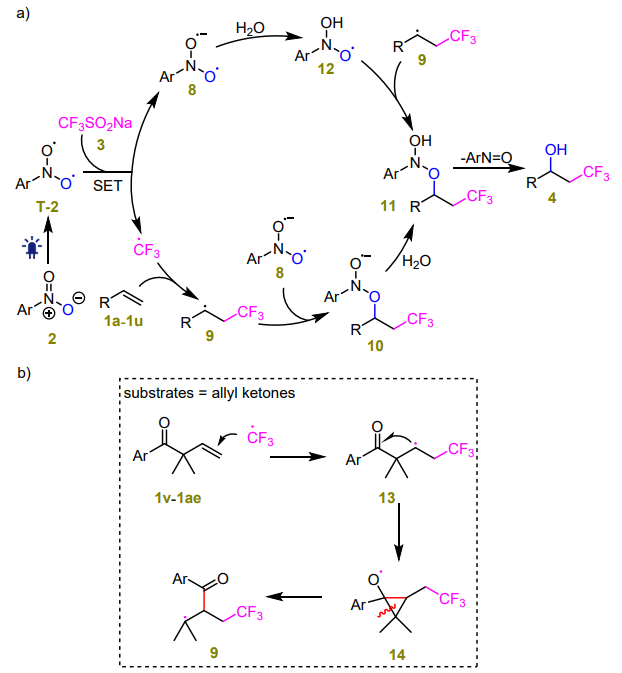
图3. 反应机理(来源:Org. Lett.)
此工作通过借助硝基芳香化合物独特的光化学特性,在无氧、无光/过渡金属催化剂条件下,完成了对非活化烯烃的1,2-/1,3-三氟甲基羟基化过程,构建β-/γ-三氟甲基醇两类功能骨架。反应条件温和,底物适用性、官能团兼容性佳。为廉价易得的硝基芳香化合物的光化学性质的拓展及应用提供了新思路。
论文信息:
Anaerobic 1,2-/1,3-Hydroxytrifluoromethylation of Unactivated Alkenes Enabled by Photoexcited Nitroarenes
Cong Shi, Ruihua Liu,* Zemin Wang, Chenxia Gao, Jia-Shu Chen, Hongyun Qin, Wenlong Shan,Wenli Zhuang, Nan Zhou, Xiangqian Li, and Dayong Shi*
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





