Nature:光诱导噻唑骨架原子及取代基的相互替换
前沿
富电子杂芳环在药物化学领域被视作“优势骨架”,然而,由于合成方法的瓶颈实现这类杂芳环的骨架编辑相当困难。例如,噻唑是药物中第五大芳香族化合物,但是其异构体异噻唑甚至没有进前100名。这种不平衡清楚的反映了合成策略面临的挑战,尤其是将这些结构引入药物分子中。传统策略构建噻唑依赖于缩合化学中适当官能化前体的多步制备,但异噻唑的合成要困难许多(图1a)。另外,反应位点的选择性及交叉偶联反应中的官能团耐受性也面临重大挑战。近年来,过渡金属催化C-H键活化或自由基促进的噻唑合成备受瞩目,但是取代基的位置聚焦于C2,对于C4或C5取代的噻唑合成仍然悬而未决。另外,在合成化学中骨架结构不变,但是取代基团的位置改变也能够显著影响化合物的理化性质。与此同时,先前对噻唑/异噻唑光化学研究提出,通过激发态4π电环化形成Dewar中间体(价键互变异构体),然后进行“硫原子行走”,或硫酮氮丙烯物种然后环化(图1c)。但是,需要使用高能汞灯,并且通常以较低收率得到混合产物。基于此,德国亚琛工业大学Alessandro Ruffoni/Daniele Leonori报道了,光激发噻唑形成单线态激发态π,π*结构,随后发生系列结构重排得到环体系原子替换或取代基位置变换的化合物DOI:10.1038/s41586-024-08342-8(图1)。
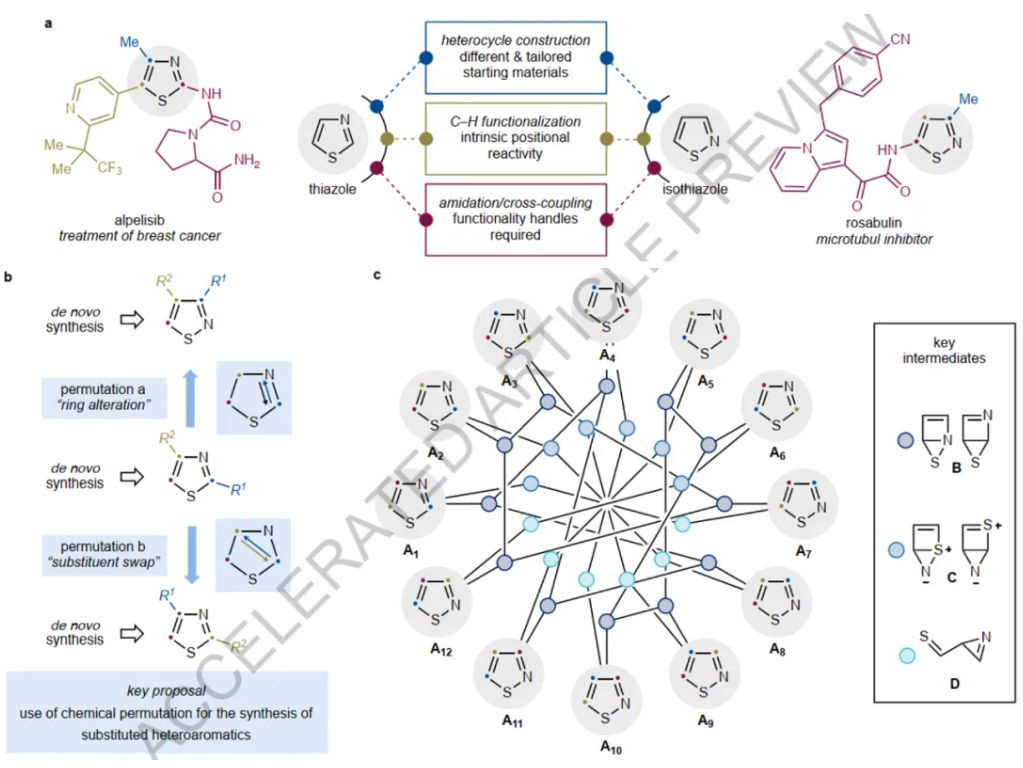
图1来源Nature
实验结果
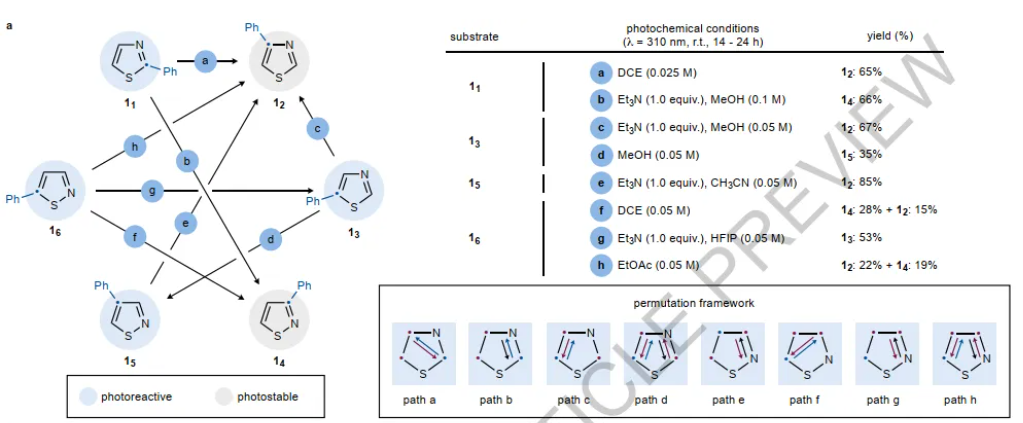
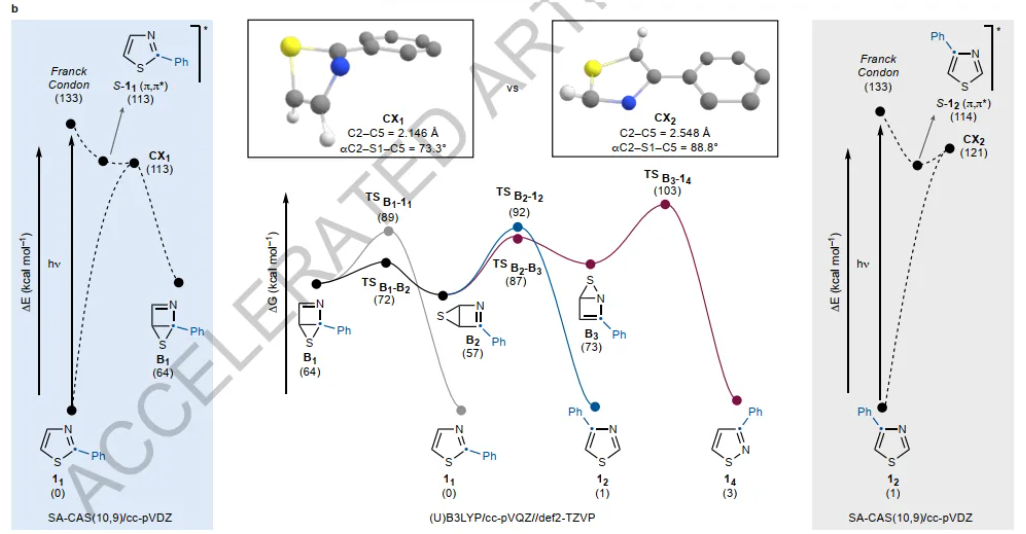
图2来源Nature

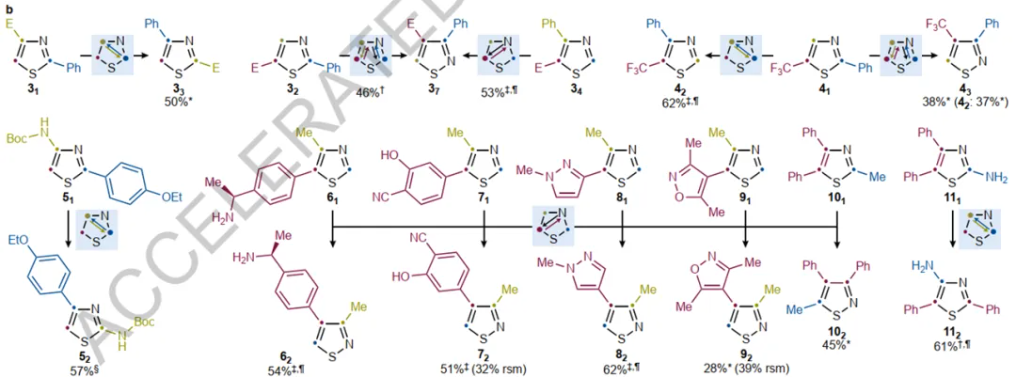
图3来源Nature
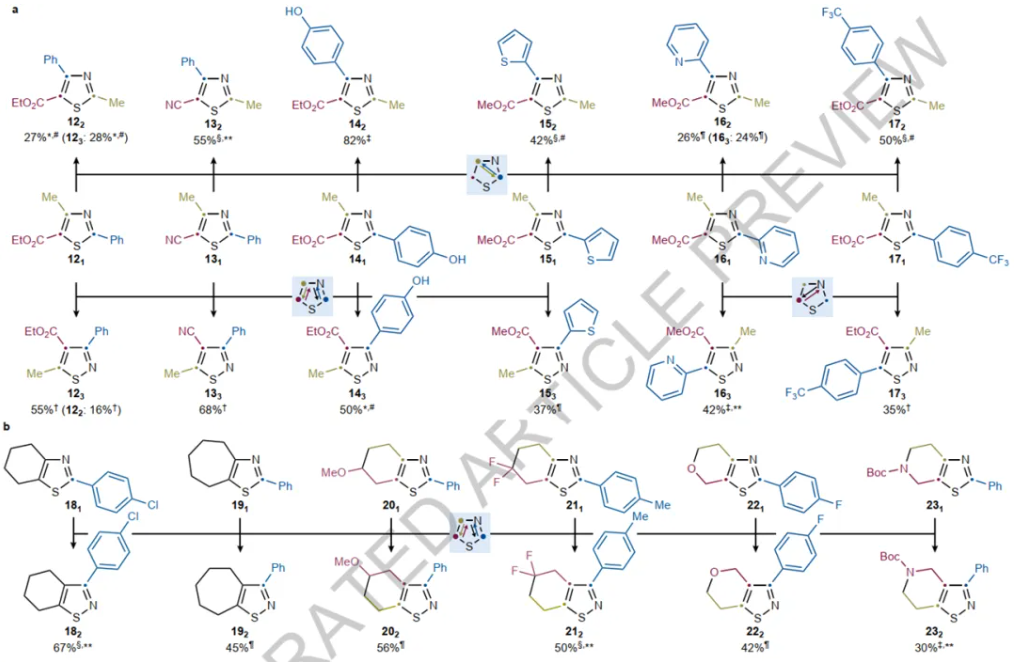
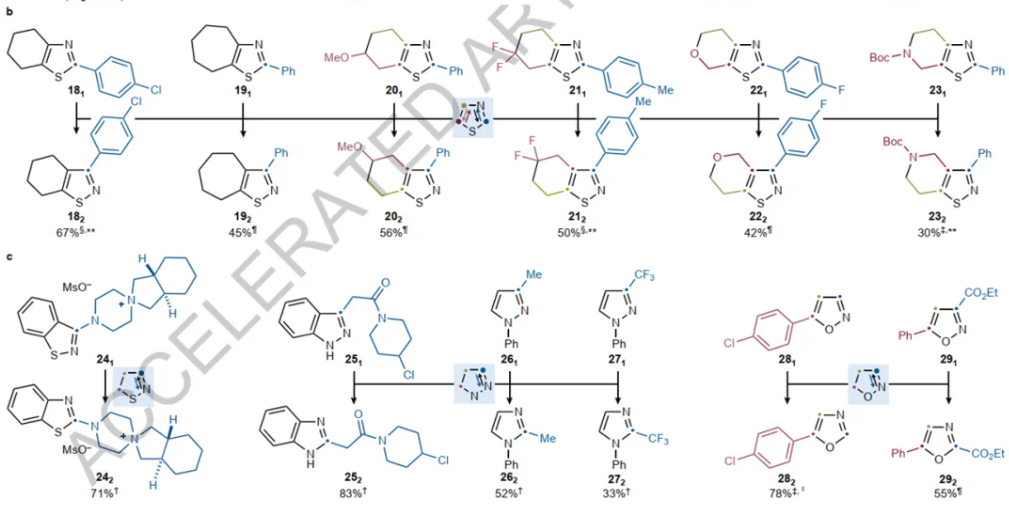
图4来源Nature
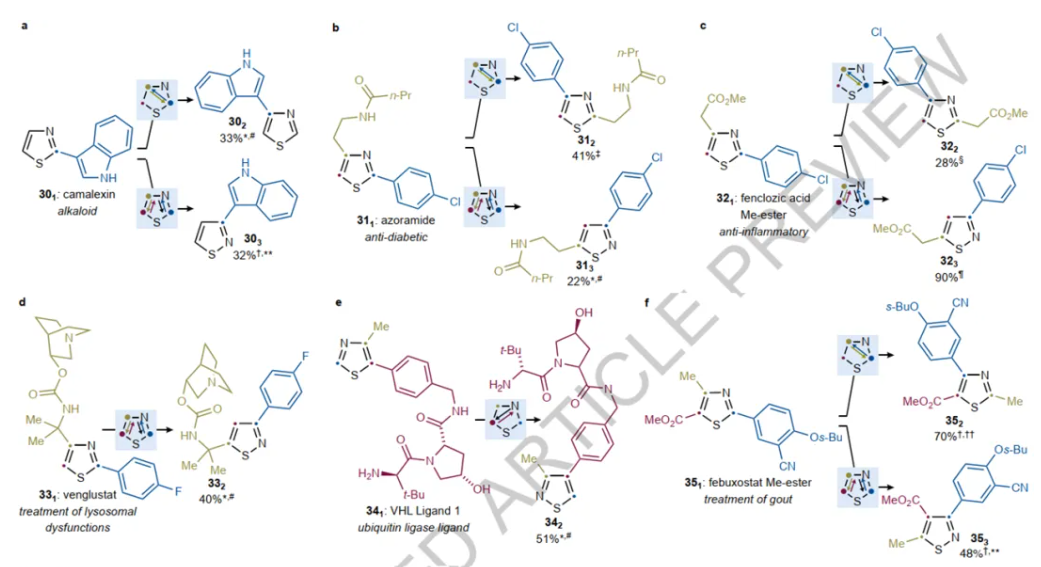
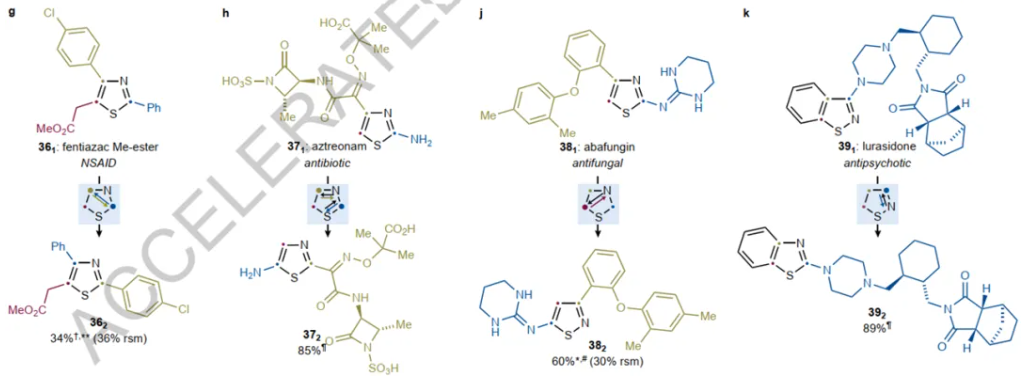
图5来源Nature
编者结语
Alessandro Ruffoni/Daniele Leonori利用光激发噻唑形成单线态激发态π,π*结构,随后进行选择性的进行骨架编辑。并且,这类策略对苯并[d]异噻唑、吲唑、吡唑和异噁唑同样适用。
Baptiste Roure, Maialen Alonso,† Giovanni Lonardi,† Dilara Berna Yildiz, Cornelia S. Buettner, Thiago dos Santos, Yan Xu, Martin Bossart, Volker Derdau, María Méndez, Josep Llaveria, Alessandro Ruffoni,* and Daniele Leonori*
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





