重庆大学熊阳课题组Angew. Chem.:可见光介导双自由基氢原子转移的硅基亚胺与烯烃[4+2]环化反应
导语
近日,重庆大学药学院熊阳课题组利用可见光介导的双自由基氢原子转移(DHAT)策略,实现了邻烷基芳基硅基亚胺、邻甲酰芳基硅基亚胺和烯烃的[4+2]环化反应。通过与马德里康普顿斯大学Fernández课题组合作,利用机理实验和DFT计算研究,认为硅基取代基能有效促进能量转移,形成关键的C,N-双自由基中间体,进行C-H键的氢原子转移反应和后续与烯烃[4+2]环化反应。相关研究成果近期发表于Angew. Chem.。
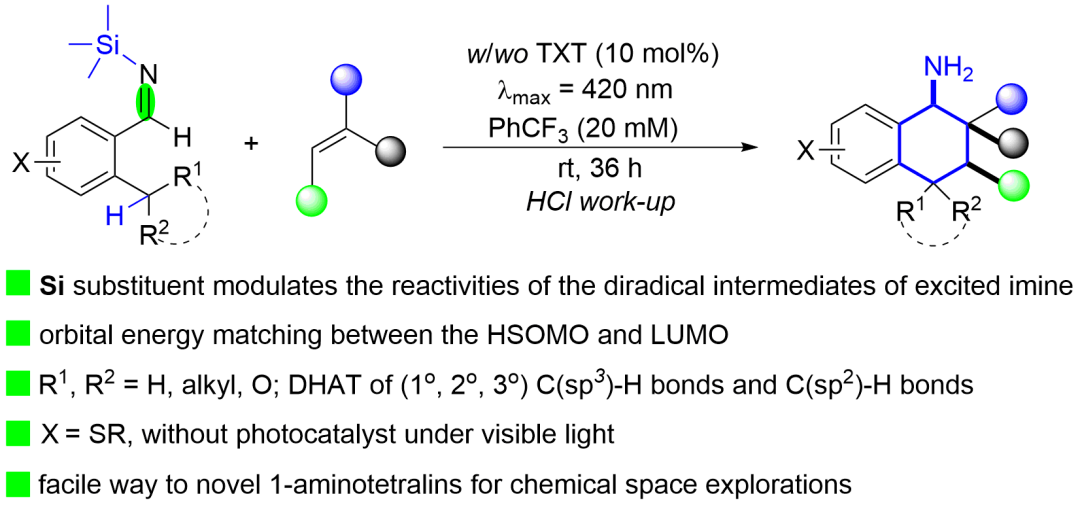
(来源:Angew. Chem.)
四氢-1-萘胺骨架存在于许多天然产物、生物活性分子和药物分子中。如:药物分子盐酸舍曲林;生物活性分子鬼臼毒素衍生物等。因此,高效简洁合成四氢-1-萘胺骨架来实现化学空间的拓展具有重要意义。目前该类分子的合成取得了一些进展,这其中通过亚胺苄位的C(sp3)-H转化的[4+2]环化策略是一种具有优异原子及步骤经济性的方法。尽管如此,亚胺的激发态为其碳氮双键的光化学转化反应带来了较大困难。事实上,由于激发态的亚胺nπ*特性降低,激发态的亚胺光化学反应活性相对有限。此外,固有的E/Z异构化对亚胺激发态反应活性的不利影响也极大地阻碍了其光化学转化的发展。近年来,随着可见光化学的复兴,化学家们在该领域利用双自由基中间体逐渐拓宽亚胺光化学反应性的边界。尽管不同课题组在aza Paternò-Büchi 反应方面取得了较好进展,但是目前激发亚胺仅限于环状亚胺来避免光异构化。此外,激发态亚胺的其他光化学转化研究,特别是非环状亚胺,仍处于起步阶段。
双自由基介导的氢原子转移和随后的[4+2]环化反应是激发态羰基化合物熟知的一个反应过程,也称为光烯醇化/Diels-Alder(PEDA)反应。然而,尽管有许多尝试,光激发亚胺类似的转化却相对匮乏。事实上,一些开创性的研究表明,在光照射后,亚胺的激发态可以进行氢原子转移反应,但随后的环化反应,由于受到双自由基中间体反应活性和稳定性的影响,较难进行。此外,这些方法都是利用紫外光照射,这通常限制了反应的选择性、官能团耐受性和适用性。在可见光化学中有三个科学难题需要解决:降低的nπ*特性、E/Z异构化的能量耗散和双自由基中间体的反应活性(1,5-DHAT和[4+2]环化中)。同时,发展可见光介导的新方法可以大大扩展这一过程的适用范围和普遍性,并能利用C(sp3)-H和C(sp2)-H键官能化为发散性合成多取代的四氢-1-萘胺骨架提供实用的方法。
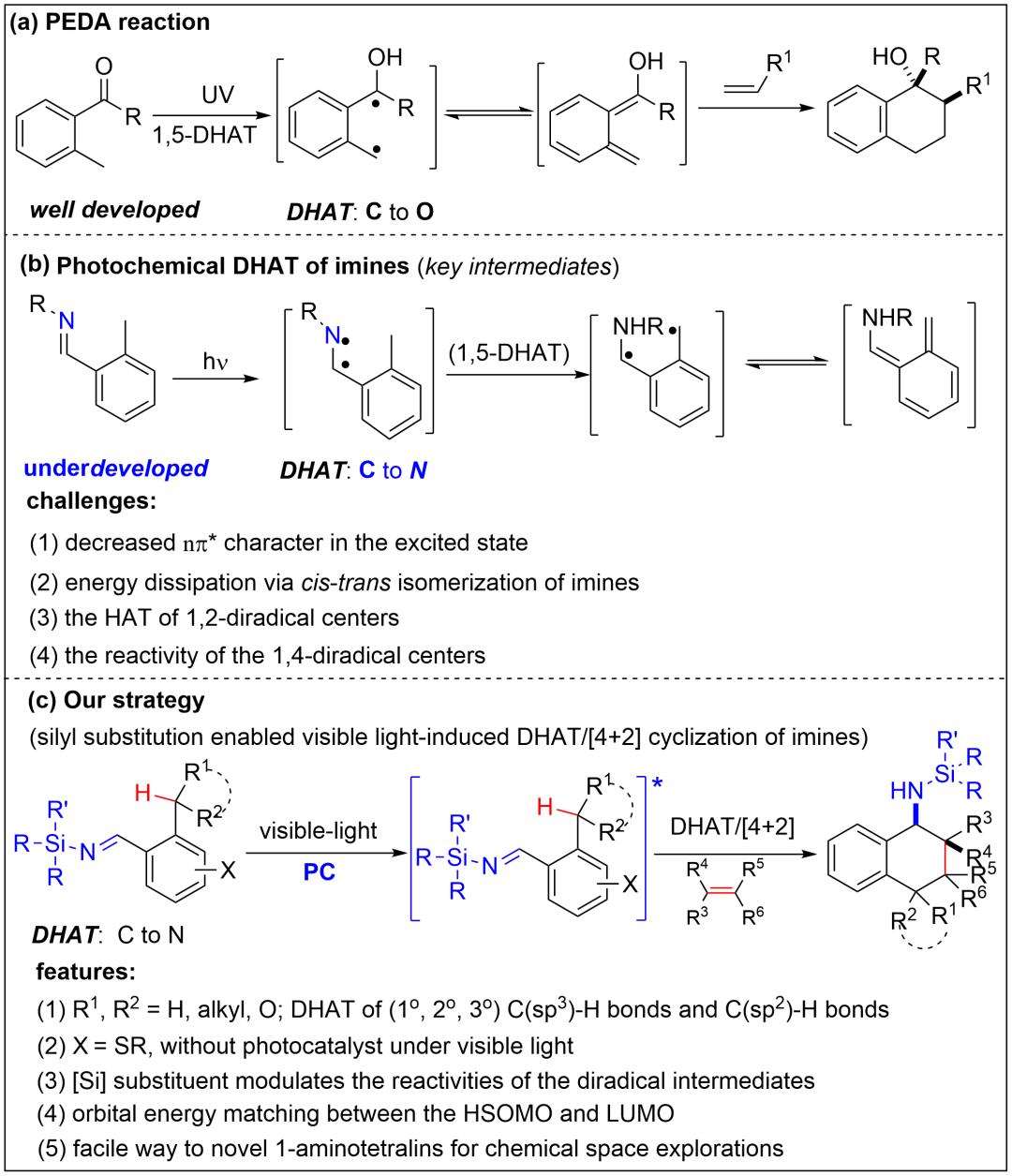
Scheme 1. Schematic reaction pathways (来源:Angew. Chem.)
因此,作者设想通过光敏剂的选择和底物的设计,利用亚胺的三线态的反应活性来实现DHAT/[4+2]环化串联反应。由于硅基取代基可以引起化合物光物理和光化学性质的变化,作者认为这有可能调节双自由基中间体的反应活性,使反应过程中HSOMO和LUMO之间的分子轨道匹配性更好。基于此,作者成功实现了激发的硅烷基芳基亚胺与烯烃发生DHAT/[4+2]环化反应。研究发现,通过一锅法的合成路线,苄基C(sp3)-H键和甲酰基C(sp2)-H键都可以进行选择性转化,从而高效简洁合成四氢-1-萘胺骨架。值得注意的是,含硫取代的邻烷基芳基硅基亚胺可以在没有任何光敏剂的情况下发生这种光化学反应,为生物应用和材料合成提供了新机会。
作者通过对不同亚胺的考察和大量的条件筛选最终获得最优条件:邻甲苯基-N-(三甲基硅烷基)-亚胺8a与丙烯酸乙酯11a,当使用TXT (10 mol%)作为敏化剂在PhCF3中以λmax = 420 nm的光照射,经HCl后处理,可以优秀收率和dr值获得目标产物12a。值得注意的是,通过一锅法,利用2-甲基苯甲醛和LiHMDS在THF中制备亚胺8a,也能有效地进行反应。
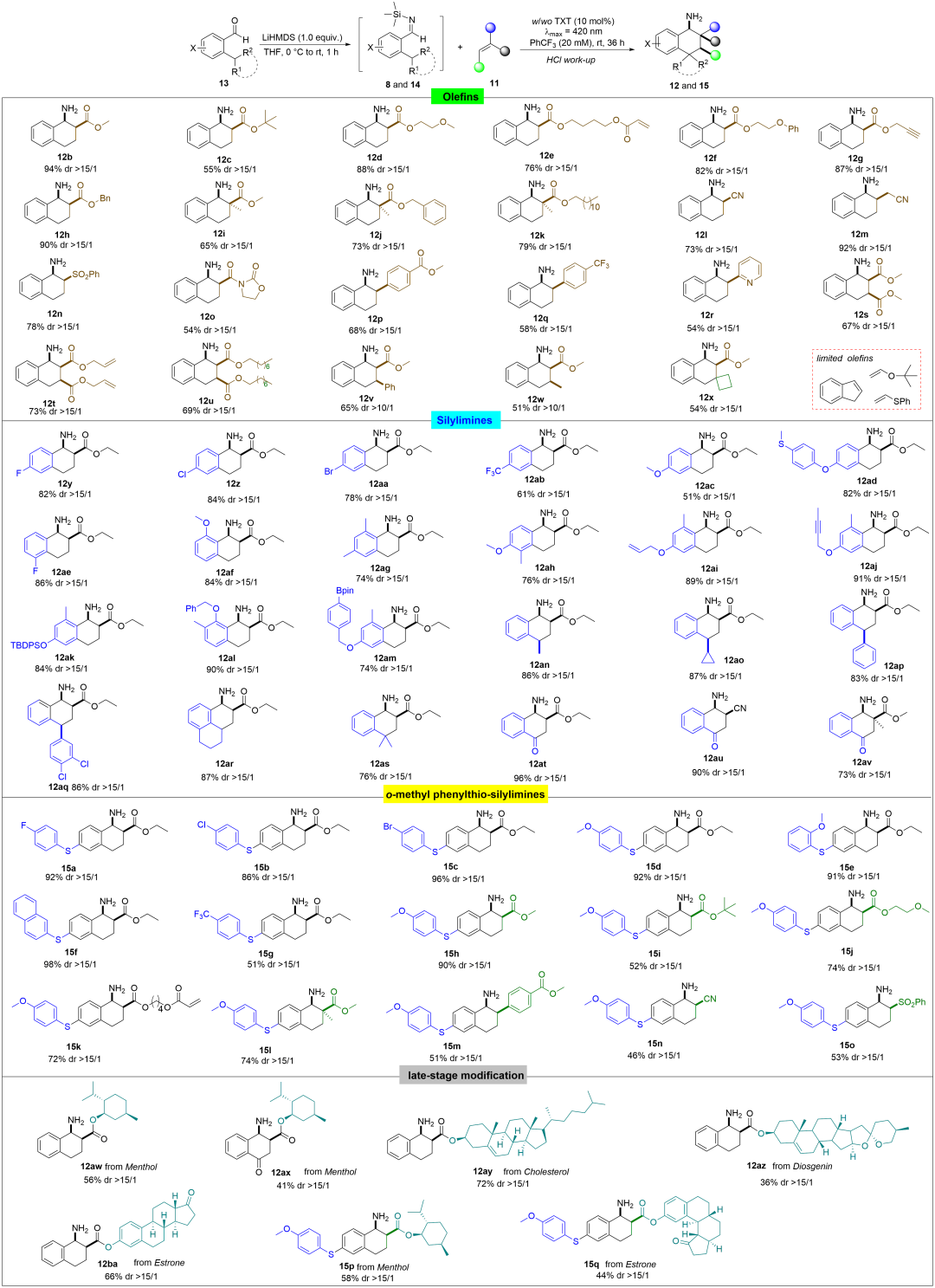
Scheme 2. Substrate scope studies.(来源:Angew. Chem.)
在最优条件下,通过一锅法合成路线研究了各种取代亚胺8与不同烯烃11的DHAT/[4+2] 环加成反应的适用范围。首先,考察了烯烃的底物范围。邻甲苯基-N-(三甲基硅烷基)-亚胺8a和各种单取代、1,1-和1,2-二取代以及三取代烯烃都可以顺利地得到目标产物,并且兼容不同的官能团。然而,富电子烯烃如茚、叔丁基乙烯基醚和乙烯基苯硫醚均不能发生此类反应或aza Paternò-Büchi反应。随后,对邻甲苯基亚胺的苯基上不同的取代基进行考察。发现可以兼容不同的官能团,均以良好至优秀的产率和dr值获得环化产物。此外,对含有苄位二级C(sp3)-H、三级C(sp3)-H和酰基C(sp2)-H碳氢键的亚胺进行了考察,发现也能高效得到为目标产物。最后,为了进一步证明这种光化学方法的实用性,合成了一些复杂的烯烃用于与代表性亚胺8a光化学转化的考察。作者发现含有薄荷醇、雌酮、薯蓣皂苷元和胆固醇的衍生物均适用于该反应,都能以较高产率和dr值得到相应的产物并且兼容复杂的官能团。作者发现使用在没有光催化剂的类似条件,在可见光的照射下,各种含硫取代的硅基亚胺与不同的烯烃底物均可以有效地进行[4+2]环化反应,以较高产率和dr值得到相应的产物。
其次,作者进行了机理实验和DFT计算研究。首先通过紫外可见光光谱实验,发现亚胺的最强吸收波的波长为251 nm。通过时间相关密度泛函理论计算,作者认为这是亚胺的π-π* 吸收。通过荧光淬灭实验,证明亚胺8a可以较好淬灭激发态的光敏剂TXT。同时,氘代标记实验表明8a发生1,5-双自由基氢原子转移反应,证实了氮原子攫取苄位氢原子的假设。分子间竞争(KIE = 3.1)和平行反应(KIE = 3.4)实验都表明H/D底物可能会影响DHAT的量子产率。添加2,5-二甲基六-2,4-二烯,一种高效的三线态淬灭剂,观察到显著的抑制作用,表明反应涉及亚胺的三线态。此外,使用14d作为光敏剂,反应也顺利进行。通过DFT计算发现,与1,2-双自由基中间体的HSOMO和丙烯酸甲酯的LUMO的发生[2+2]环化(△E = 6.44 eV)相比,1,4-双自由基中间体的HSOMO与丙烯酸甲酯的LUMO之间更好的分子轨道匹配,更加支持亚胺[4+2]环化(△E = 5.89 eV)。通过DFT计算表明,三线态的光催化剂首先与底物碳氮双键发生三线态能量转移形成三线态C,N-1,2-双自由基中间体8a-T1。由于化学键的极性性质,氮原子表现出比碳原子(0.52 E)更高的自旋密度(1.05 E),这有助于邻位甲基基团的1,5-DHAT。这一关键步骤通过过渡态TS1-T1发生,具有10.8 kcal/mol的低活化能垒,从而形成1,4-双自由基中间体INT1-T1(△G = -5.8 kcal/mol)。1,4-双自由基中间体INT1-T1与甲基丙烯酸酯反应通过过渡态TS2-T1在放能过程 (△G = -10.8 kcal/mol)中形成中间体INT2-T1。与光环化类似,新的双自由基中间体INT2-T1通过系间窜越和双自由基环化从而得到最终产物。对于硅基取代基在此过程中的作用,作者通过DFT计算认为一个可能的解释是,与亚胺8a-H(△E = 1.15 eV)相比,光敏剂(TXT)的三线态HSOMO与亚胺8a的HSOMO(△E = 0.61 eV)之间的轨道能量匹配更好,可以更有效地进行能量转移。
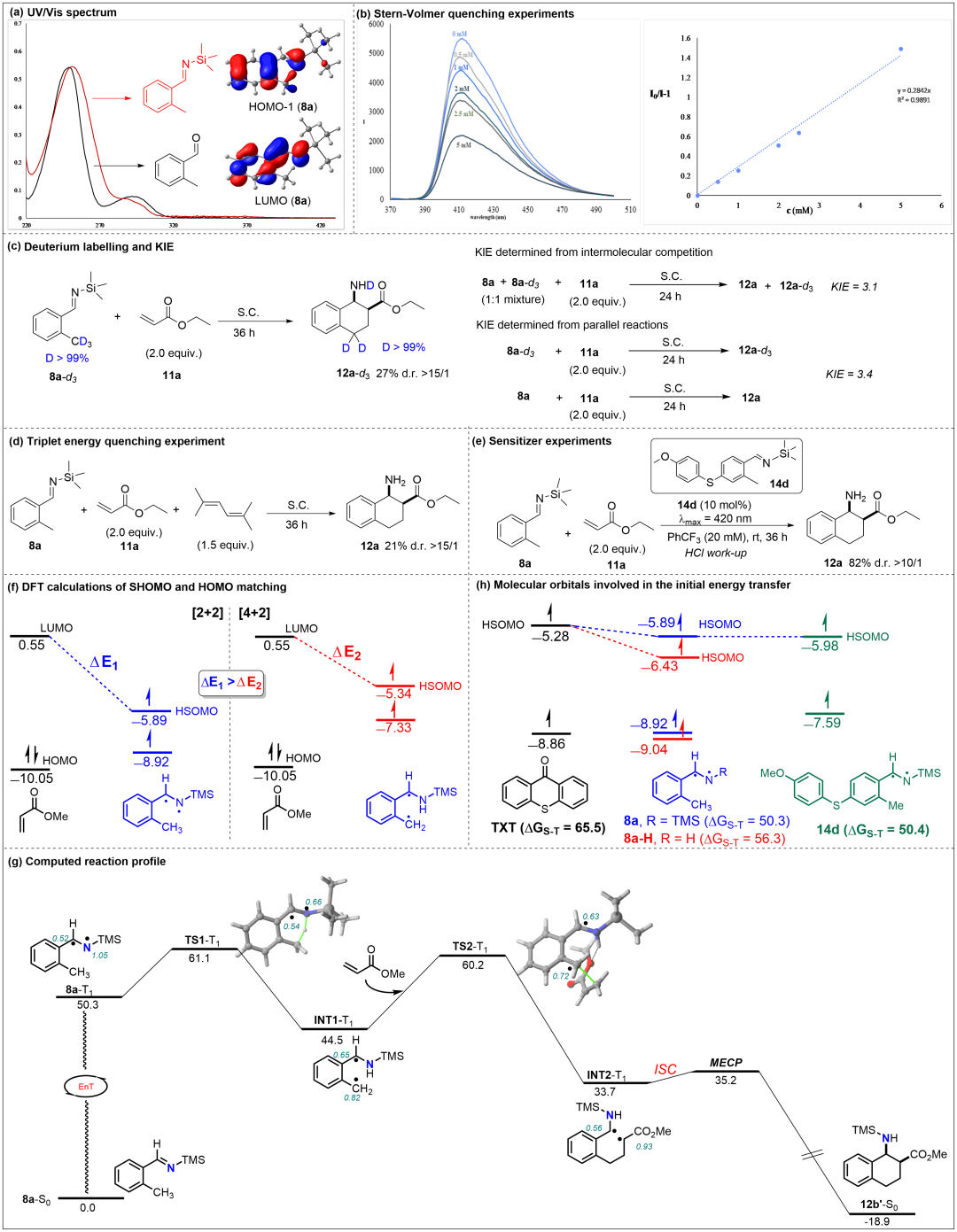
Scheme 3. Mechanistic studies(来源:Angew. Chem.)
考虑到四氢-1-萘胺是存在于有机合成和生物活性分子中的重要骨架,作者选择了一些化学转换来显示发展方法学的应用潜力。首先,从商业易得的邻甲基苯甲醛,利用两次C-H官能团化的策略,可以快速合成舍曲林类似物。同时,作者通过简单的后续化学转化,可以快速实现该类分子的多样性转化,为后续研究奠定了基础。
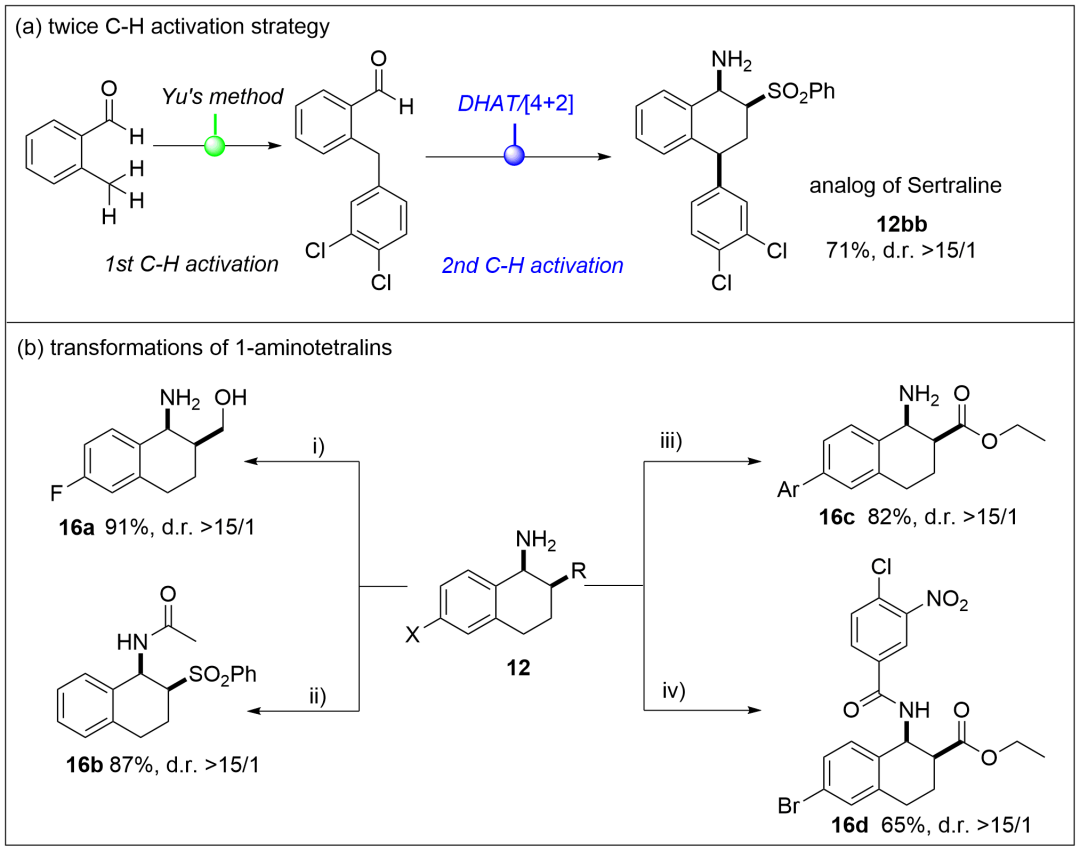
Scheme 4. Applications(来源:Angew. Chem.)
综上,重庆大学药学院熊阳课题组和马德里康普顿斯大学Fernández课题组合作发展了一种可见光介导激发态亚胺与烯烃的[4+2]环化反应。反应中三线态硅基亚胺的氮原子可以攫取一级、二级、三级C(sp3)-H键和C(sp2)-H键的氢原子,形成1,4-双自由基。该1,4-双自由基可以被烯烃有效捕获从而发生[4+2]环化反应。值得注意的是,硫取代的芳基硅基亚胺可以在可见光照射下,无需任何添加剂进行该类反应。氮原子上的硅基取代基对反应的成功至关重要,它能够有效的实现能量转移,从而形成关键的C,N-双自由基;同时,前沿轨道能量匹配有利于后续1,4-双自由基和烯烃[4+2]环化反应。硅基取代基的独特作用不仅为控制激发态亚胺的反应活性提供新方法,也为光促C-H键官能化反应带来新机遇。
论文的第一作者是硕士研究生刘倩。研究工作得到国家自然科学基金委员会,中央高校基本科研业务费、重庆市自然科学基金,重庆大学启动基金的资助。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





