山东大学于松杰课题组Org. Lett.:光催化偕二氟烯烃氧化活化引发[2π+2σ]环加成合成偕二氟双环[2.1.1]己烷
在药物化学中,双环3D结构已经被证明是苯环的有效生物电子等排体,使用双环3D结构替代候选药物分子中的苯环通常可以改善药物的药代动力学性质,同时保留生物活性。众所周知,将氟原子引入药物分子能够显著改变药物的多种药代动力学特性。因此构建含氟的sp3杂化双环3D结构骨架是有重要意义的研究话题。目前仅有少量通过二氟卡宾插入双环[1.1.0]丁烷(BCB)合成二氟双环[1.1.1]戊烷(FBCP)的研究报道,而含氟双环[2.1.1]己烷(FBCH)的合成研究相对欠缺。
近两年,BCB作为构建多种双环3D骨架的合成子成为了有机合成学术界的热门研究话题。以BCB为原料构建双环化合物的反应模式目前包括将π键经能量转移(EnT)活化为双自由基后发生[2π+2σ]环化,以及BCB张力σ键活化(主要类型包括经能量转移断键为双自由基,经单电子还原为自由基阴离子,经单电子氧化为自由基阳离子以及Lewis酸催化的离子型反应)后参与的多种形式环化反应(图1b)。基于这些认识,通过BCB与偕二氟烯烃反应来合成偕二氟双环己烷(FBCH)这一思路似乎直截了当且顺理成章。然而,一般的偕二氟烯烃由于氟原子的引入,得到了一个较为“硬”的二氟碳反应位点,现有的各种反应模式下均无法成功得到环化产物,这是合成含氟双环化合物的难点(图1c,上)。
近期,山东大学于松杰课题组通过设计筛选偕二氟烯烃,实现了通过偕二氟烯烃的单电子氧化活化引发的与BCB的[2π+2σ]环化反应,成功构建了一系列独特的偕二氟双环[2.1.1]己烷(FBCHs)化合物,并且带有丰富的可后期修饰衍生的反应位点(图1c,下)。
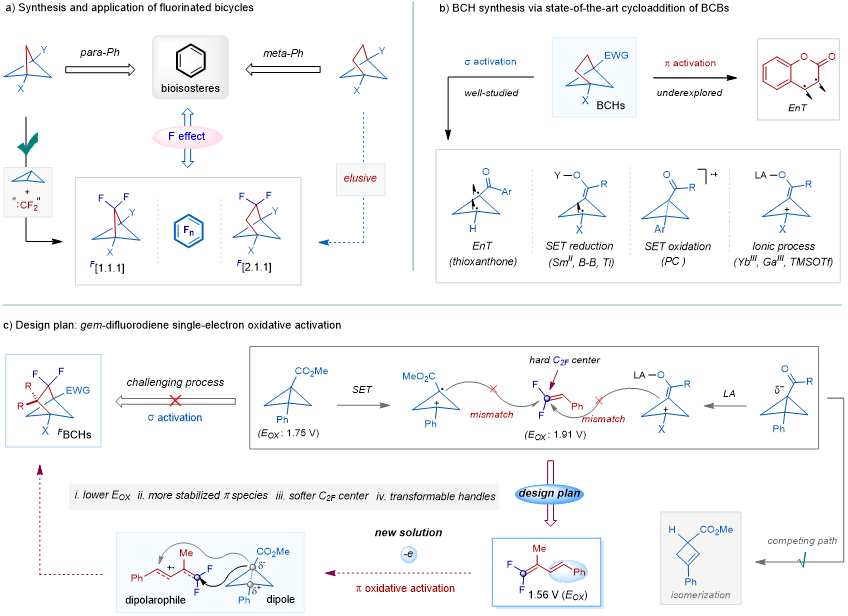
图1. 研究设计思路(来源:Org. Lett.)
一般的含氟烯烃,如偕二氟苯乙烯,拥有较高的氧化电势(EOX = 1.91 V),远高于常见的BCB化合物,在光氧化条件下尝试反应时往往会导致BCB自身发生二聚反应。增大烯烃的π体系明显能够使其更易给出电子,降低其氧化电势,但随之而来的区域选择性问题同样十分棘手。事实发现,共轭偕二氟二烯烃的2号位存在取代基时,能够显著降低其氧化电势,在光氧化条件下,能高效控制反应的区域选择性,基本完全得到偕二氟烯烃1,2-加成的FBCH产物。经条件筛选,模板反应BCB化合物1在1,2-二氯乙烷溶剂中,以2 mol%的吖啶光敏剂PC1催化,455 nm蓝光照射下与3当量偕二氟二烯烃2反应,能够以65%的分离收率得到目标FBCH化合物3。
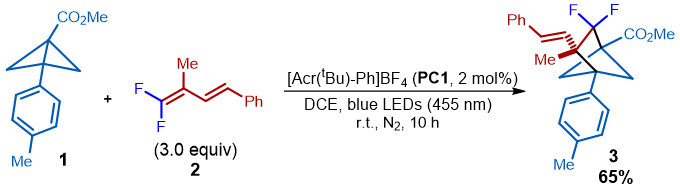
图2. 模板反应(来源:Org. Lett.)
在该最佳条件下,多种不同芳基取代的BCB底物都能够以较好的收率获得FBCH产物,部分吸电子取代基导致收率有所下降,带有不同酯基的BCB和酮基的BCB同样能适用于该反应条件。对于共轭偕二氟二烯底物,各种取代的芳基均能够适用,当2号位的取代基为环丙基、环己基、苯基以及其他更为复杂结构时都能得到良好收率的对应目标产物(35–41)。共轭偕二氟三烯则能以36%的收率得到FBCH产物(42)。当缺失共轭的苯环时,反应的产率则明显降低,仅以17%的收率得到43。作为对比,当偕二氟二烯烃的2号位没有取代基时,仅能以21%的产率得到FBCH产物45,而3,4-加成的BCH产物则达到44%的产率,该区域异构产物的生成可能经历了不同的反应路径。
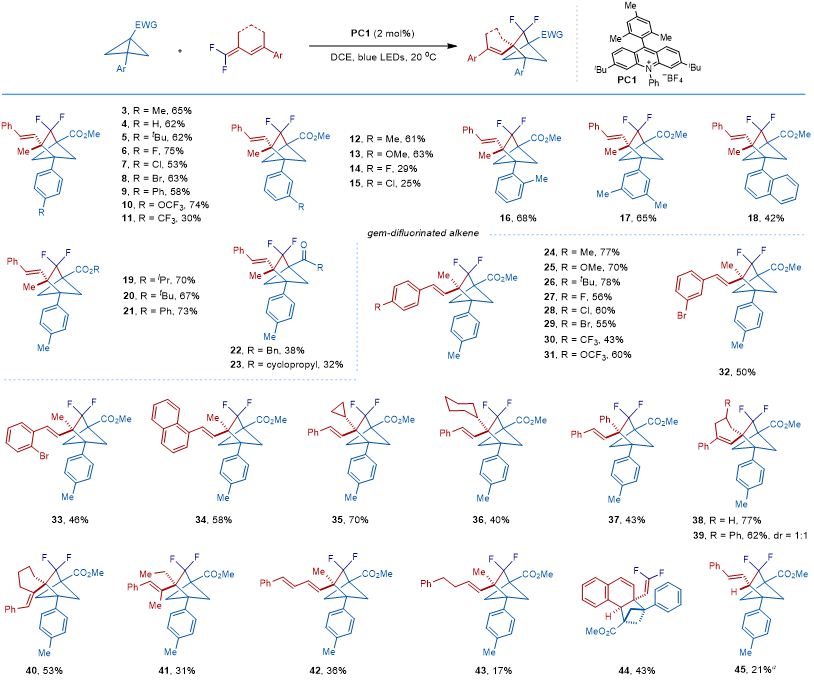
图3. 反应的底物拓展(来源:Org. Lett.)
该方法获得的产物能够应用于各种转化反应(图4)。产物中的酯基水解为羧酸后,可以通过常规方法胺化(47),碘化(48),转化为weinreb酰胺(49),转化为氧化还原酯(50),以及与复杂化合物上的羟基酯化(51)。酯基还可以直接用LiAlH4还原为醇(53)。偕二氟烯烃底物中的双键可以通过钯碳加氢还原为单键(52),也可氧化为环氧化合物(54),也能够直接氧化切断得到对应的醛(55)。
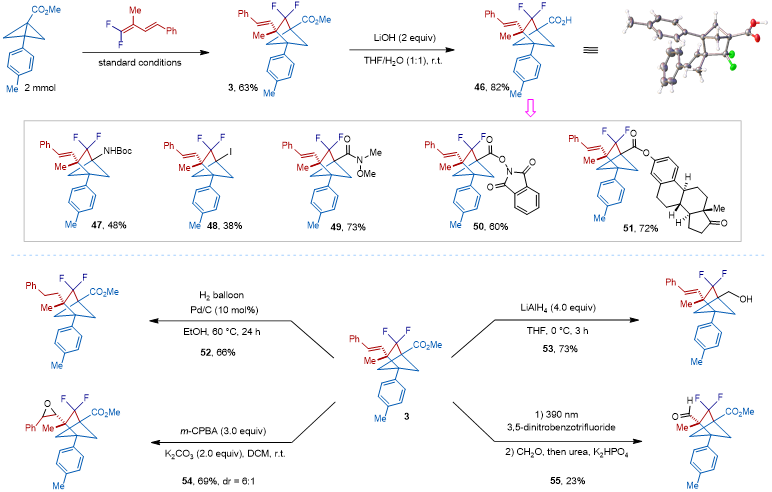
图4. 产物的转化(来源:Org. Lett.)
为了更深入的了解反应,作者进行了一系列测试。紫外-可见光吸收光谱结果表明仅有光敏剂在反应条件的455 nm光源下有吸收,底物并不能直接被光源活化(图5d)。通过循环伏安法测得了不同底物的氧化电势,结果显示2号位甲基取代的偕二氟二烯的氧化电势显著低于无取代基的偕二氟二烯,而BCB的氧化电势则与无取代的偕二氟二烯接近,这表明偕二氟烯烃和BCB都可能在反应体系中发生单电子氧化,这会导致反应经历不同的路径,指向不同区域选择性的环化产物。荧光淬灭实验的结果证实使用的吖啶光敏剂能够被BCB和偕二氟烯烃淬灭,进一步证实多反应路径的理论可行性。Hammett实验表明偕二氟二烯上的取代基对反应速率呈现负的线性影响(ρ=-0.7),这说明偕二氟二烯上在反应过程中存在正电荷的累积。
此外,作者还进行了精彩详细的理论计算,限于篇幅此处不展开讨论,大家可查阅SI 3.6节了解相关内容。
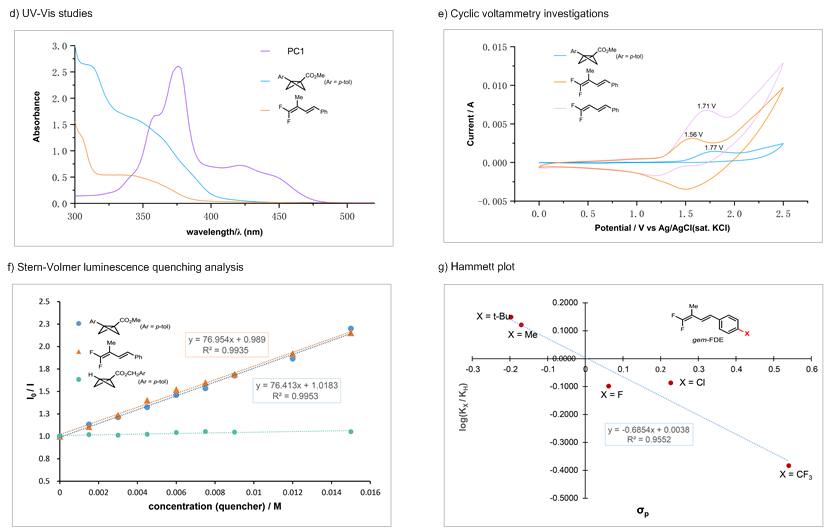
图5. 部分测试结果(来源:Org. Lett.)
基于以上结果,作者提出了合理的反应历程。偕二氟二烯底物首先与光敏剂发生单电子转移,被氧化为自由基阳离子物种,随后亲电进攻极化的BCB张力键,得到自由基阳离子中间体II(π-stabilized distonic radical cation)。芳基对正电荷的稳定作用促进了该步骤的发生,之后正电荷经单电子转移被还原为自由基,经过自由基-自由基偶联得到最终的FBCH产物。

图6. 提出的反应历程(来源:Org. Lett.)
总结
该论文提供了一种通用的构建偕二氟双环[2.1.1]己烷(FBCH)新骨架的策略,并带有多个方便的转化位点,通过一系列转化实验验证了该方法合成上的适用性;机理研究表明,光敏剂单电子氧化偕二氟二烯生成了关键的自由基阳离子物种,进而通过对极化的BCB张力键的亲电进攻引发了环化反应。这种新的反应模式和新构建的FBCH骨架有望在药物开发及相关领域有所应用。
该成果近期发表于Org. Lett.,山东大学为第一单位,山东大学博士研究生付振达为第一作者,李晓溪副研员,李兴伟教授和于松杰教授为通讯作者。感谢国家重点研发计划、国家自然科学基金委、山东省和山东大学的经费支持。
论文信息
gem-Difluorobicyclo[2.1.1]hexanes via Photochemical [2π+2σ] Cycloaddition Initiated by Oxidative Activation of gem-Difluorodienes.
Zhenda Fu, Jianzheng Cheng, Xiao-Xi Li,* Xingwei Li,* and Songjie Yu*
Org. Lett. 2024, 26, 9961−9966.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





