哈佛Daniel G. Nocera JACS:单金属铜氧配合物可见光催化氧化烷烃
导读
烷烃氧化生成高附加值液体产品是可持续化学的重要目标。自然界中,在温和条件下,加氧酶的单金属和多金属铜中心可以完成烷烃的羟基化反应。作为生物学C-H键羟基化试剂,CuII-O·促使人们在均相和非均相材料中模拟这种中间体。据报道,CuII-O·中间体可以活化惰性C-H键。传统方法制备单核活性铜物种通常涉及到铜与H2O2和PhIO等活性氧化剂的反应。这些铜中间体反应性极强,需要低温才能观察到。光化学和电化学方法也可以获得铜基氧化物中间体,从而替代热生成策略。光照射铜配合物4天得到一种具备C-H氧化能力的铜中间体(Figure 1A)。C-H裂解是反应的决速步骤,这可能是铜氧部分相对稳定的结果。基于此,美国哈佛大学(Harvard University) Daniel G. Nocera课题组研究了Cu-1至Cu-4这几种三吡唑基硼酸酯(TpR)配合物的C-H光氧化催活性(Figure1B)。所有配合物都能在室温下光氧化轻质烷烃,产率在16-77%之间,其中性能最好的Cu-3配合物可以将甲烷光氧化为甲醇。相关成果发表于J. Am. Chem. Soc. 期刊。
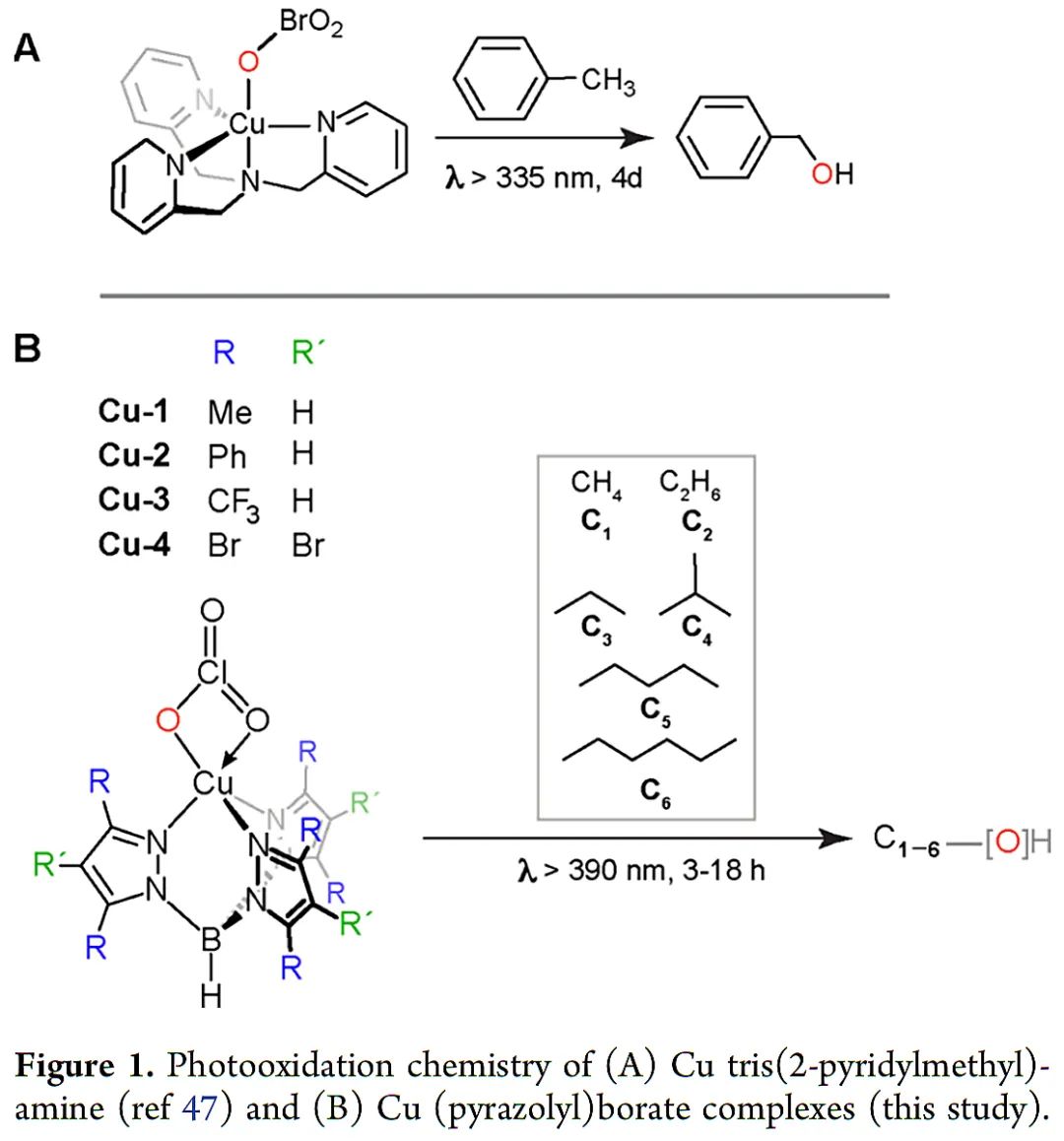
(Figure 1,来源:J. Am. Chem. Soc.)
成果
Cu-1至Cu-4可以通过相应的三(吡唑基)硼酸盐CuBr2配合物与AgClO3之间的盐复分解反应制备。配合物的X射线单晶衍射结果表明:CuII位点采用伪四方锥配位,氯酸盐κ2连接。EPR谱证明了结构中有一个轴对称的CuII。TpR配体明显改变了CuII/CuI的氧化还原电位。作者利用配合物Cu-3研究乙烷氧化的反应曲线(Figure 2A),5小时内反应产率增加到75%,随后增加到77%。所有配合物均可实现乙烷到乙醇和乙醛的转化。与Cu-3相比,相似配位环境的Cu-1配合物乙烷氧化的产率降低(Figure 2B),表明CH3与CF3的取代基电子性质不同会引起反应性差异。作者推测TpR骨架上带有吸电子基团的配合物在Cu中心产生较弱的Cu-O键和较高的氧化能力,从而提高了整体转化率。配合物Cu-2表现出与Cu-1相似的光氧化还原活性(18%),Cu-4的产率中等。
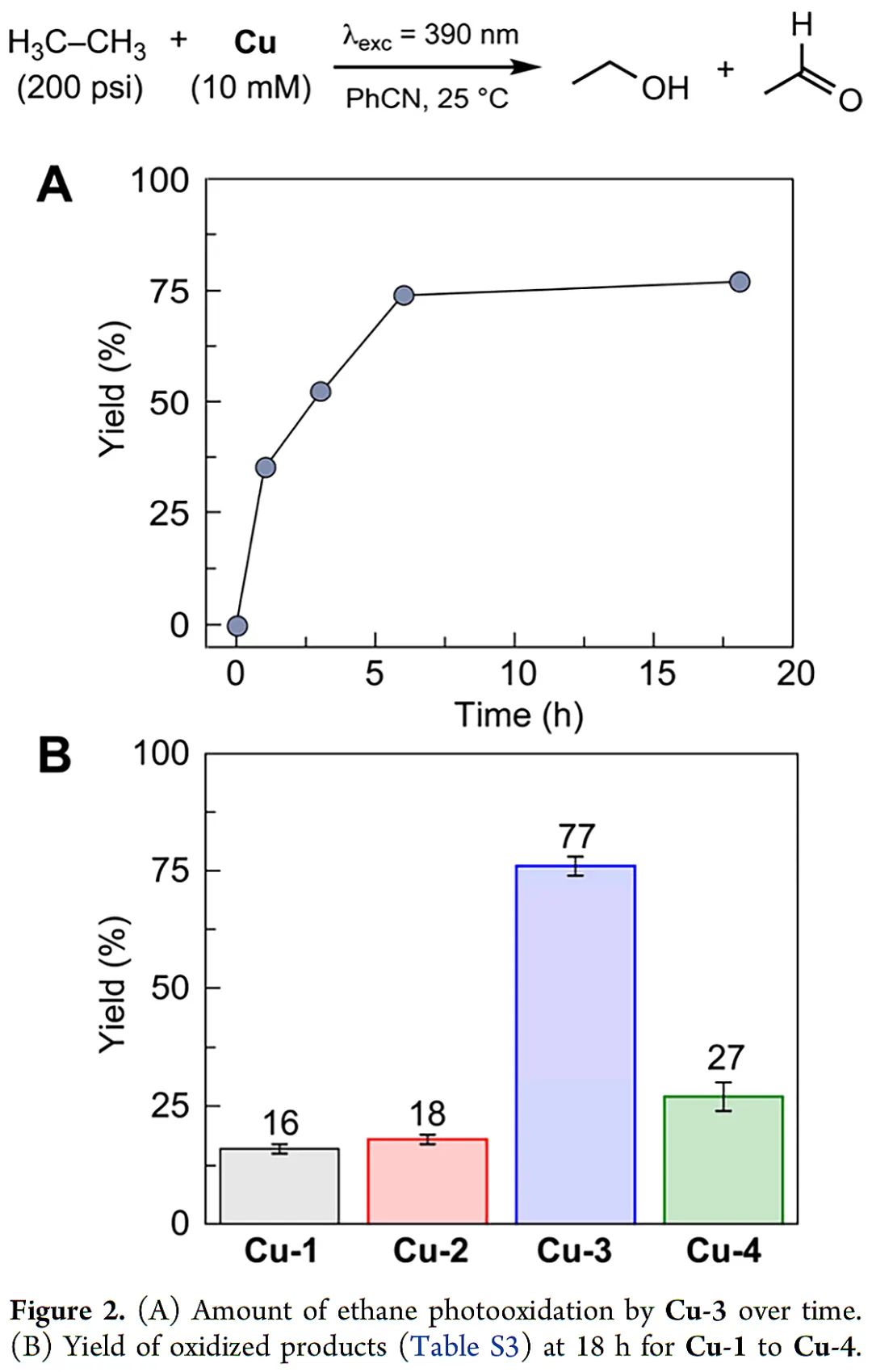
(Figure 2,来源:J. Am. Chem. Soc.)
乙烷中惰性C-H键的活化能力鼓励作者尝试研究其他以丙烷和异丁烷2°和3°C-H键为目标的轻质烷烃。考虑到有机溶剂中这些气体的溶解度较大,反应使用30 psi的压力,时间缩短到3小时。Figure 3A展示了每种配合物中丙烷1° 和2° C-H位点的氧化选择性。氧化性更强的Cu-3配合物导致1° C-H位点的氧化作用比2° C-H位点更强。1° C-H位置的氧化产率随着Cu(II)氧化还原电位的增加而线性增加。异丁烷的1° 与3° C-H键的氧化也有类似的趋势(Figure 3B)。活化1° C-H键的区域选择性表现出明显地偏好,表明C-H活化受热力学与动力学控制。随后,作者使用液态烷烃进行了进一步的实验。390nm激发下,光氧化己烷生成烯烃和酮,戊烷也是类似的结果。
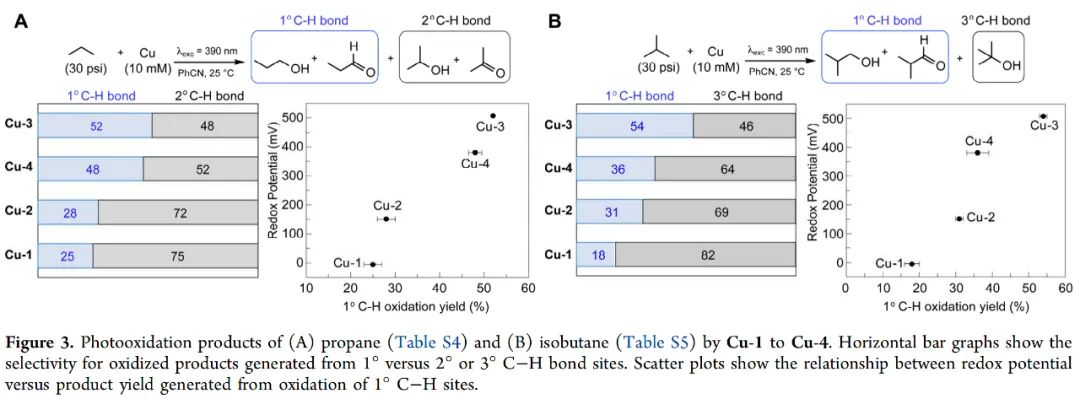
(Figure 3,来源:J. Am. Chem. Soc.)
接下来,作者对烷烃光氧化机理进行了推测(Figure 4),该机理类似于H2O2氧化TpCuI中心生成CuII-O·的机制。光生CuII-O·从烷烃(RH)中攫取氢原子(HAA),生成CuII-OH和R·。在甲苯和甲苯-d8存在下照射铜配合物,动力学同位素效应值从3.6到4.3,表明过渡态中显著的C-H裂解。回弹机理将OH基团转移回烷基,产生ROH和TpRCu。或者,TpCuII(OH)中心的氧上具有足够的自由基性质,促进HAA进程生成烯烃。
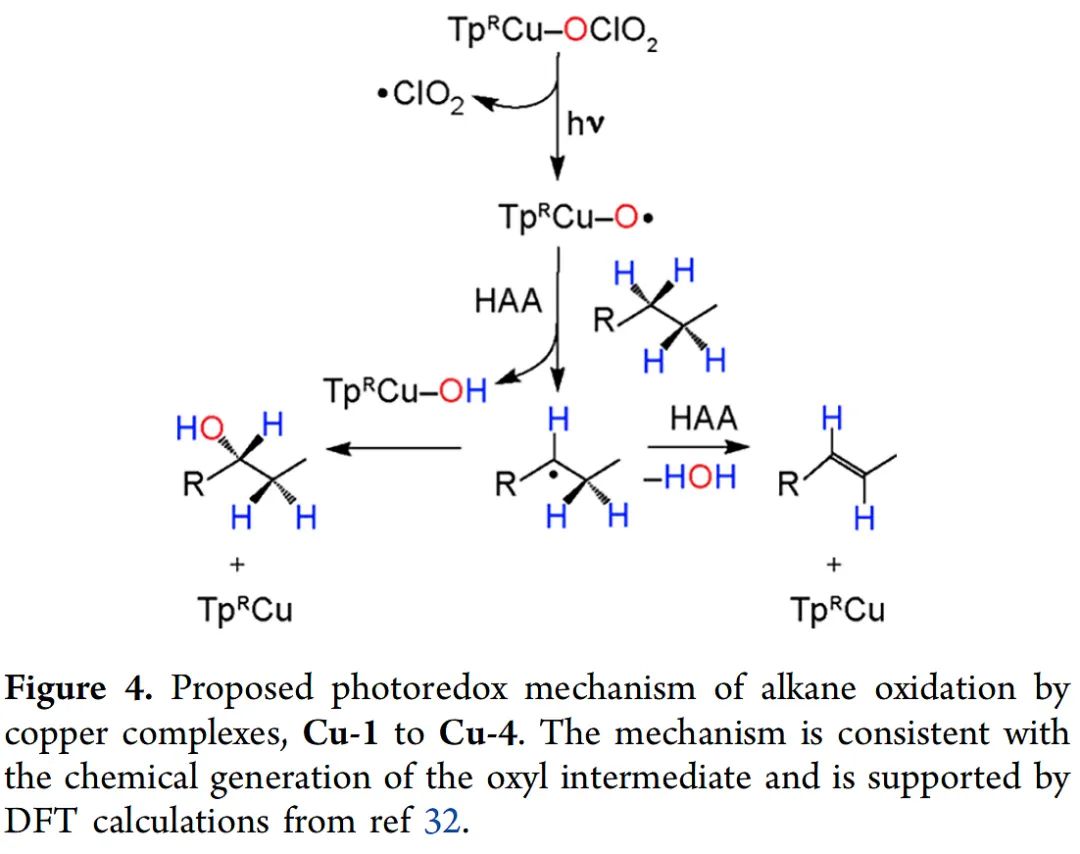
(Figure 4,来源:J. Am. Chem. Soc.)
100 K下用405 nm光照射Cu-4单晶,单晶结构的变化支持ClO2光剥离产生CuII-O·这一猜测。暗态结构和光诱导结构的比较表明,配合物的光解导致ClO2的消除和Cu-O片段的形成(Figure 5)。光解结构展示了弯曲和拉长的Cu1-O2处的末端氧。
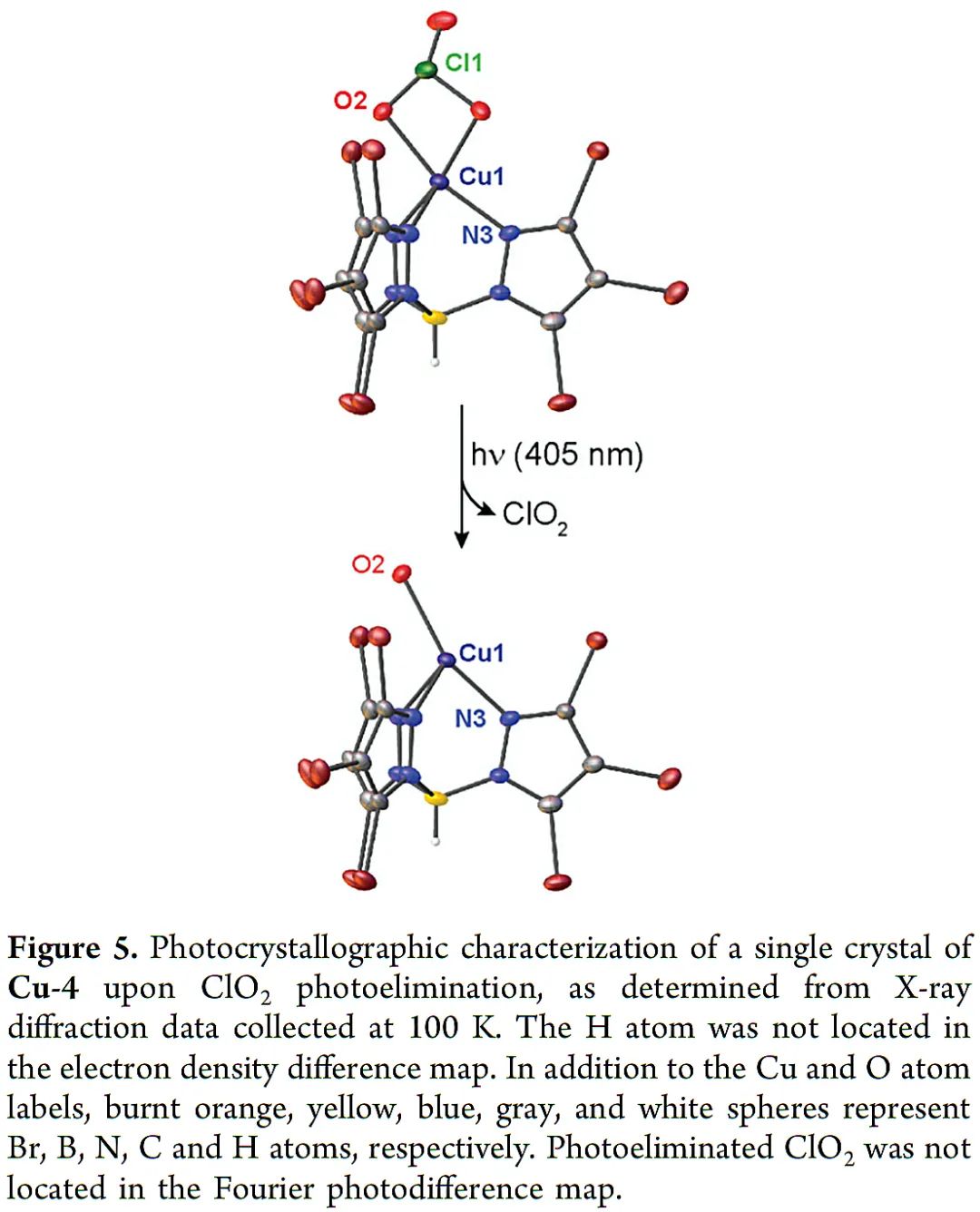
(Figure 5,来源:J. Am. Chem. Soc.)
在轻质烷烃中,甲烷具有最难活化的1° C-H键(BDE=105 kcal/mol)。在与其他轻质烷烃类似的条件下,作者利用性能最佳的Cu-3配合物进行了光氧化甲烷实验(Scheme 1)。在25°C下,在200 psi CH4的存在下,在MeCN-d3中的N2下照射10 mM Cu-3 18小时,可以成功生成甲醇,产率为6%。
有氧条件下产生的CuII-O·中间体可以用来启动自由基链途径,从而提高甲烷的氧化产率。事实上,在全氟己烷(PFH)的有氧条件下,甲烷到甲醇的光氧化转化率显著增加。在200 psi CH4存在下,在O2饱和的PFH中照射2mM Cu-2 24小时,可以生成44%的甲醇。光子通量增加约×2使得Cu-2生成MeOH收率提高至78%,而Cu-3的MeOH收率为38%,这证实了前者的选择性因MeOH的过度氧化减少而提高。甲醇收率的增加与甲烷H·撅取引发的自由基链机制一致。在过量氧气的情况下,Me·可以与O2生成MeOO·,MeOO·歧化为O2和MeO·,然后与另一当量的CH4反应生成MeOH和Me·。在室温下,可见光从CH4中产生MeOH的能力突显了光氧化还原方法产生反应性中间体的好处,这些中间体可以活化惰性的C-H底物。
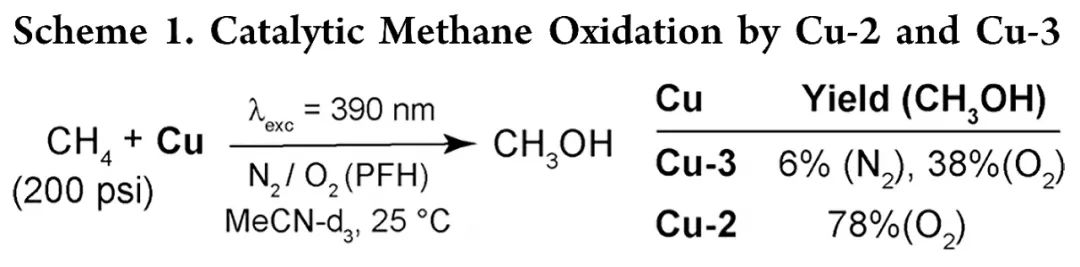
(Scheme 1,来源:J. Am. Chem. Soc.)
总结
总而言之,作者证实了温和条件下光化学实现烷烃氧化的实用性。铜的伪四方锥配体场允许烷烃在室温下使用氯酸盐作为主要氧化剂进行光氧化。可见光,包括1个太阳光照射,诱导配体与金属之间的电荷转移,可能会产生强氧化性的铜氧基中间体。对于液态烷烃,光氧化还原得到的结果与过氧化氢生成铜氧化物中间体时的结果相似。辅助配体场调节铜基氧化物的氧化能力,从而控制底物氧化的水平。
论文信息
Photoredox Oxidation of Alkanes by Monometallic Copper–Oxygen Complexes Using Visible Light Including One Sun Illumination
Daniel L. Nascimento, David Gygi, Matthew C. Drummer, Miguel I. Gonzalez, Shao-Liang Zheng and Daniel G. Nocera*
J. Am. Chem. Soc.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





