川大冯小明/刘小华团队Chem. Sci. : 通过Lewis酸/光氧化还原协同催化实现酮和甘氨酸酯的不对称aldol反应
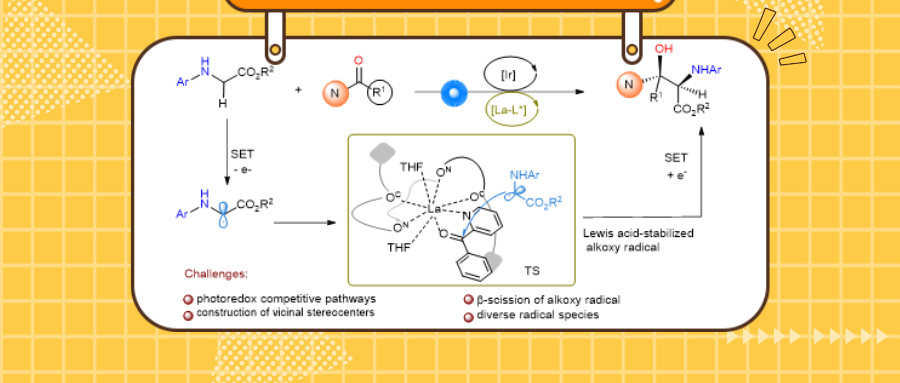
近日,四川大学冯小明/刘小华团队在光催化甘氨酸酯α-C(sp3)–H官能团化构建非天然氨基酸上取得进展,相关成果“Visible-light-driven asymmetric aldol reaction of ketones and glycinates via synergistic Lewis acid/ photoredox catalysis” 以研究论文的形式发表于Chemical Science,四川大学化学学院为第一通讯单位,冯小明教授和刘小华教授为共同通讯作者,博士研究生谭九七为论文第一作者。
非蛋白源 α-氨基酸(αAAs)在设计具有更好生物特性的药用肽和蛋白质方面发挥了至关重要的作用。甘氨酸的 α-C(sp3)-H 官能化是生成一系列非天然手性 α-氨基酸的高效方法。可见光驱动的光化学技术的出现促进了甘氨酸直接官能化的广泛应用。这一方法已被证明是甘氨酸直接进行 α-C(sp3)-H 烷基化和芳基化的有效方法。然而,仅有零星的报道涉及不饱和化合物,如羰基化合物、偶氮化合物或苯丙炔等,它们可以作为甘氨酸 α-C(sp3)-H 官能化的补充方法(Scheme 1a,1b)。但是,甘氨酸酯与酮特别是芳基酮反应构建丝氨酸衍生物仍然存在大的挑战。存在的具体困难如下:(ⅰ) 芳香酮与甘氨酸酯在光氧化还原反应过程中存在氧化淬灭和还原淬灭的竞争过程;(ⅱ) 体系中产生自由基物种过多易发生多种副反应,如自偶联;(ⅲ) 芳基酮自身容易受光激发到达激发态,发生直接的HAT过程;(ⅳ) 经过aldol反应生成的烷氧基自由基容易发生β-裂解;(ⅴ) 构建连续相邻季碳手性中心是具有合成挑战性的。
因此,冯小明/刘小华团队基于此前在光催化酮的不对称转化领域的研究(ACS Catal. 2022, 12, 5136−5144; J. Am. Chem. Soc. 2022, 144, 22140−22149; CCS Chem. 2024)提出Lewis酸/光氧化还原协同催化策略成功克服了上述困难,首次报道一系列β-二芳基-β-羟基-α-氨基酸衍生物的高效、高对映选择性合成。首先通过配体加速效应提高自由基加成反应的速率,尽可能避免副反应;然后La(Ⅲ)/双氮氧配合物在提供优异手性环境的同时能够稳定烷氧基自由基,抑制β-裂解的过程(Scheme 1c)。
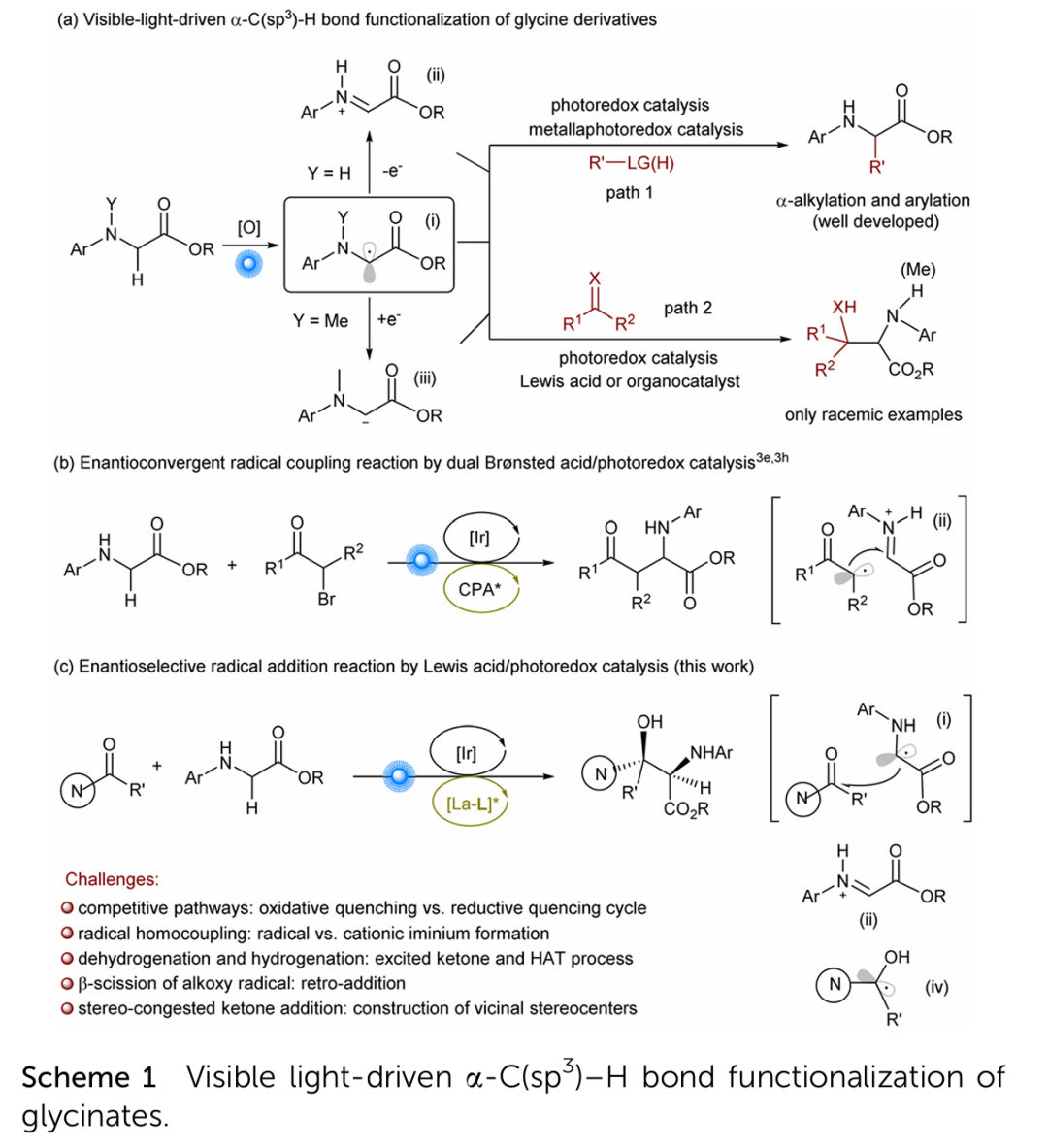
(来源:Chem. Sci. )
首先作者经过大量条件筛选,确定最优反应在-30℃,THF为溶剂,460nm 2W Blue LEDs光照的氮气氛围条件下进行。手性La(OTf)3/L3-RaPr3配合物为Lewis酸催化剂,Ir[dF(CF3)ppy]2(dtbbpy)PF6为光催化剂,DMAP为碱,NaBArF4为添加剂(Table 1)。
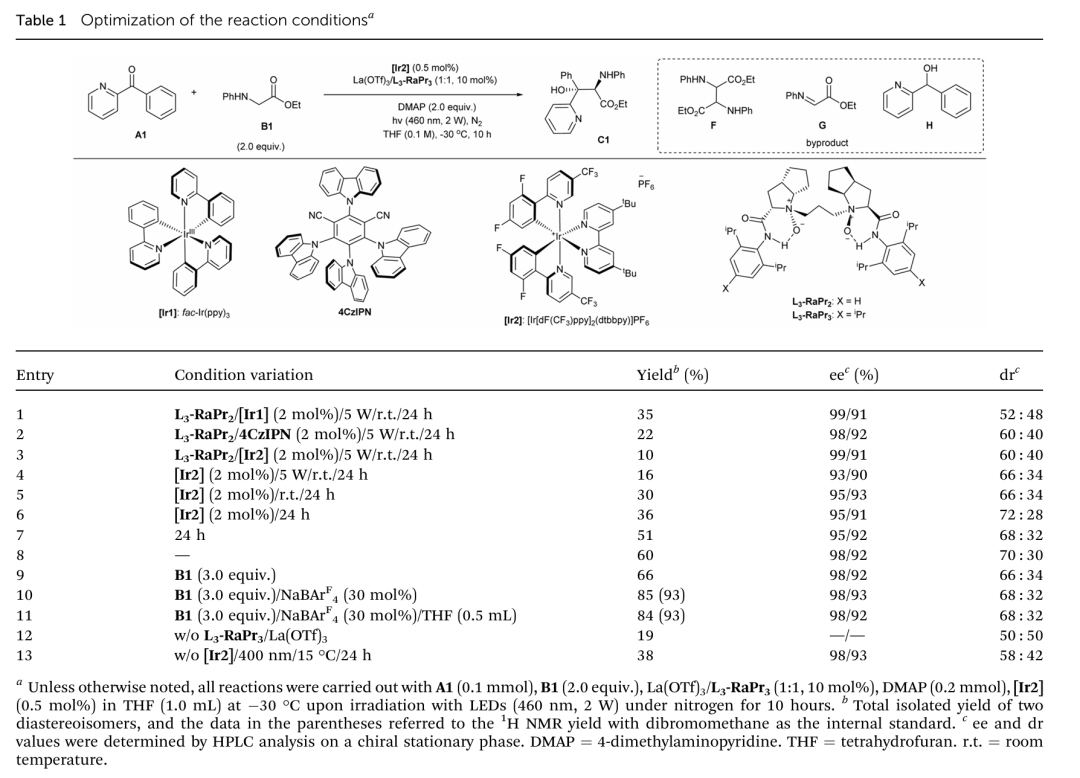
(来源:Chem. Sci. )
在获得上述最佳反应条件后,作者首先对各种甘氨酸酯进行考察,发现不同酯基对反应无明显影响(Scheme 2)。芳基上不同位置取代基均能发生反应,且取代基的电子效应对反应的收率有略微影响并不改变反应的对映选择性。并且各种官能化基团也能很好的发生转化,如氰基、烯基、炔基、酰基、酯基、硼酯基等。除此之外,作者对醇类天然产物进行修饰,同时也能对多肽进行修饰。
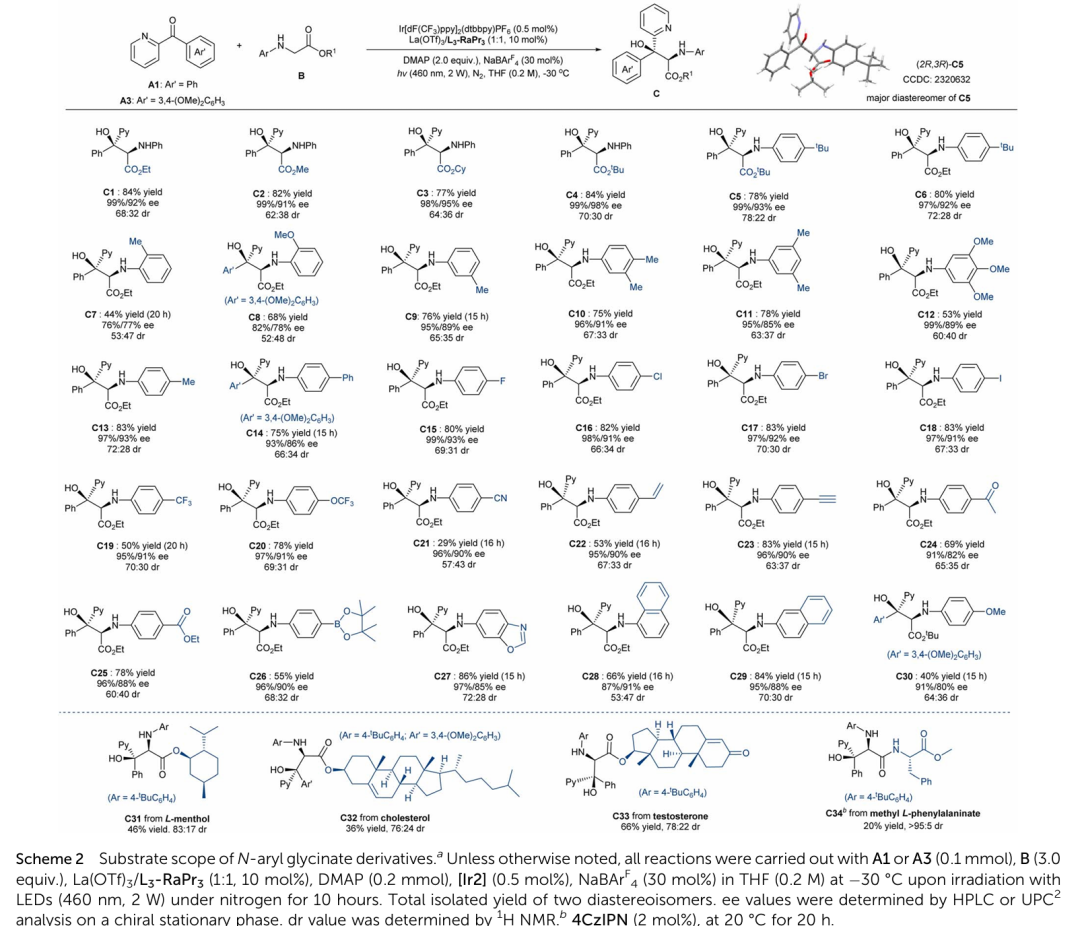
(来源:Chem. Sci. )
随后,作者对氮杂芳基酮和烷基酮的普适性进行了考察(Scheme 3)。不管是苯基还是氮杂芳基上都能兼容各种取代基,此外烷基酮也能很好的转化。令人遗憾的是,苯基C2位以及吡啶基C5位存在取代基,不能转化为目标产物,可能是由于靠近反应位点存在位阻会阻碍两底物的靠近。
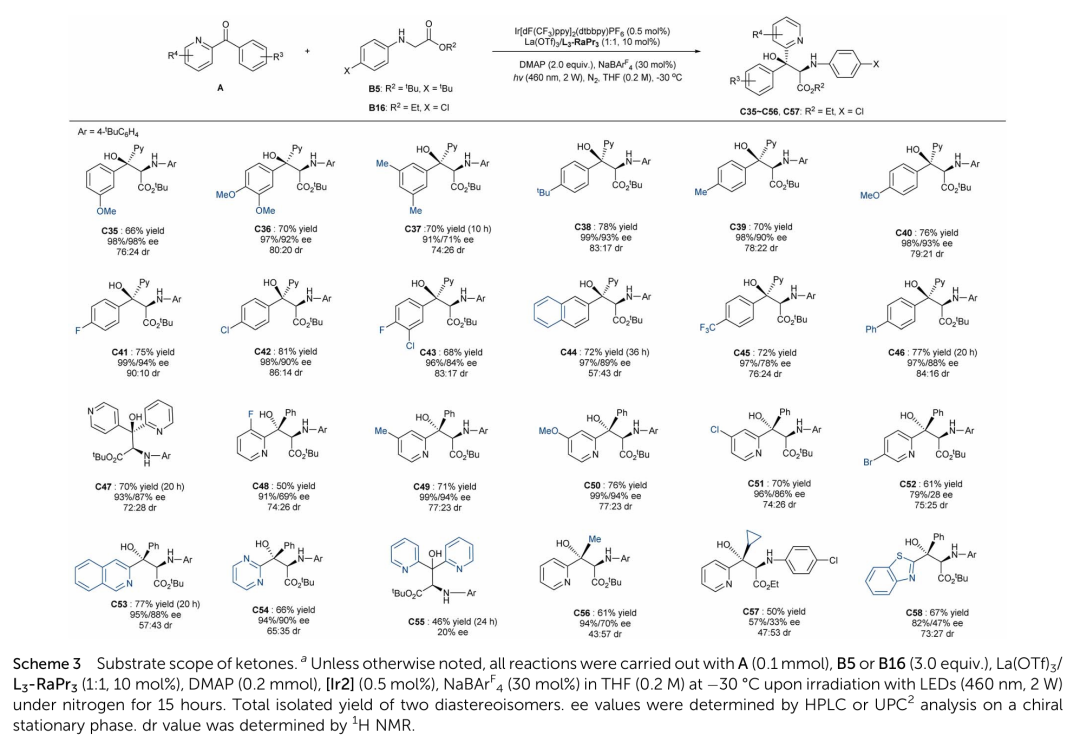
(来源:Chem. Sci. )
为了展现该合成方法的有用性,作者首先进行克级规模放大实验,反应结果都能保持。然后利用DIBAL-H能顺利将酯基还原成羟甲基,高效合成2-氨基-1,3-二醇。同时在三光气的作用下,产物能够顺利转化为恶唑烷酮的衍生物(Scheme 4a)。
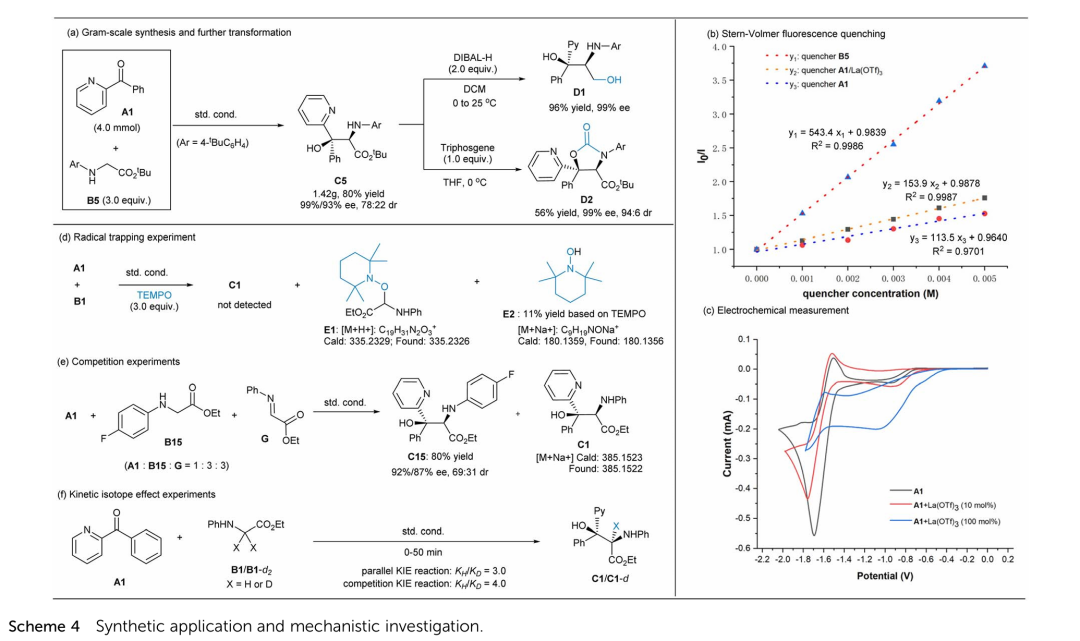
(来源:Chem. Sci. )
为了理解整个反应过程,作者进行一系列机理实验。Stern–Volmer荧光淬灭实验表明激发态光催化剂首先与甘氨酸酯作用。循环伏安法说明Lewis酸与酮配位后能降低其还原电势并且与还原态光催化剂电势相匹配。自由基捕获实验说明存在α-氨基自由基。竞争实验说明酮基自由基存在的可能性,结合自由基捕获实验以及自由基钟实验可以排除酮基自由基占主导的机理。KIE实验揭示了反应的决速步骤是C-H键断裂过程。结合上诉的实验结果,作者推测可能的反应机理为:首先光催化剂受光激发达到激发态,然后单电子氧化甘氨酸酯B1,在DMAP作用下脱去质子生成中间体Ⅰ,紧接着经历path a路径自由基加成到La(OTf)3/L3-RaPr3与酮A1的配合物得到Lewis酸稳定的烷氧基中间体Ⅱ,随后释放手性Lewis酸催化剂再质子化得到相对稳定的烷氧基中间体Ⅲ,最后经过基态Ir(Ⅱ)单电子还原得到产物C1,同时再生Ir(Ⅲ)光催化剂完成整个催化循环(Figure 1a)。为了直观说明该反应优异对映选择性的来源,作者对自由基加成的过渡态进行DFT计算(Figure 1b)。对映选择性控制模型表明酮与中间体Ⅰ发生Re/Re面接触的能垒低于Si/Si面;IGMH弱相互作用揭示了TS-(R,R)过渡态存在弱的π-π相互作用,而TS-(S,S)存在空间位阻排斥作用,最终导致高对映选择性生成R,R构型产物。
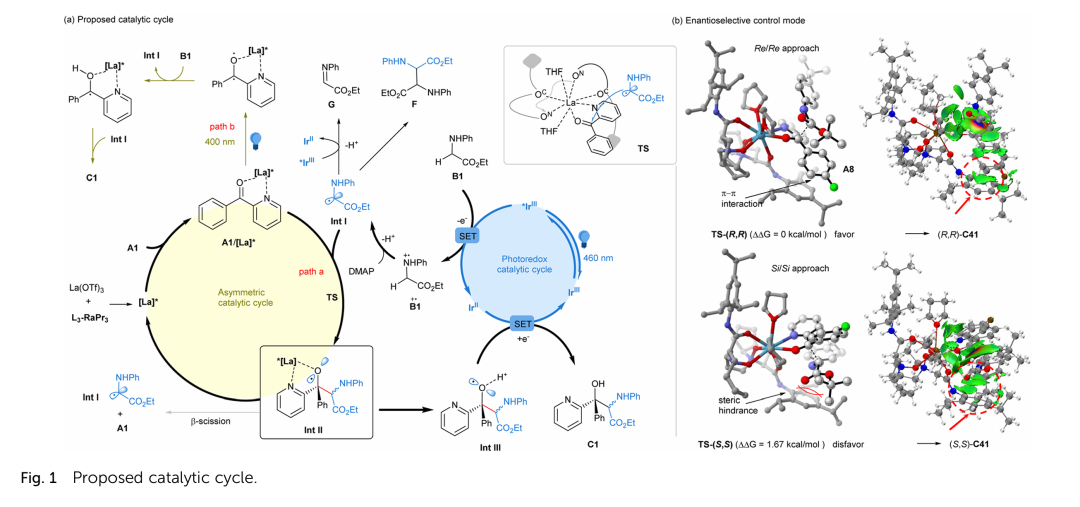
(来源:Chem. Sci. )
综上,冯小明/刘小华团队发展了一种铱光氧化还原催化剂和N,Nʹ-双氮氧手性镧配合物协同催化的方法,实现了甘氨酸酯不对称α-C(sp3)-H羟烷基化,构建一系列β-季碳立体中心丝氨酸衍生物。
该工作得到国家自然科学基金、国家重点研发计划和四川大学的经费资助。同时作者感谢周宇乔博士(四川大学)提供的X-射线单晶衍射分析。
Visible-light-driven asymmetric aldol reaction of ketones and glycinates via synergistic Lewis acid/photoredox catalysis
Jiuqi Tan, Longqing Yang, Hanyu Su, Yuntian Yang, Ziwei Zhong, Xiaoming Feng* and Xiaohua Liu *
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




