陕西师范大学薛东/康腾飞ACS Catal.:有机光敏剂促进镍催化醇与氯代芳烃的脱氧交叉偶联反应

第一作者:熊伟康
通讯作者:薛东,康腾飞
通讯单位:陕西师范大学
开发一种通用且高效的C-C键形成技术一直是有机化学中的核心课题,因为这些技术被广泛应用于复杂分子的构筑和药物分子以及天然产物的合成中。其中,过渡金属催化的芳基或烷基卤化物与有机金属试剂的交叉偶联反应为C-C键的构建提供了一个优异且强大的平台。但大多数情况下,Stille、Negishi和Kumada偶联反应中所用到的有机锡、有机锌和格氏试剂都是有毒且危险的,因此它们需要在交叉偶联反应之前进行预制备。虽然上述一些交叉偶联反应在合成具有药用价值的产品中得到了应用,但Suzuki-Miyaura交叉偶联反应因其使用的硼酸衍生物具有环境友好且易于处理的优点而广受欢迎。然而,这类试剂仍需从相应的芳基溴化物、烯烃或炔烃制备而来,从而增加了这些反应的经济成本。因此,为了避免使用硼酸衍生物或有机金属试剂,一种新的C-C还原交叉偶联反应策略被开发—即通过外加还原剂条件下,过渡金属催化的两个亲电体(如芳基卤化物与烷基卤化物或其他烷基前体)之间的交叉偶联反应,已成为该领域被广泛应用的方法。然而,该类方法仍需要使用当量、甚至过量的金属锰或者锌作为还原剂。基于此,陕西师范大学薛东/康腾飞团队报道了一种使用二芳基酮作为有机光敏剂,镍/光催化醇和氯代芳烃交叉偶联的脱氧芳基化反应。首次报道了二芳基酮诱导苯并噁唑盐和醇的加合物历经HAT过程产生烷基自由基,且使用自然界丰富的醇和工业化偏向的氯代芳烃作为亲电试剂,展现了该催化体系的优异应用前景。相关研究成果发表在ACS Catal.上。
醇是自然界中最丰富的产物之一,也是廉价的化学原料,为有机合成化学提供了普遍且多功能的底物类别。因此,将醇类分子作为直接的C(sp3)偶联伙伴对于有机合成的发展具有重要价值,最近,MacMillan小组利用镍和光氧化还原催化的协同作用,采用了一种巧妙的脱氧策略实现了醇的原位脱氧芳基化。该方案中苯并噁唑鎓盐(BS)能够与醇加合,得到的加合物会在金属Ir(III)光催化剂的诱导下经历单电子转移(SET)和去质子化过程,紧接发生β-断裂以生成烷基自由基(方案1,路径a)。基于此,作者设想了一个全新的脱氧活化过程,烷基自由基可以通过直接的光氧化还原-氢原子转移(HAT)过程获得(方案1,路径b)。近年来,激发态的芳基酮已被证明是一种性能良好的HAT催化剂,同时它们成本低廉、易于获得且结构多样。但使用芳基酮作为HAT光催化剂用于活化醇为C(sp3)偶联伙伴的脱氧偶联研究并未被报道过。同时,氯代芳烃是一类极具吸引力的亲电试剂,与溴代芳烃和碘代芳烃相比,它们成本更低且来源更广泛,通常更受工业化合成的青睐。然而,氯代芳烃的广泛应用始终面临着一个固有的难题,即其结构中高强度的C-Cl键显著降低了其反应活性,进而减缓了其与金属的氧化加成速率。鉴于这些考虑,课题组在此报道了一种在镍和三重态酮催化的协同作用下,醇与氯代芳烃的高效脱氧交叉偶联(方案1,路径b),这为C(sp2)-C(sp3)交叉偶联提供了一个高效且通用的新方案,该方案以良好至高产率得到各种芳基化加合物,并具有出色的官能团耐受性。
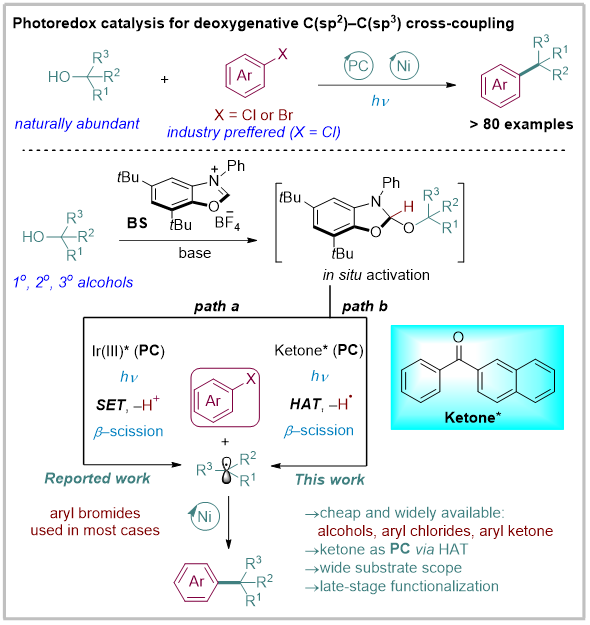
图1. 醇与芳基卤化物的脱氧交叉偶联反应(来源 ACS Catal.)
首先,作者将该方法广泛应用于氯代芳烃的底物扩展中,显著展示了其卓越的官能团兼容性(包括缺电子、富电子及电中性基团)。引人注目的是,杂芳基氯代物也有着高效的反应活性,如,2-、3-、4-位置取代的吡啶、嘧啶、喹啉及异喹啉等杂环化合物的广泛兼容性,为杂环化学及药物化学领域的发展提供全新途径,进一步证明了该方法的强大潜力和广泛应用前景。同时值得注意的是,氯代芳烃中含有丰富数量的天然产物及药物分子,作者将该策略应用于此类分子的后期修饰也得到了不错的成果。这些发现不仅丰富了杂环化合物的合成工具箱,还为设计具有新颖结构和潜在生物活性的药物分子提供了宝贵的资源(图 2)。
紧接着,作者深入探索了醇脱氧反应的底物适用性,该方法成功地应用于广泛范围的醇类底物,包括一级、二级及三级醇,更令人振奋的是,该方法同样适用于糖类分子、氨基醇以及复杂的天然产物或药物活性分子,实现了这些重要化合物的高效脱氧芳基化反应,从而获得了结构新颖且功能丰富的修饰产物。这一系列的发现不仅扩展了醇类化合物转化的边界,还为药物化学、材料科学等领域提供了强有力的合成工具(图 3)。
此外,作者发现尽管吡啶化合物的功能化已经得到了广泛的研究,但将烷基基团引入未取代吡啶的C-4位置仍然是一个公认的挑战。其常见的难题包括官能团耐受性差、较多伴随的副反应以及难以规模化放大。因此作者使用4-氯吡啶盐酸盐作为原料,与各类高价值的官能团保留的醇相偶联,其中包括羟基、烷基基序、酯基及杂环,均能以高收率(82-90%)转化为吡啶对位取代的交叉偶联产物,值得关注的是,手性氨基醇衍生物和药物分子表雄酮也被成功应用。
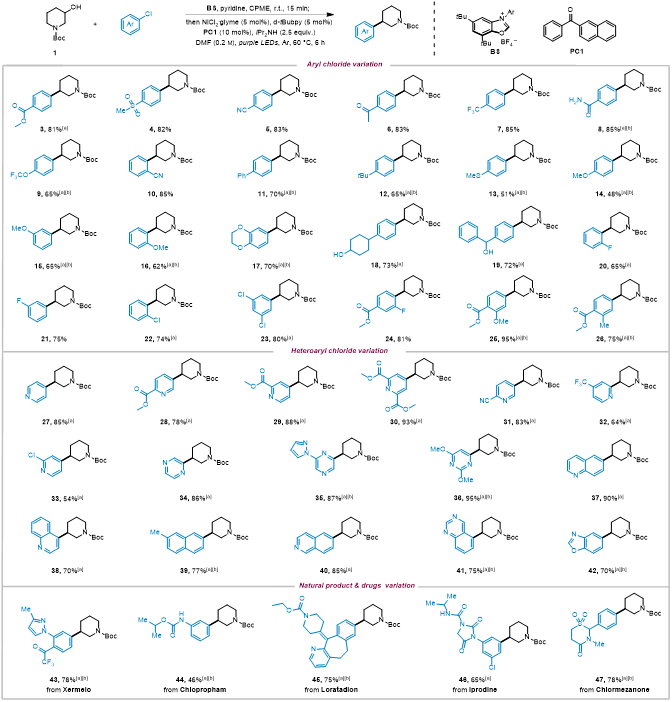
图2. 氯代芳烃的底物范围(来源 ACS Catal.)
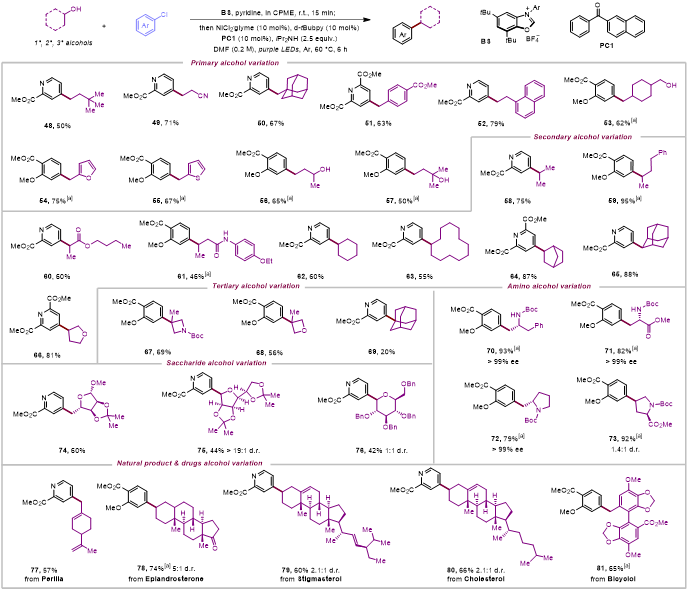
图3. 醇的底物范围(来源 ACS Catal.)
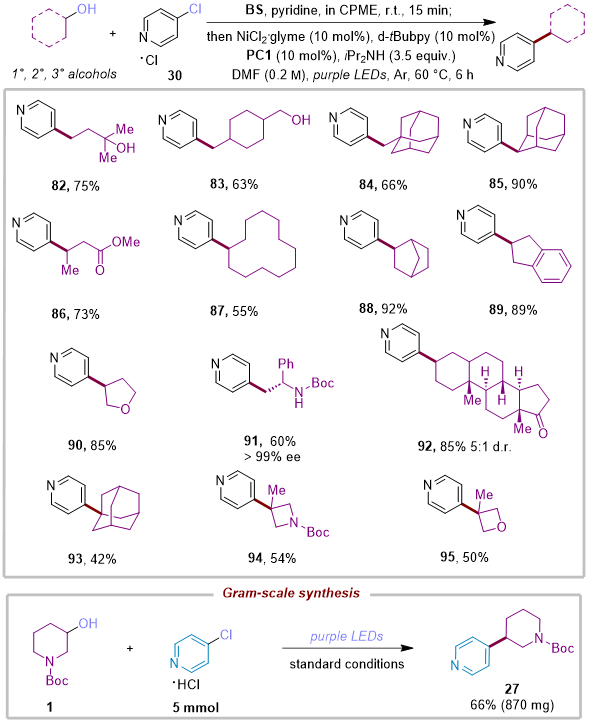
图4. C-4烷基吡啶的合成(来源 ACS Catal.)
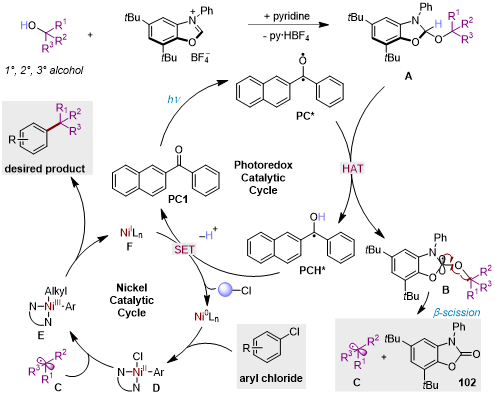
图5. 可能的机理循环(来源 ACS Catal.)
最后,基于已有的控制实验和有机酮引发的HAT的相关文献为基础,作者提出了该脱氧芳基化反应的一个合理机制。苯并噁唑鎓盐和醇的加合物在吡啶作用下脱去质子得到酰胺缩醛A。接着紫光照射激发光催化剂PC1至三重态双自由基PC*,进而与酰胺缩醛A历经一个HAT过程,生成PCH*自由基和瞬态碳自由基中间体B,B迅速发生β-断裂得到游离的烷基自由基C和苯并噁唑烷酮102。同时,在镍催化循环中,Ni(II)催化剂前体与活化的光催化剂经历两个连续的SET过程(PCH*(在乙腈中,E1/2red (Ph2CO) = −2.20 V vs Ag/AgNO3)和Ni(I)(在N,N-二甲基甲酰胺中,[Ni(I)/Ni(0)] ≈ −1.13 V vs Ag/AgNO3)生成Ni(0)物种,Ni(0)物种与氯代芳烃进行氧化加成得到芳基Ni(II)物种D。接着捕获脱氧烷基自由基生成关键的Ni(III)物种E。最后,Ni(III)物种E发生热力学驱动的还原消除,生成脱氧芳基化产物及Ni(I)中间体F,从而完成光敏剂/镍催化的双循环。
综上所述,作者开发了一个新颖的构筑C(sp2)-C(sp3)键的平台,利用镍·联吡啶络合物和二芳基酮作为协同催化剂,采用自然界丰富的醇和工业上首选的氯代芳烃作为亲电偶联伙伴。在此平台中,二芳基酮作为一种简单、模块化且廉价HAT光催化剂驱动烷基自由基的生成,它是昂贵的Ir(III)光催化剂的优良替代品。值得注意的是,通常被认为在氧化加成过程中惰性的氯代芳烃作为通用的底物参与反应,以良好的收率和广泛的官能团耐受性合成多样的偶联产物。在此,作者还展示了复杂天然产物和药物的大规模合成以及后期官能团化修饰,展示了该技术在工业和药物化学中的潜在应用价值。值得注意的是,通过该方法还可以轻松制备C-4烷基化的吡啶。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




