上海交大张兆国/吴晶晶 | 可见光诱导的脱羧烯丙基化反应合成天然产物dafachronic酸和boophiline
研究背景
Dafachronic acid 分子是存在于线虫体内的类固醇激素,这类化合物作为 DAF-12 的配体对线虫的生长发育起到了重要的调控作用,因此研究这类化合物对于农业上线虫病虫害防治以及人类的抗衰老研究具有重要的意义。Boophiline 作为一种抗菌甾醇酰胺,除了有趣的生物活性外,其 C-25 手性中心的绝对构型尚未确定。研究表明,分子侧链 C-25 位的立体化学构型是影响其生物活性的重要因素。因此,C-25 手性甲基的构筑成为了合成 dafachronic acid 分子及相关化合物的关键步骤。对于这一关键步骤,少数研究小组采用了手性砌块的策略,而大多数研究小组采用了包括 HWE 反应、Wittig 反应或 Julia 烯化反应与不对称氢化反应联用的策略。但是这些方法都需要使用化学计量的强碱(如 n-BuLi 或 t-BuOK 等),合成过程需要额外的保护和去保护步骤。因此,开发简明高效的合成路线是十分有必要的。
研究内容
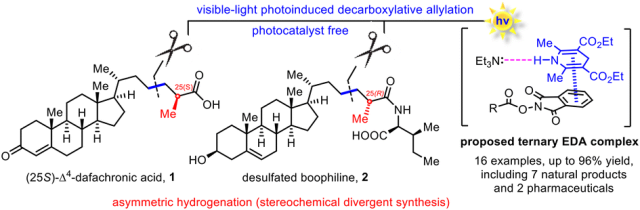
近日,上海交通大学吴晶晶与张兆国课题组以廉价易得的胆酸化合物作为原料,以可见光诱导的脱羧烯丙基化反应串联不对称氢化反应作为关键步骤,高效地合成了天然产物 (25S)-Δ4-dafachronic acid 和脱硫酸酯的 boophiline,并首次确定了 boophiline C-25 位的绝对构型。此外,新发展的可见光诱导的脱羧烯丙基化反应不仅反应条件温和,而且具有优秀的底物适用性,可以兼容许多结构复杂的天然产物和药物分子。通过机理验证实验,作者证明该反应是通过 Hantzsch 酯 (HE) 和氧化还原活性酯形成电子给受体 (EDA) 复合物进行的。
首先,作者对目标分子进行逆合成分析,对于合成的关键步骤,设计了两种策略:其一是直接的脱羧烷基化策略,即化合物 6 或 7 与含有手性甲基的化合物 5 进行脱羧烷基化反应,直接引入手性甲基;另一种有效的策略是在可见光照射下,烯丙基砜试剂 9 与氧化还原活性酯 7 发生脱羧烯丙基化反应,随后串联不对称氢化反应构筑手性甲基。
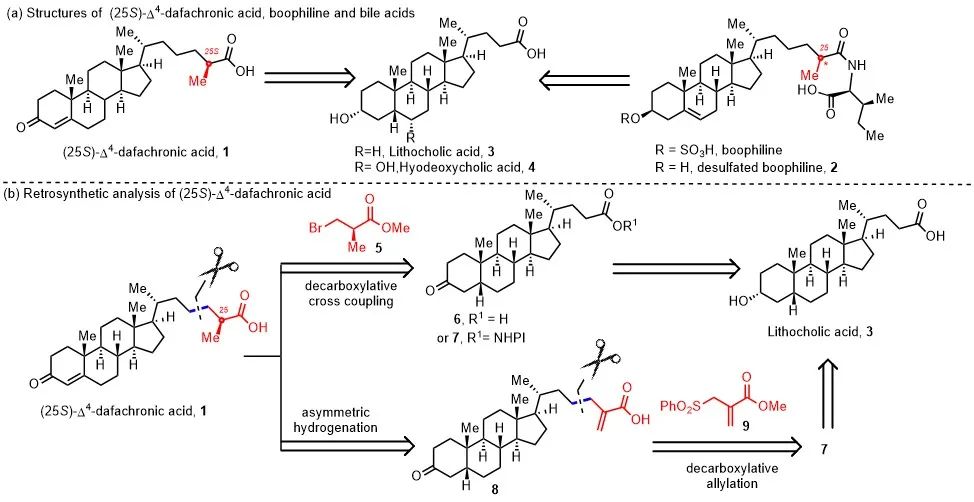
图1 逆合成分析
接下来,作者对直接脱羧烷基化策略进行尝试,对于这一策略作者尝试了 MacMillan 课题组发展的光氧化还原/镍协同催化体系:化合物 5 与 6 的发生直接脱羧烷基化反应以 30% 的收率得到了所需的产物 10。但 13C-NMR 显示,得到的产物为比例为 1 : 1 的非对映体。随后,作者尝试了金属镍催化的还原偶联反应,可以 10–12% 的收率获得目标产物 10,但是得到的产物 C-25 位手性甲基的构型也发生了部分异构化。接着作者尝试了 Baran 课题组发展的镍催化的氧化还原活性酯与有机锌试剂的偶联反应。作者将 (S)-Roche 酯转化为具有较高反应活性的锌试剂 11,并与化合物 7 进行反应,以 28% 的收率得到手性完全保留的产物。然而经过对联吡啶型双齿配体和溶剂一等系列的条件筛选,反应收率没有得到显著提高。
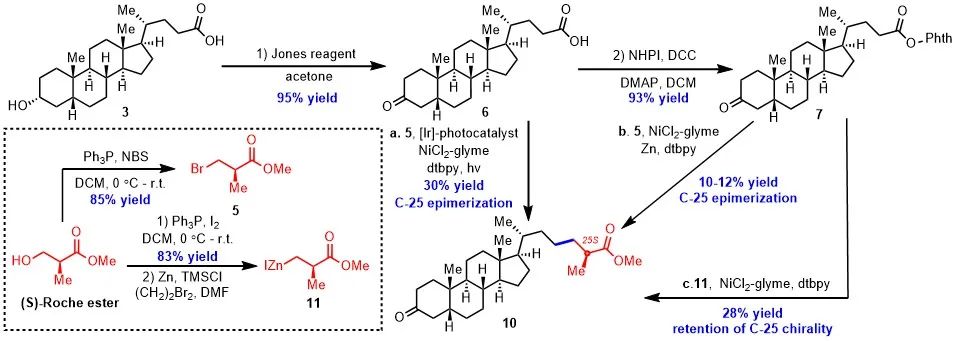
图2 通过直接脱羧烷基化策略构筑手性甲基
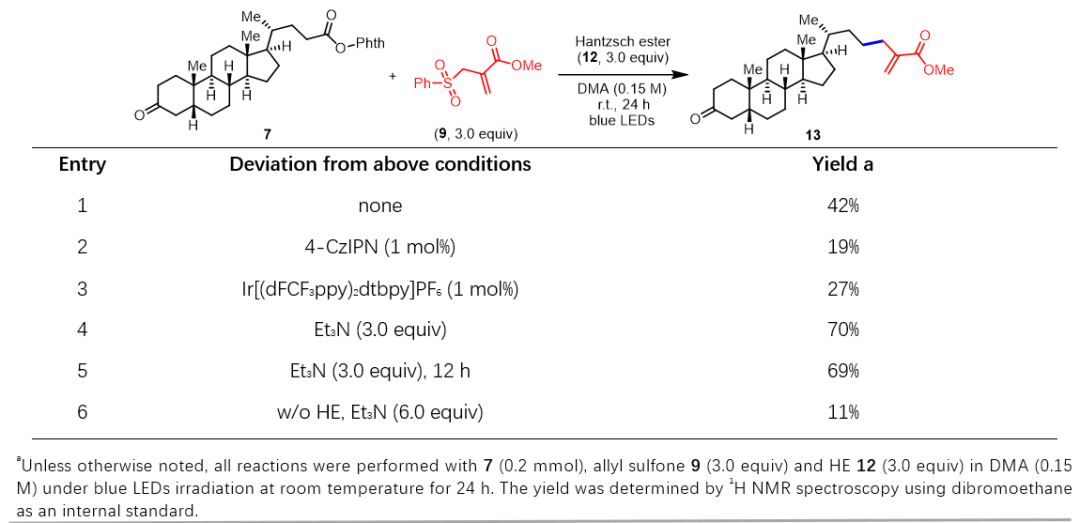
随后,作者对可见光诱导的脱羧烯丙基化策略进行了实验尝试。虽然陈以昀课题组已经通过光氧化还原催化策略报道了类似的反应,但作者希望开发一种无光催化剂参与的转化。受 Aggarwal、陈以昀以及尚睿等课题组开创性工作的启发,作者提出 Hantzsch 酯 (HE) 和氧化还原活性酯可以形成电子给受体 (EDA) 复合物,在可见光照射下生成烷基自由基,烷基自由基随后可与烯丙基砜化合物发生反应实现脱羧烯丙基化反应。具体实验中:在蓝光照射下,以 DMA 为溶剂,化合物 7 和 9 在三当量的 Hantzsch 酯存在的条件下,可以 42% 的收率得到目标产物。当在体系中加入 3 当量的三乙胺时,收率可以提高至 70%。
表1 可见光诱导的脱羧烯丙基化反应条件优化
在完成了关键步骤的探索后,作者开始了对目标分子的高效合成。首先,从石胆酸 3 出发,经过 Jones 氧化和 DCC 缩合反应,可以很容易地制备出氧化还原活性酯 7。在标准光诱导脱羧烯丙化条件下,以 69% 的收率得到了所需产物 13。化合物 13 水解后,在 NaHCO3 和 PPh3 存在下,以 (S,Sp)-RuPhox-Ru 为手性催化剂,在 20 bar H2 条件下对丙烯酸进行不对称氢化反应,可以优秀的产率 (99%) 和非对映选择性 (>20:1 d.r.) 得到目标产物手性羧酸 14。最后,化合物 14 经 IBX 氧化得到最终的目标产物 (25S)-Δ4-dafachronic acid,总路线包括六步,总收率为 29%。
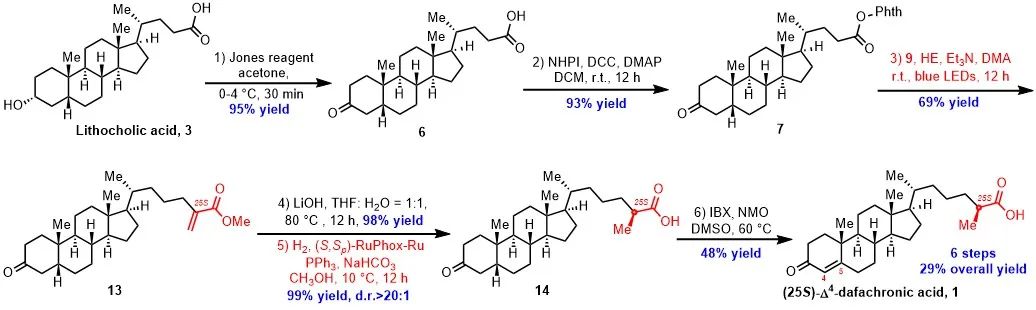
图3 6步合成天然产物 (25S)-Δ4-dafachronic acid
对于目标分子 2,作者选择以猪去氧胆酸 4 为初始原料进行合成。化合物 4 依次经过甲酯化、对甲苯磺酰基保护 C-3 和 C-6 羟基得到化合物 15。随后,该化合物在醋酸钾存在下在冰醋酸溶液中回流同时发生 6α-tosylate 消除和 C-3 Walden 翻转,得到化合物 16,产率为 61%。随后,通过连续的水解、DCC 缩合反应,可以制备氧化还原活性酯 17。在标准光诱导脱羧烯丙化反应条件下,可以 78% 的收率得到目标产物 18。接下来,化合物 18 经水解得到丙烯酸化合物 19。为确定目标产物在 C-25 位置的绝对构型,作者使用了两种构型的 RuPHOX-Ru 催化剂对化合物 19 进行了不对称氢化反应,以优异的产率和非对映选择性得到化合物 20 和 22,随后二者分别与 L-异亮氨酸反应完成最后的合成,得到两种异构体。最后,通过与天然产物分离文献中 13C-NMR 谱的比较,确定其 C-25 绝对构型为 R。总合成路线包括九步,总收率为 14%。
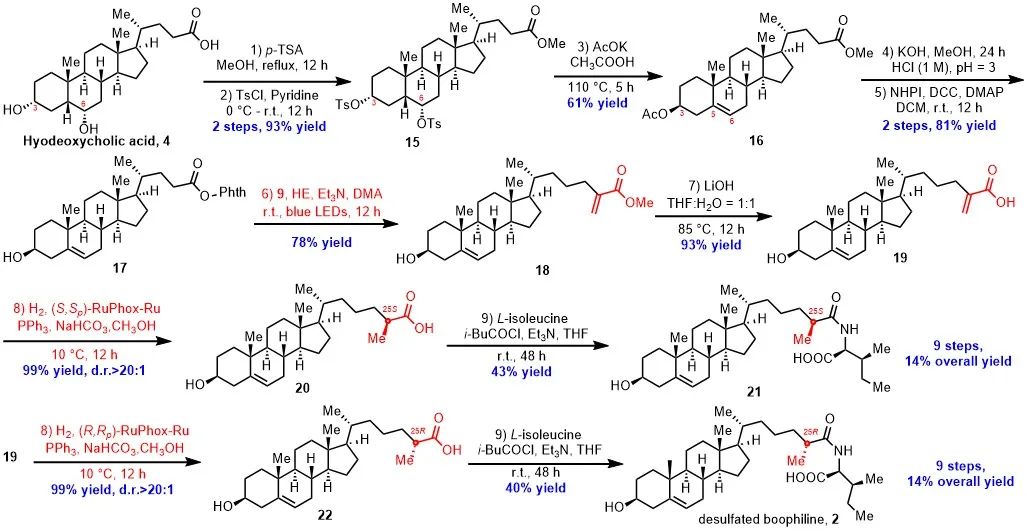
图4 9步合成天然产物脱硫酸酯 boophiline
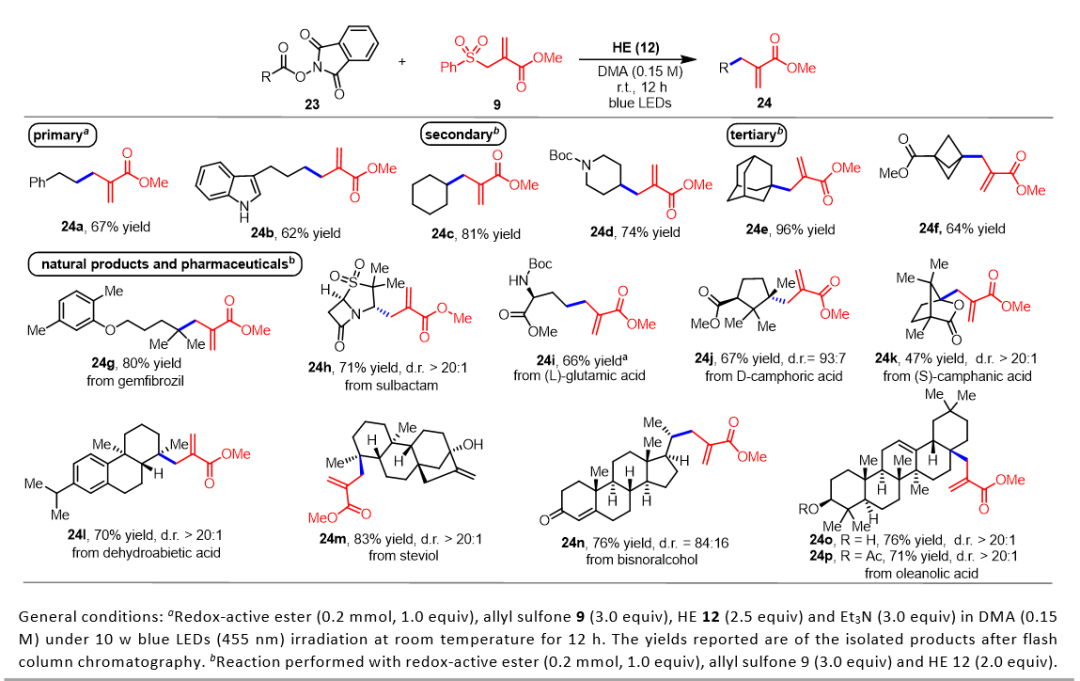
上述两个天然产物合成验证了新发展的可见光诱导的脱羧烯丙基化反应的实用性。作者认为,新发展的反应操作简便,条件温和,应该可以应用于复杂天然产物后期修饰中。于是作者首先挑选了几种有代表性的简单一级、二级、三级羧酸,进行脱羧烯丙基化研究,发现都能以中等到优秀的收率给出目标产物。进而作者利用新发展的反应,对一些复杂的药物分子和天然产物,如:舒巴坦、谷氨酸、樟脑酸、脱氢松香酸、甜菊醇、齐墩果酸等分子,进行了后期脱羧烯丙基化修饰,反应都能顺利进行,收率普遍在中等到良好,且大多数情况下都能得到较好的非对映选择性。
表2 脱羧烯丙基化反应底物拓展
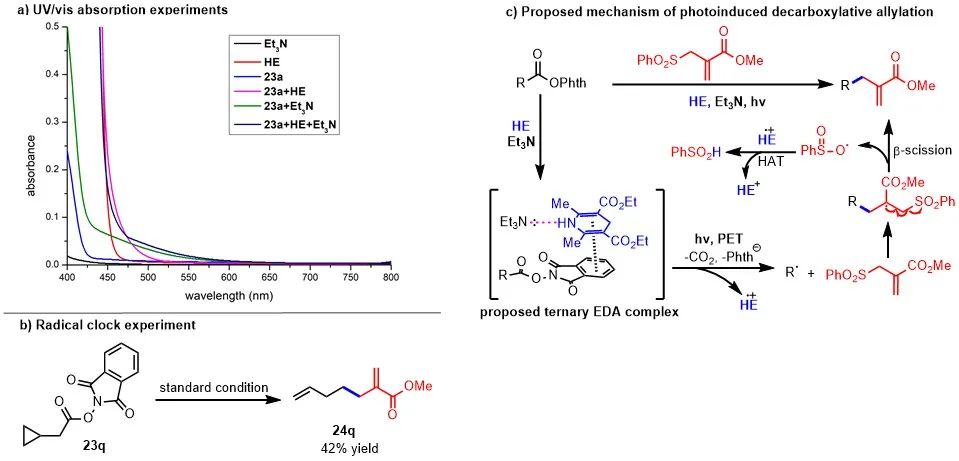
通过 UV-Vis 实验、自由基钟实验,作者对该反应的机理进行了初步验证,并提出以下可能的机理:氧化还原活性酯与 Hantzsch 酯相互作用形成 EDA 复合物,该复合物通过光致电子转移 (PET) 生成烷基自由基和 Hantzsch 酯自由基阳离子。产生的烷基自由基被烯丙基砜捕获,然后发生 β-裂解,即可得到所需的烯丙基化的产物。
总结展望
综上所述,上海交通大学吴晶晶和张兆国课题组从廉价易得的胆酸出发,以光诱导的脱羧烯丙基化策略作为关键步骤,完成了生物活性天然产物 (25S)-Δ4-dafachronic acid 和脱硫酸酯的 boophiline 的简明合成。值得强调的是,作者通过立体化学发散性合成,完成了脱硫酸酯的 boophiline 的两个非对映异构体的立体化学发散性合成,从而首次确定了 boophiline C-25 位的绝对构型。此外,作者开发的基于可见光激发 EDA 复合物的脱羧烯丙化反应,具有条件温和、操作简单、官能团耐受性广等特征,为复杂天然产物和药物分子的后期官能团化修饰提供了新的可能。
论文信息

Concise synthesis of (25S)-Δ4-dafachronic acid and desulfated boophiline enabled by photoinduced decarboxylative allylation and asymmetric hydrogenation
Xiaotong Li, Yuxuan Zhang, Zhaoguo Zhang and Jingjing Wu
Org. Chem. Front., 2024, Advance Article
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





