纽约大学Marvin Parasram课题组:光诱导下氮原子迁移的烯烃氮杂环丙烷化反应
纽约大学Marvin Parasram课题组报道了在可见光激发下,容易获得的氮氧基三氮烯可以作为氮原子源,用于邻苯二甲酰亚胺保护的烯烃的氮杂环丙烷化。这种方法避免了外加氧化剂、贵过渡金属和光催化剂的需求,并且可以实现具有不同电子构型的活化和未活化的多取代烯烃的选择性氮杂环丙烷化。值得注意的是,这一过程避免了竞争性C−H插入产物的形成。机理研究支持氮氧基三氮烯的光裂解会产生游离的单线态氮烯。此外,该方案报道了温和的光氧化还原催化保护基的N−N裂解以提供游离的氮杂环丙烷。
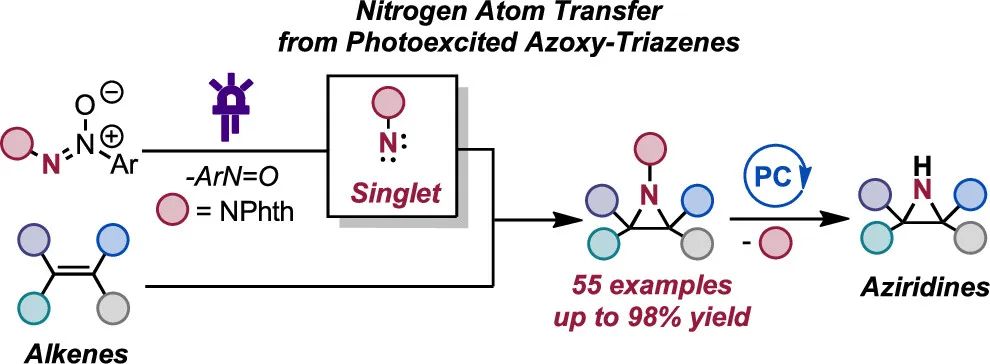
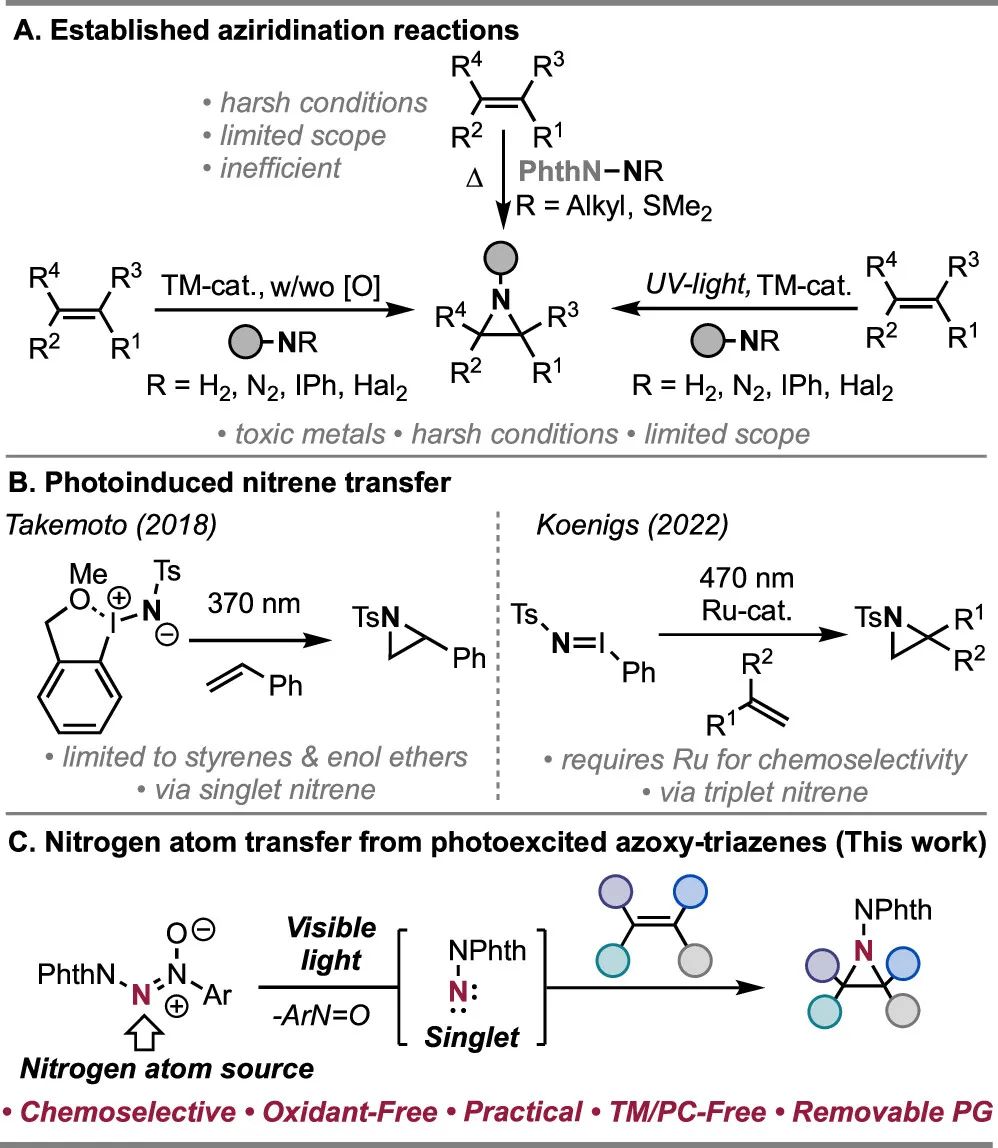
氮杂环丙烷具有27 kcal mol−1的环应变,使因而能高效实现开环下的1,2-胺-官能化转化。氮杂环丙烷核心本身在某些小治疗剂和天然产物(如抗肿瘤药物丝裂霉素Mitomycin)中发挥着重要作用。因此,获得氮杂环丙烷的创新策略仍然是合成界关注的焦点。常见的策略包括反应性nitrene中间体与烯烃的[2+1]环加成。在20世纪90年代初,Atkinson及其同事证明,邻苯二甲酰亚胺能够进行氮杂环丙烷化(方案1A)。然而,反应效率较低。在过去几十年中,已经表明,使用过渡金属可以稳定来自前体(如卤代胺、亚氨基碘和有机叠氮化物)或来自氧化条件下的胺的氮卡宾中间体(方案1A,左)。虽然每种方法都有独特的优势,但这些方法都是在苛刻的条件下进行的,并且底物范围有限。此外,值得注意的温和方法目前仍需要Rh等贵金属。
多年来,氮卡宾的光发生不断发展,过去仅限于紫外光和过渡金属进行分子间氮卡宾转移(方案1A,右),最近的进展包括直接光解或在温和的可见光条件下利用光催化剂形成游离的氮卡宾。2018年,Takemoto小组证明,特殊邻位取代的亚氨基碘的光激发可以有效地产生游离的单线态氮卡宾(方案1B,左);然而,该方法仅限于甲硅烷基烯醇醚和苯乙烯。2022年,柯尼希斯报道称,亚氨基二胺的蓝光激发可以产生三重态硝基烯的形成,从而产生烯丙基C−H插入产物(方案1B,右)。从成本角度来看,对Ru等贵金属的化学选择性的依赖可能被视为一种限制。因此,开发一种不含金属和氧化剂的氮杂环丙烷法是非常有必要的。
在此,纽约大学Marvin Parasram课题组报道了容易合成的氮氧基三氮烯,可以在直接可见光照射下形成游离的氮卡宾,从而实现烯烃的立体特异性和化学选择性氮杂环丙烷化(方案1C)。此前,该团队和其他人已经报道了使用光激发的硝基芳烃作为氧原子转移剂,从碳氢化合物中获得醇,从烯烃、醛类和亚胺中获得羰基衍生物。因此,,纽约大学Marvin Parasram课题组假设使用等电子的氮氧芳烃可能会在烯烃的可见光照射下引发氮原子转移,从而产生氮杂环丙烷。1981年,Hoesch和Koëppel报道了在苛刻的紫外光下使用偶氮氧基芳烃作为氮卡宾前体的一个例子。最近,Koenigs小组证明,甲苯磺酰基保护的偶氮氧基三氮烯可以经历直接可见光激发,导致N−S键均裂,以实现偶氮氧基向烯烃的基团转移。反过来,假设使用邻苯二甲酰亚胺脱保护的偶氮三氮烯,其N−N比N−S结合更强,可能导致邻苯二甲酸酰亚胺保护的胺在可见光照射下的氮原子转移,用于烯烃的功能化。
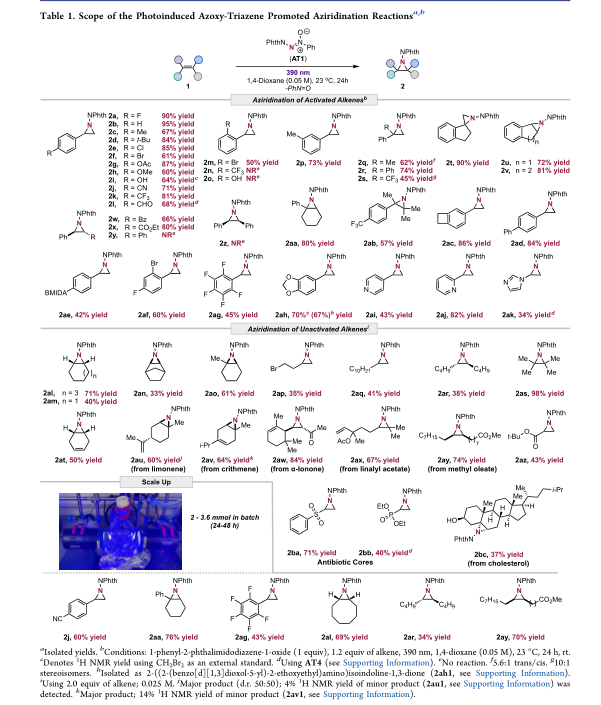
将4-氟苯乙烯(1a)和在二氯甲烷中容易合成的1-苯基-2-邻苯二甲酰亚胺二氮-1-氧化物(AT1)置于390nm的光照射下,产生了70%1H NMR产率的所需氮杂环丙烷产物(2a)。
研究发现,同时具有富电子和缺电子基团的底物获得良好到高的产率(2a−2l,2p,60−95%)。此外,易于C−H氮卡宾插入或氢原子转移的取代基如Me(1c,1p)、t-Bu(1d)、OH(1i)和CHO(1l)以高产率获得目标产物。1n和1o没有反应。二取代烯烃产生中等至优异产率(2q−2x;45−90%)的所需氮杂环丙烷化产物。值得注意的是,缺电子苯乙烯1s的氮杂环丙烷化在无金属催化的条件下是具有挑战性的;然而,在该方案下,以45%的分离产率获得了氮杂环丙烷2s。在β-取代苯乙烯中,顺式和反式二苯乙烯(1y,1z)没有反应。这可能是由于起始材料的强荧光猝灭。在反应条件下,具有挑战性的三取代(1aa)和四取代(1ab)苯乙烯以中等至良好的产率产生2aa−2ab。双环取代苯乙烯1ac以良好的产率生成2ac。其他苯乙烯如对联苯(1ad)导致84%的2ad。具有BMIDA功能手柄的底物1ae在反应条件下是可耐受的(2ae,42%)。双环取代苯乙烯1ac以良好的产率生成2ac。其他苯乙烯如对联苯(1ad)导致84%的2ad。具有BMIDA功能手柄的底物1ae在反应条件下是可耐受的(2ae,42%)。高度缺电子的苯乙烯,如1af−1ag,导致氮杂环丙烷化产物(2af−2ag)的中等产率。1ah的敏感缩醛基团,具有易于插入氮卡宾的C−H键,以良好的1H NMR产率(70%)选择性地产生氮杂环丙烷化产物2ah。由于2ah的敏感性,将产物进行乙醇裂解(2ah1)并分离。其他易于AT1荧光猝灭的底物,如杂环胺(1ai−1aj),以中等至良好的产率(43−82%)产生氮杂环丙烷产物2ai−2aj。然而,咪唑(1ak)的产率较低(2ak,34%)。
接下来,在这些条件下研究未活化的烯烃(见SI)。将环烯烃置于反应条件下可获得良好的氮杂环丙烷化产物产率(2al−2am,40−71%),而双环降冰片烯以33%的产率获得2an。具有甲基(1ao)取代基的环状三取代烯烃以中等产率(61%)产生相应的氮杂环丙烷2ao。对于非环状底物,末端和内部烯烃导致氮杂环丙烷产物的中等至优异产率(2ap−2as,35−98%)。
未活化的烯烃上考察了转化的区域选择性。环己二烯(1at)仅产生2at(50%),未检测到二氮杂环丁烷化。1au以15:1的内部烯烃(dr50:50)与末端烯烃的比例产生氮杂环丙烷化产物2au。为了研究空间位阻对烯烃反应性的影响,检测了1av,氮杂环丙烷化(2av)以4.7:1的区域异构比发生在位阻较小的烯烃上。接下来,研究了具有三取代环状和二取代线性烯烃的1aw。二取代线性烯烃的氮杂环丙烷化是检测到的唯一产物(2aw)。当测试乙酸芳樟醇酯(1ax)时,同时具有非环状内部和末端烯烃,内部烯烃的区域选择性氮杂环丙烷化以67%的产率获得(2ax)。这些区域选择性研究表明,氮杂环丙烷化对烯烃的空间分布是敏感的。顺式脂肪酯,油酸甲酯(1ay),在反应条件下得到74%的2ay。以良好至优异的产率合成了抗生素核心2ba和2bb。胆固醇(1bc)与无保护的乙醇以中等产率获得2bc。这一结果补充了现有的氮杂环丙烷方案,由于我们方案的厌氧性质,不需要保护氧化敏感基团。值得注意的是,在所有情况下,都没有检测到烯丙基C−H胺化产物,这表明这种氮杂环丙烷方法具有高度的化学选择性。为了评估该方法的可扩展性,进行了克级反应(表1)。
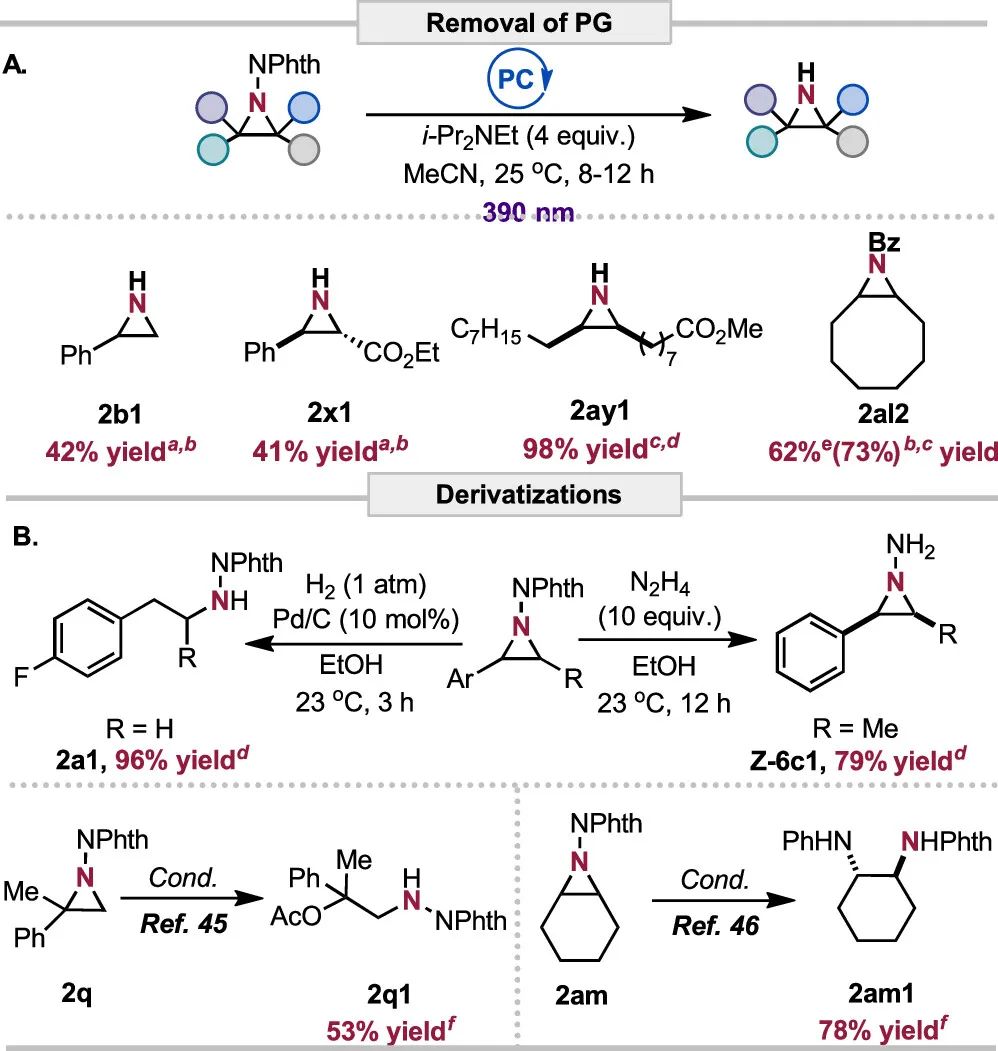
对于产率较低的底物(1m、1ai、1ak和1ap),使用光流反应器(见支持SI)可使产率提高3-5倍。就转化的合成用途而言,报道了邻苯二甲酰亚胺氮杂环丁烷(2b、2x、2ay和2al)的N−N键断裂的第一个方案,以在温和的光氧化还原催化下提供未保护或衍生的氮杂环丙烷(2b1、2x1、2ay1和2al2)(方案2A)。反应产物的其他衍生作用有:还原性(2a1,吩嗪衍生物)44和亲核性(2p1和2n1)开环,以及Z-6c的肼后处理,以提供氨基氮杂环戊烷(Z-6c1)也是可能的(方案2b)。
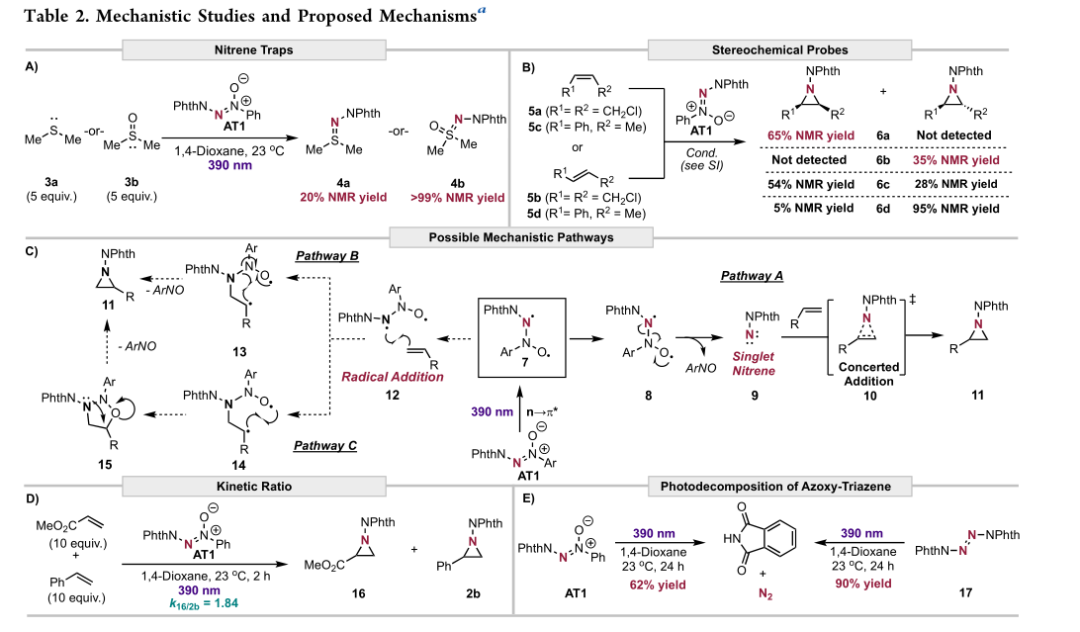
紫外-可见光谱研究表明,在反应条件下,氮氧基三氮烯是唯一的吸收物种(图S3)。对照实验(表S4;图S4)证实,持续的光照对氮杂环丙烷和氮氧基三氮烯的形成和裂解都至关重要。此外,涉及各种三重态和单重态猝灭剂的实验表明,与其他偶氮氧基芳烃系统类似,偶氮氧基三氮烯在激发时主要进入单重态(表S6)。由于该方法导致化学选择性氮杂环丙烷化,在反应过程中可能形成单重态氮卡宾中间体。为了支持这一点,独立使用了单线态氮卡宾,如二甲基硫醚(DMS,3a)和二甲基亚砜(DMSO,3b),并分别以20%和>99%的 1H NMR产率产生了捕获的产物4a和4b(表2A),有力地支持了单线态氮卡宾物种的形成。
通过使用立体化学探针(表2B),来确定对单重态nitrene形成的进一步支持,其中初始几何形状的保留表明通过单重态氮卡宾的协同机制,而消旋化支持通过三重态氮卡宾的逐步机制。在反应条件下测试未活化的烯烃,(Z)-1,4-二氯丁-2-烯(5a)和(E)-1,4二氯丁2-烯(5b),并进行浓度依赖性研究。这两种烯烃都导致立体特异性氮杂环丙烷化,从而支持单重态氮烯的形成(表2C,途径a)。值得注意的是,(Z)-和(E)-β-甲基苯乙烯(5c−5d)导致立体构型消失。这种现象可以通过苯乙烯基氮杂环丙烷产物发生光异构化的倾向来解释,使5c−5d作为探针无效(见SI)。尽管如此,通过光激发的双自由基中间体7与烯烃的逐步自由基加成(12)得到中间体13(途径B)或15(途径b)随后进行分子内裂解以产生氮杂环丙烷产物(11)。
为了确定氮杂环丙烷化是否通过途径A而不是途径B或C发生,用苯乙烯和丙烯酸甲酯进行了动力学竞争研究(表2D)。获得了k16/2a=1.84的值,这与先前关于游离邻苯二甲酰亚胺形成的报道相同。在不存在烯烃的情况下,起始氮氧基三氮烯材料的光照射提供了途径A的进一步证据,这导致邻苯二甲酸酰亚胺的显著检测,可能是通过氮卡宾二聚体1,4-二苯二甲酰基四氮烯的光裂解(17)(表2E,左)。这通过使17经受反应条件来验证,从而以90%的产率形成相应的邻苯二甲酰亚胺产物(表2E,右)。使用自由基猝灭剂、自由基时钟和Hammett研究(见SI)排除了以碳为中心的自由基中间体(13或14)的可能性。根据机制研究结果,最有可能的是路径A,其特征是单重态游离氮卡宾的光发生。
总之,纽约大学Marvin Parasram课题组已经证明,光诱导的偶氮氧基三氮烯可以实现活化和未活化烯烃的化学选择性氮杂环丙烷化。这种方法相对温和,为可持续的氮杂环丙烷化和相关的氮原子转移反应开辟了途径。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





