光诱导多组分分子内环化/羟基三氟甲基化级联反应:多官能团3,4-二氢喹唑烷酮的简便合成
导读
近日,浙江工业大学药学院谢媛媛课题组报告了一种用一锅光驱动多组分方法从基本构件中组装CF3修饰的3,4-二氢喹唑酮的模块化组装方法。在该方案中,揭示了1-(2-乙酰苯基)-3-苯基脲在成功触发分子内环化的同时,在能量转移(ENT)激活时达到反应性三重态的潜在能力。以商业上可得的2-氨基苯乙酮、对甲苯基异氰酸酯和Togni‘s II为原料,可合成药用相关的3,4-二氢喹唑啉酮类化合物,具有无金属结构和广泛的官能团耐受性。机理研究揭示了ENT介导的分子内环化和单电子转移(SET)介导的羟基三氟甲基化级联反应。密度泛函理论计算说明了这种光诱导转变的能量图景。相关研究成果发表在Green Chemistry.上(DOI: 10.1039/d3gc04653b)。
研究背景
多组分反应(MCR)在生成各种杂环中占有重要地位,显示出它们作为一种与绿色化学和以多样性为导向的合成标准相一致的合成方法的可靠性和有效性。涉及羰基和/或亚胺底物的MCR是构建复杂N-杂环的最基本的转化(例如,Mannich、Petsis、和Biginelli-type MCR)。近年来,由于光驱动自由基化学反应的引入,这一经典领域取得了快速的进展,揭示了超越传统极性反应的新的合成途径。通过光致能量转移(ENT)和单电子转移(SET)过程,产生的高活性中间体(例如离子、自由基或自由基离子)在温和的条件下促进了各种具有挑战性的化学转化。然而,它们与MCRs的集成主要限于杂环化合物的官能化。此外,利用光化学MCR方法从非杂环反应物合成杂环在很大程度上还没有被绘制出来。
N-杂环是上市药物和生物活性天然产物中普遍存在的和关键的支架。尤其是三氟甲基(CF3)修饰的N-杂环,由于其优越的性质,包括改善的物理化学特性、代谢稳定性和膜通透性,最近引起了越来越多的关注。这类支架显示出广泛的生物活性,跨越抗癌、抗艾滋病毒和抗心律失常的作用,并已成为药物化学中的优先结构(图1a)。虽然已经建立了有效的三氟甲基化策略(亲核、亲电、和自由基三氟甲基化),但通过CF3自由基(·CF3)介导的自由基加成/环化反应或N-杂环的后期三氟甲基化反应构建含CF3的N-杂环往往效率和选择性较低,并且需要复杂的原料(图1B)。在这项努力中,光诱导MCR合成方法直接生产多种CF3修饰的N-杂环,利用现成的原料资源,并表现出高的反应效率和选择性,具有重要的意义。
关于CF3修饰的N-杂环的光催化多组分构筑方面的报道还很少。在光催化反应中,芳基羰基经常用作ENT催化剂,需要高能光(∼300 nm)照射,很少直接参与反应。值得注意的是,研究表明芳基羰基的激发π→π*三重态表现出比基态更大的极性。这种激发态合成子在形成C-N键方面的合成适用性被忽视,而且远未被探索。在本文中,我们将一种激发态极性合成子应用于光诱导MCR。利用原位生成的尿素来降低芳基羰基的活化能,实现可见光照射下的ENT活化。激发态的芳基直接参与了C-N键的形成,从而促进了环化反应。随后,通过光氧化还原三氟甲基化的级联反应合成了CF3修饰的N-杂环,扩大了芳酮基三联体反应性的合成应用(图1C)。
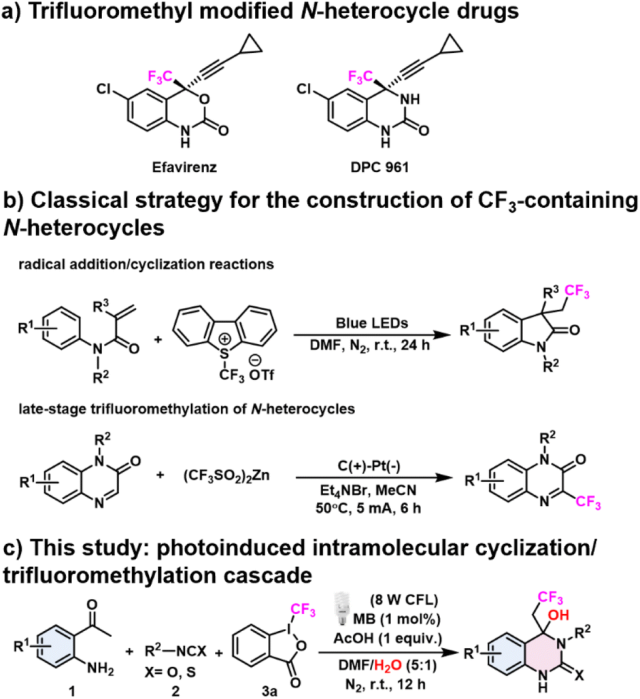
在这篇文章中,报道了光诱导的MCR反应,该反应是由ENT介导的亚甲基蓝染料与原位生成的二芳基尿素之间的分子内环化,然后经过自发脱水步骤生成烯基喹唑烷酮中间体。随后的SET过程触发·CF3的形成,经历了自由基加成和意想不到的羟化过程。这种一锅级联转化允许高效和方便地制备具有医学意义的多官能团喹唑烷酮和喹唑硫酮衍生物。
研究内容
首先,使用2-氨基苯乙酮(1a)、对甲苯基异氰酸酯(2a)和Togni的I I(3a)的多组分作为模型底物开始研究。在确定了最佳条件后,然后探索了底物的范围。
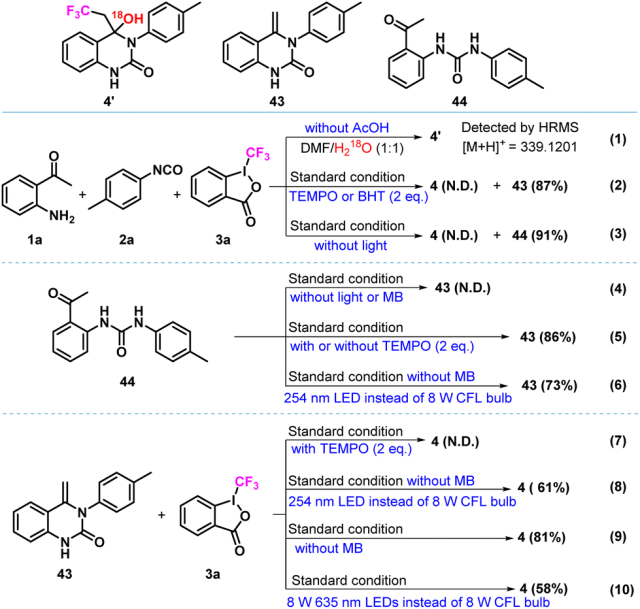
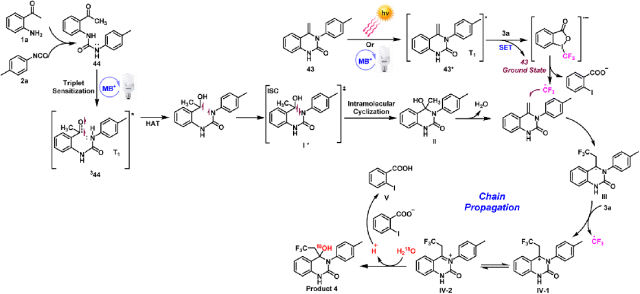
为了证实反应机理,进行了一系列对照研究,并对1a、2a和3a之间的模型反应进行了详细的研究。首先进行氧同位素标记实验,以确定产品中羟基的来源。HRMS检测到~(18)O标记的43个羟基的显著丰度信号,表明43个羟基来源于外部水。如图3所示,这种转变可能包括两个连续的光化学过程。首先,1,3-二苯基脲类似物中间体44来源于1a和2a之间的原位缩合反应,它预计会发生ENT介导的分子内环化反应,随后发生分子内脱水,最终形成喹唑烷酮类似物中间体43。对照实验表明,可见光和光敏剂对这一转化都是必不可少的,中间体43和44被分离出来,并通过核磁共振光谱进行了验证。然后,中间体43经过光诱导的羟基三氟甲基化,得到产物4a。在TEMPO存在下,反应活性被抑制,这表明这是一种自由基机制。值得注意的是,尽管没有外部光敏剂,但当使用254 nm紫外灯或CFL灯泡进行实验时,这一转移途径的反应性保持不变。显然,这种光诱导的羟基三氟甲基化是一种不同的机制。
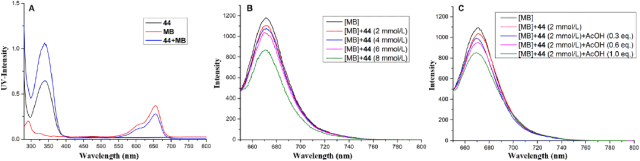
为了阐明反应机理,进行了一系列的光学研究。稳态UV-Vis吸收光谱表明,可见光(400 nm<λ≤750 nm)仅被[MB]光催化剂吸收,44与[MB]之间没有直接相互作用(λmax=341 nm,图4A中的蓝线)。通过荧光猝灭(Stern-Volmer)实验,证明了可见光照射下[MB]与44之间存在能量转移过程。如图4b和图4c所示,逐渐增加44的浓度降低了激发的[MB]的发射强度。此外,逐步加入ACoH添加剂对猝灭效果的刺激表明,ACoH促进了反应的进行。
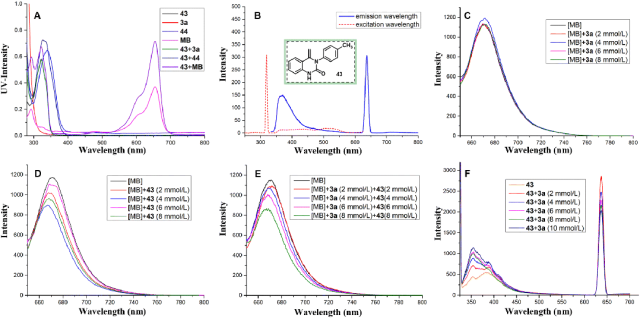
由于羟基三氟甲基化过程仍然可以在没有外部光敏剂的情况下进行,预计反应混合物中存在光活性EDA聚集的中间体。然而,没有观察到溶液的任何波长变化,也没有进一步证实光吸收基态EDA络合物(图5A)。这一令人费解的观察促使我们评估了3a光化学激活的替代途径。图5b分别显示了43在323 nm和636 nm的吸收和发射光谱。同时,如图5B中的红线所示,观察到43的弱吸收(约400-550 nm)。假设43在这一过程中可能起到光敏剂的作用。Stern-Volmer猝灭分析表明,[MB]的激发态不能被3a(图5C)或43(图5D)单独猝灭,但可以被3a和43(图5E)的组合有效地猝灭。此外,3a以剂量依赖的方式有效地猝灭了43的激发态(图5F)。这表明电子转移发生在激发态43和3a之间。
基于这些实验结果,提出了图6所示的机理。首先,可见光照射将MB激发到[MB]*。从激发的光敏剂到44的能量转移产生三联体344,它迅速经历分子内环化和分子内脱水事件,导致中间体43的形成。喹唑烷酮43从[MB]*直接吸收光或被ENT敏化后,接受电子激发,达到其激发态43*,作为光引发剂,通过SET机制,通过Togni‘s C-I键的还原断裂,触发缺乏电子的·CF3自由基的形成。3a、43和44的循环伏安图分别在−0.55V、−0.91V和−1.05V(相对于Ag/AgNO_3,在MeCN中)处显示不可逆的还原波(见图3)。Esi†中的s1)。将·CF3加到基态43得到了烷基中间体III。考虑到α-氨基烷基自由基公认的强大还原性能,中间体III预计会通过外球设定过程诱导3a的还原裂解,产生亚胺离子IV-1或碳阳离子IV-2,从而重新生成·CF3自由基。随后,亚胺离子IV的水解释放产物4。
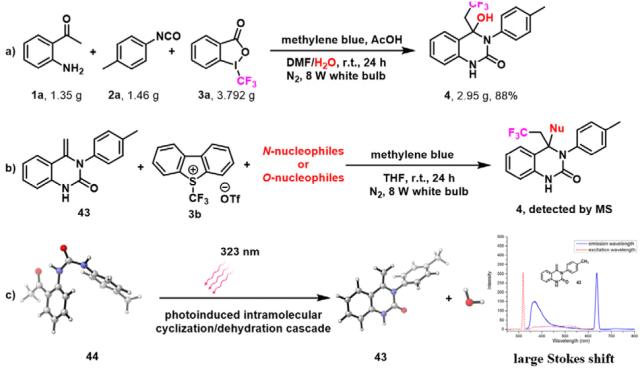
为了进一步探索目前建立的方案的适用性,对4克级的制备进行了调查。在标准条件下,当反应在10 mmol规模下进行时,产率略低(88%比小规模的87%),并且一些未反应的起始原料被回收。值得注意的是,当反应时间延长到24小时时,反应产率显著提高(88%,孤立)(图9A)。
总结展望
综上所述,本文开发了一种高效、有价值的光诱导多组分方法,可以从商业原料2-氨基苯乙酮、对甲苯基异氰酸酯和Togni‘s II中方便地获得具有药用价值的3,4-二氢喹唑啉酮类似物。该方法将极大地扩大喹唑啉酮类化合物的化学和生物空间,加速先导化合物的优化,从而促进药物的发现。此外,还揭示了1,3-二苯基脲独特的光化学行为,在光的刺激下发生不可逆的分子内环化/脱水反应。作者相信,该议定书将成为材料和生命科学领域发展一次性“光开关”的适用战略。
通讯作者:
谢媛媛- 浙江工业大学药学院
E-mail: xyycz@zjut.edu.cn, zhangchangjun@zjut.edu.cn
A photoinduced multicomponent intramolecular cyclization/hydroxytrifluoromethylation cascade: facile access to polyfunctionalized 3,4-dihydroquinazolinones
Changjun Zhang,*‡a Yuxin Ding,‡a Wenkai Huang,a Hao Zhang,a Xue Yang,a
Yuan Shi,a Hongmei Luo,a Dingyuan Loua and Yuanyuan Xie *a,b,c
DOI: 10.1039/d3gc04653b
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。





